 |
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
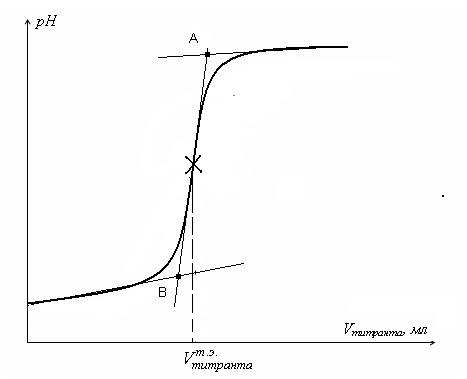
Измерение рНОдним из наиболее часто применяемых методов определения рН растворов является потенциометрический метод. Он основан на измерении электродвижущей силы (ЭДС) гальванического элемента. В таком гальваническом элементе имеются два электрода, погруженные в анализируемый раствор. Потенциал одного из электродов зависит от концентрации, а точнее от активности ионов водорода в растворе. Этот электрод называется измерительным или индикаторным. Потенциал второго электрода постоянен и не зависит от концентрации ионов водорода, он называется электродом сравнения. ЭДС гальванического элемента равна разности потенциалов двух электродов и соответственно она связана с концентрацией определяемых ионов, и эту ЭДС можно измерить. В качестве измерительного электрода для определения рН наиболее широкое применение нашел стеклянный электрод. В качестве электрода сравнения чаще всего используется хлорсеребряный электрод. Потенциометр измеряет значение ЭДС этого гальванического элемента. Потенциометрический метод широко используется в биологии и медицине для измерения рН биологических жидкостей (желудочного сока, мочи, крови, кровезаменителей и др.). Кроме того, можно измерять рН при проведении реакции нейтрализации по мере добавления кислоты к щелочи или наоборот. Этот метод называется потенциометрическим титрованием. При нейтрализации кислоты щелочью при добавлении первых порций раствора титранта рН изменяется мало, но вблизи точки эквивалентности рН повышается резко от незначительного прибавления раствора щелочи. После точки эквивалентности рН меняется опять незначительно. Результаты титрования представляют графически в виде кривой потенциометрического титрования (рис. 6.1). На оси абсцисс откладывают число миллилитров раствора щелочи в последовательные моменты титрования, а на оси ординат – соответствующую величину рН (или ЭДС). Для нахождения точки эквивалентности продолжают линейные участки кривой титрования, как показано на рис.6.1. Затем проводят прямую через участок резкого увеличения рН. Полученный отрезок АВ делят пополам, опускают перпендикуляр на ось абцисс (см. рис.). Находят объем титранта в точке эквивалентности.
Рис. 6.1. Кривая потенциометрического титрования
Расчет концентрации кислоты по результатам титрования производят по закону эквивалентов (см. работу 1):
Преимущества потенциометрического метода определения рН и потенциометрического титрования заключаются в следующем. Во-первых, рН определяется более точно, чем с помощью индикаторов. Во-вторых, можно определять рН и проводить титрование в окрашенных и мутных средах. В-третьих, точка эквивалентности при потенциометрическом титровании определяется по кривой титрования более точно, чем по изменению окраски индикатора, в этом случае исключен субъективный фактор оценки цвета раствора.
Дата добавления: 2015-01-12 | Просмотры: 1386 | Нарушение авторских прав |
 .
.