|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Альтернативные методы лечения локализованного рака предстательной железыКриотерапия. Предстательная железа замораживается с помощью нескольких криозондов, введенных чрез кожу под контролем УЗИ (рис. 10). Принято использовать пять зондов: два вводят спереди и медиально, два сзади и латерально и один - сзади. Большинство авторов рекомендуют проводить два цикла замораживания и оттаивания. Если верхушка предстательной железы не попала в зону замораживания во время сеансов, во время извлечения зондов проводят третий цикл замораживания-оттаивания. Температура по краям замороженного участка колеблется от 0 до -2о С. Поскольку клетки погибают при температуре от -25 до -50о С, на самом деле разрушается несколько миллиметров ткани внутрь замороженного участка и точно определить границы деструкции по УЗИ невозможно. После двукратного замораживания-оттаивания разрушается более обширный участок. Теоретически при этом границы некроза приближаются к границам замороженного участка. Рис. 10. Криотерапия при раке предстательной железы. Лазеротерапия. Основана на трансформации световой энергии лазерного луча в тепловую, в результате чего температура внутри железы может на несколько секунд достигать 60о С. На фоне этой температуры возникает денатурация белковых структур клеток и гибель. Глубина проникновения светового лазерного луча зависит от длины волны. Открытие гибких световодов позволило более точно подводить и фокусировать лазерный луч на предстательной железе. Sander и Beisland впервые применили неодимовый лазер (Nd:YAGLaser) для лечения больных с локализованным раком простаты. Излучение этого лазера продуцирует равномерную коагуляцию на глубине 3-4 мм. Зона некроза покрывается фибрином с минимальным рубцеванием. Гипертермия является методом термической деструкции различных тканей, предположительно обладающим селективным цитотоксическим действием на опухолевые клетки. Хотя до конца механизм подобного действия не определен, существует теория о разрушающем воздействии повышенной температуры на измененные опухолевые сосуды. Кроме того, на опытных моделях выявлена повышенная чувствительность именно опухолевых клеток к повышению температуры. При РПЖ локальная гипертермия может быть выполнена с использованием трансректального доступа. По данным других авторов, у ряда пациентов с РПЖ после проведения гипертермии простаты отмечено прогрессирование заболевания, что, однако, может быть обусловлено недостаточно тщательным отбором пациентов для данного метода. Гипертермия как вспомогательный метод лечения пациентов с локализованным раком простаты может быть допустим на ранней стадии опухолевого процесса. На сегодняшний день практически невозможно оценить истинную эффективность методики, так как ни в одном из исследований гипертермия не была проведена в самостоятельном варианте в качестве основного вида лечения. Высокоинтенсивная сфокусированная ультразвуковая аблация простаты (HIFU) – один из малоинвазивных методов лечения рака предстательной железы (рис. 11).
Рис. 11. Этапы проведения HIFU- терапии. Исследования по изучению воздействия сфокусированных ультразвуковых волн были начаты в 1989 году во Франции, в Лионе. В течение 10 лет метод проходил клинические испытания и получил европейский сертификат. В Европе этим методом пролечено уже более 9000 больных раком простаты. HIFU используется не только в европейских странах (Франции, Германии, Италии и др.), но и в Канаде, Южной Корее. В настоящее время проходят испытания в США. HIFU-терапия показана больным локализованным раком простаты стадии Т1-Т2, которым не может быть проведена радикальная простатэктомия (по возрасту, соматическому статусу) или в случае отказа больного от оперативного вмешательства по тем или иным причинам. Методика также может использоваться у больных с местным рецидивом после наружной лучевой терапии и радикальной простатэктомии. Операция выполняется в положении на правом боку под спинальной анестезией на специально оборудованном столе фирмы EDAP (рис. 12).
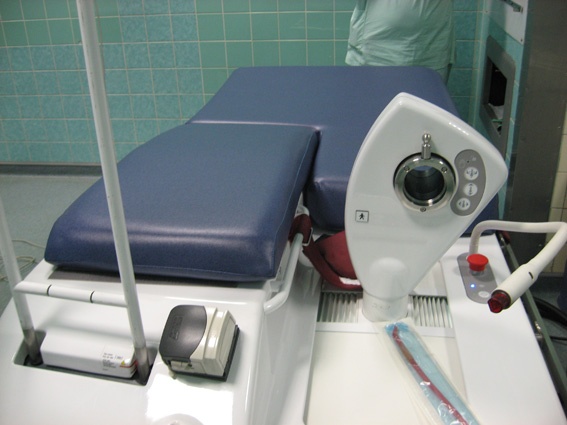
Рис. 12. Стол для проведения HIFU-терапии. Через прямую кишку устанавливается датчик, излучающий высокоинтенсивные, конвергирующие (сходящиеся) ультразвуковые волны. В определенной точке, где происходит фокусирование лучей, повышается температура (от 85 до 100о С), разрушающая клетки, и возникает эффект кавитации. Зона разрушения при каждом воздействии - 24 мм по высоте и менее 2 мм в диаметре. Повторяя импульсы и одновременно перемещая датчик, специалист последовательно разрушает всю ткань предстательной железы с опухолью (для этого требуется примерно 400-600 импульсов). Процедура занимает около 2-3 часов. Непосредственно после воздействия агрессивных ультразвуковых лучей развивается отек ткани предстательной железы за счет некроза, что требует постоянного дренирования мочевого пузыря на период в среднем 7 дней. Для этого в мочевой пузырь устанавливается по уретре катетер или в некоторых случаях ставится цистостома. Почти всем больным перед сеансом HIFU-терапии выполняется трансуретральная резекция простаты. Эта операция выполняется в один день непосредственно перед сеансом HIFU. Без разреза, через мочеиспускательный канал специальной петлей удаляется часть предстательной железы – так как это делается при аденоме простаты. Трансуретральная резекция (ТУР) простаты перед сеансом HIFU уменьшает объем предстательной железы, что делает последующую HIFU-терапию более радикальной. С предварительной ТУР предстательной железы процент осложнений после лечения, связанных с расстройствами мочеиспускания, значительно снижается. Сразу после HIFU происходит пик нарастания ПСА, а затем в течение 3 месяцев уменьшение его до 0,1 нг/мл. Абсолютными противопоказаниями являются выраженный проктит после лучевой терапии, утолщенная стенка прямой кишки (более 4 мм), пациенты после брахитерапии, предшествующие свищи в прямой кишке, инвазия опухоли в прямую кишку, отсутствие прямой кишки и ряд пациентов после лучевой терапии со склеротическими изменениями в органах малого таза.
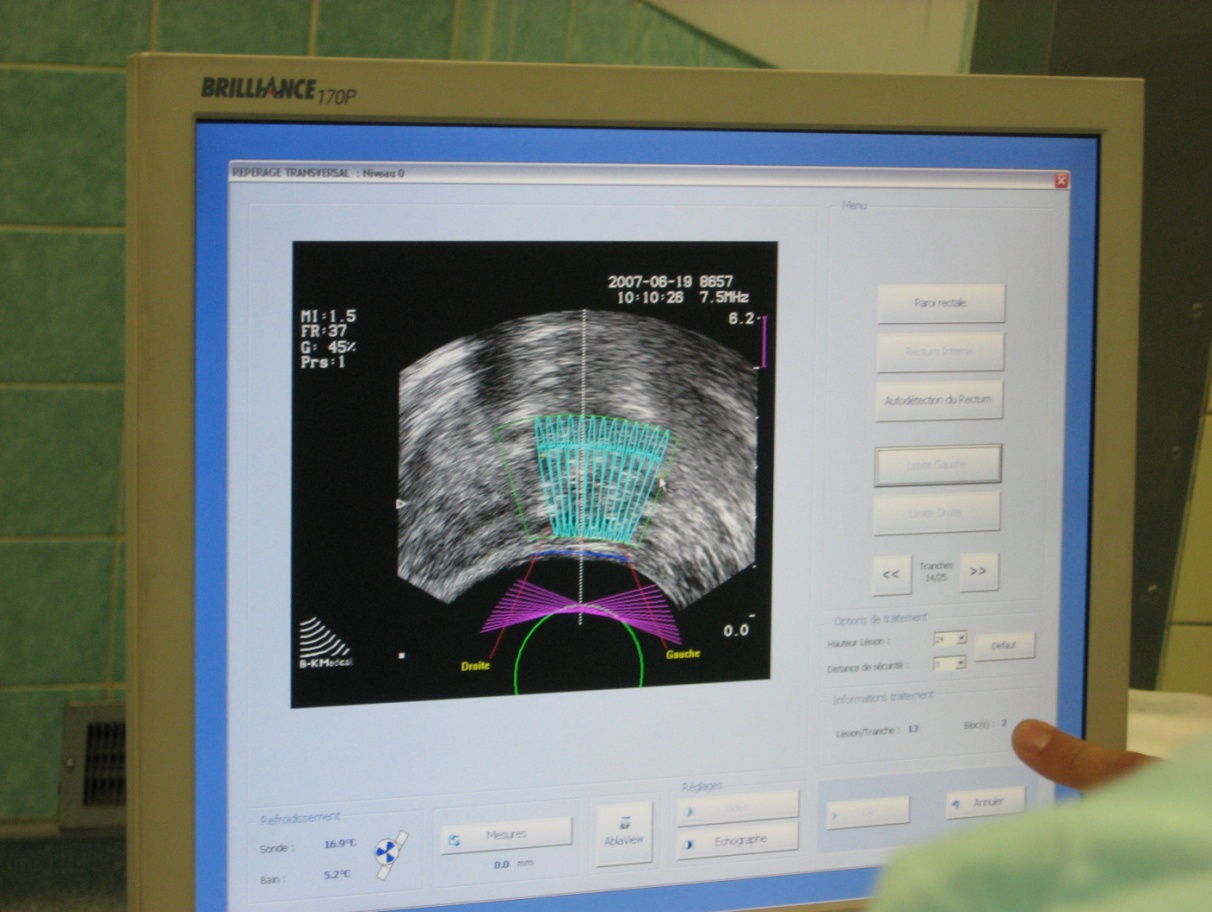
Рис. 13. Рабочее место врача. Сеанс HIFU-терапии. Для точного определения показания или противопоказания к HIFU-терапии необходимо предварительное трансректальное ультразвуковое исследование (рис. 13) и другие общепринятые обследования при раке простаты. Прогноз лечения зависит от степени онкологического риска, который устанавливается по данным проведенного обследования. 1.13.7. Особенности лечения местно распространенного (T3-4N0M0 или T1-4N1M0) и диссеминированного рак предстательной железы Основное место в лечении местно распространенного (T3-4N0M0 или T1-4N1M0) РПЖ принадлежит гормонотерапии и лучевой терапии. Большинству больных раком предстательной железы с Т3 проводят неоадьювантную гормональную терапию с последующей лучевой терапией при необходимости. Сочетание 2-х методов значительно улучшает результаты лечения и безрецидивную выживаемость. В стадии Т3-Т4 рекомендуется СОД 70 Гр на предстательную железу и 44-50 Гр на таз. При конформном (3D) облучении СОД может быть 76 Гр и больше без риска увеличения осложнений. Увеличение дозы лучевой терапии улучшает отдаленные результаты лечения. Облучение регионарных лимфатических узлов проводится во всех случаях, кроме тех, когда отсутствие метастазов в тазовых лимфоузлах доказано морфологически (pN0). Подробнее схемы гормонотерапии приведены далее. Основное место в лечении диссеминированного РПЖ принадлежит гормональной терапии. Цель гормонального лечения рака предстательной железы - увеличение показателей выживаемости и улучшения качества жизни больных. Гормонотерапию как самостоятельный вариант проводят с паллиативной целью, но гормонопрепараты могут быть использованы в сочетании с радикальным оперативным и лучевым лечением как комбинированная противоопухолевая терапия. В основе механизма действия эндокринного лечения лежит снижение концентрации тестостерона в клетках предстательной железы, которое может быть реализовано двумя механизмами: 1) подавление секреции андрогенов яичками (достигается снижение уровня сывороточного тестостерона); Дата добавления: 2015-02-05 | Просмотры: 1073 | Нарушение авторских прав |