|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Гематологигеские показатели плода при гемолитшеской болезни разлитой степени тяжести
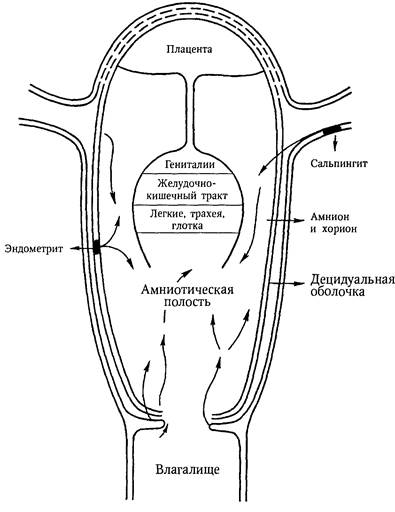
Оценка степени тяжести позволяет определить тактику ведения изоиммуни-зированной беременности, обосновать необходимость внутриматочного лечения и оптимального времени досрочного родоразрешения. Содержание общего белка и альбумина в плазме крови плодов по мере увеличения срока беременности при неосложненной беременности увеличивается. Концентрация альбумина с 20-й по 37-ю неделю увеличивается почти в полтора раза, достигая к концу беременности величины 35 г/л. При развитии у плодов тяжелой анемии, особенно при формировании отека, содержание альбумина в крови плода снижается, что позволило разработать новый патогенетический метод лечения тяжелых форм гемолитической болезни плода с использованием препарата альбумина. Отечная форма гемолитической болезни может развиваться уже в течение II триместра беременности, и, в этом случае, практически 100% таких плодов погибают антенатально до 30-й недели беременности. Тем не менее, даже при отечной форме плода показатели красной крови могут быть успешно корригированы. Однако при проведении переливания только отмытых эритроцитов донора, несмотря на полную нормализацию показателей крови у плода, отек разрешается после первого переливания лишь у 33% плодов. Поэтому в настоящее время разработан метод сочетанного переливания плоду отмытых эритроцитов донора и 20% раствора альбумина в соотношении 5:1. Такая терапия приводит к исчезновению выраженного отека у всех плодов. При этом происходит нормализация как показателей красной крови, так и содержания сывороточного альбумина. Так как до настоящего времени этиопатогенетических методов лечения гемолитической болезни плода в начальной стадии развития не существует (нет убедительных данных о положительном влиянии на течение заболевания у плода каких-либо медикаментозных средств или процедур), то сегодня можно утверждать, что основным методом легения тяжелых форм гемолитшеской болезни плода является проведение ему внутриматоъных переливаний отмытых эритроцитов донора в соъетании с альбумином под ультразвуковым контролем. Например, при отсутствии отека у плода после переливания наблюдается полная нормализация показателей его крови, в частности, гематокрит повышается в среднем в 1,9 раза. Даже при тяжелейшей гемолитической анемии на фоне развившегося отека у плода этот метод позволяет осуществить полную коррекцию анемии при увеличении значений гематокрита в 3 раза. При л е ч е н и и рано развившейся тяжелой формы гемолитической болезни требуются неоднократные внутрисосудистые переливания плоду. В Н И И А Г им. Д. О. Отта Р А М Н имеется собственный опыт 5-кратных переливаний одному ЧАСТЬ 2 ПАТОЛОГИЧЕСКОЕ АКУШЕРСТВО плоду и 10-кратных у одной беременной при двуплодной беременности. Опыт трансфузий отмытых эритроцитов донора и одновременно 20% раствора альбумина свидетельствует о том, что своевременное их выполнение позволяет существенно пролонгировать течение беременности на фоне удовлетворительных показателей крови плода и производить родоразрешение близко к сроку родов. При ведении подобных пациентов следует стремиться к родоразрешению при сроке беременности 36-37 недель. Для успешного внутриматочного лечения тяжелых форм гемолитической болезни плода важно своевременное обращение беременных женщин высокого риска по развитию этого заболевания в специализированный перинатальный центр. Общеизвестны данные, которые свидетельствуют: при обращении женщин в центр до 18 недель беременности все внутриматочные переливания были предприняты до развития у плода отека. При позднем обращении — после 24 недель беременности у 81% женщин лечение начиналось уже на фоне имеющегося отека плода. Таким образом, особая роль в обеспечении хороших результатов терапии гемолитической болезни принадлежит женской консультации. Риск осложнений, непосредственно связанных с диагностическими вмешательствами при проведении только кордоцентеза, незначительно превышает 1%. Общие потери плодов за время беременности и раннего неонатального периода не превышают при этом популяционного уровня. При проведении длительных внут-риматочных вмешательств — а именно такими являются трансфузии — риск, естественно, повышается Это связано с тремя основными причинами: 1. Вмешательства проводятся на фоне исходно патологического состояния плода. 2. На сердечно-сосудистую систему плода оказывается существенная нагрузка введением объемов крови, сопоставимых, а иногда и превышающих общий фетоплацентарный объем циркулирующей крови. 3. Двигательная активность плода существенно затрудняет выполнение длительных внутриматочных манипуляций. Контроль за состоянием плода во время вмешательства, во избежание перегрузки его сердечно-сосудистой системы и развития тяжелой брадикардии, проводится путем постоянного кардиомониторного наблюдения за сердечным ритмом. При появлении признаков нарушений функционального состояния плода следует уменьшать скорость трансфузии вплоть до ее полного прекращения. Это особенно важно при отечной форме гемолитической болезни, поскольку развитие отека обусловлено сердечно-сосудистой недостаточностью, формирующейся на фоне нарушения плодово-плацентарной циркуляции. Двигательная активность плода значительно усложняет условия выполнения переливаний и может явиться причиной тяжелых повреждений сосудов пуповины и органов плода. Для обездвиживания плоду внутрисосудисто вводится мио-релаксант пипекуроний (ардуан). Ардуан не оказывает влияния на частоту сердечных сокращений плода и в дозе 0,1 мг на 1 кг расчетной массы плода вызывает полное его обездвиживание в течение 40-50 минут. Обездвиживание плода позволяет сократить длительность внутриматочных вмешательств, значительно снизить частоту случаев выхода конца пункционной иглы из просвета сосуда пуповины и, следовательно, избежать трансфузии крови донора в амнио-тическую полость и необходимости выполнения повторных кордоцентезов в целях продолжения переливания. Течение беременности при изосерологигеском конфликте. Течение беременности отличается большим числом осложнений, к которым относятся: невы- Раздел 4. Патология плода и новорожденного нашивание за счет увеличения частоты самопроизвольных выкидышей (13%) и преждевременных родов (до 10%), анемии, ОПГ-гестозов, кровотечений в последовом и раннем послеродовом периодах. Повышается число гнойно-септических заболеваний у матерей и новорожденных. Гемолитигеская болезнь новорожденного. Значительный гемолиз эритроцитов плода, как правило, приводит к развитию тяжелой формы гемолитической болезни, завершающейся антенатальной гибелью плода или смертью ребенка в первые часы жизни из-за сердечно-легочной недостаточности. Однако в большинстве случаев заболевание быстро развивается после рождения, чему способствует поступление большого количества антител в кровь ребенка при нарушении целостности сосудов плаценты, а также повышение конглютинаци-онной активности крови ребенка. Значительную роль в патогенезе ГБ играет пониженная ферментативная активность печени новорожденного. В норме в ретикулоэндотелиальных клетках в результате гемолиза эритроцитов из гемоглобина образуется свободный (или непрямой) билирубин, который далее в печени при участии системы ферментов, из которых основным является глю-куронилтрансфераза, соединяется с глюкуроновой кислотой и превращается в конъюгированный (или прямой) билирубин. Последний хорошо растворяется в воде и выводится печеночными клетками в желчные протоки, а затем удаляется с мочой и калом. У новорожденных в первые дни жизни активность ферментов печени еще низкая, и даже физиологический гемолиз приводит к накоплению в крови повышенного количества свободного билирубина (физиологическая гипербилиру-бинемия) и к так называемой физиологической желтухе новорожденных. При гемолитической болезни, когда интенсивный гемолиз наслаивается на пониженную способность печени трансформировать билирубин, происходит патологическое накопление в крови новорожденного свободного непрямого билирубина. Свободный билирубин циркулирует в крови в виде комплексов с альбумином, в таком состоянии он не проникает через клеточные мембраны. При значительном накоплении прямого билирубина его связи с альбумином нарушаются, и он легко проникает из сосудистого русла через клеточные мембраны в ткани, особенно в ткани, богатые липидами, — жировую, нервную. Переходу билирубина в ткани способствуют недостаточное количество альбумина, сдвиг кислотно-основного состояния в сторону ацидоза, наличие в крови повышенного количества веществ — конкурентов билирубина при связывании с альбумином (гормоны, свободные жирные кислоты, салицилаты, сульфамиды и др.). В клетках нервной системы билирубин проявляет свое токсическое действие, нарушая процессы клеточного дыхания. Это приводит к расстройству функций центральной нервной системы, т. е. к развитию клинических симптомов билиру-биновой энцефалопатии (ядерная желтуха), в результате чего могут наступить или смерть ребенка, или стойкие неврологические нарушения, сохраняющиеся на всю жизнь. К л и н и ч е с к а я к а р т и н а. Гемолитическая болезнь новорожденного имеет следующие варианты течения: 1) гемолитическая анемия без желтухи и водянки; 2) гемолитическая анемия с желтухой; 3) гемолитическая анемия с желтухой и водянкой. Гемолитигеская анемия без желтухи и водянки (а н е м и ч е с к а я ф о р - ма) в чистом виде встречается редко. Анемия выявляется, как правило, на 2-й и 3-й неделе жизни и быстро прогрессирует. Количество эритроцитов снижается ЧАСТЬ 2. ПАТОЛОГИЧЕСКОЕ АКУШЕРСТВО до 2 х 1012/л, гемоглобина — до 60-80 г/л. Анемия связана не с усиленным гемолизом эритроцитов, а с подавлением функции костного мозга. При анемической форме заболевания нет ретикулоцитоза, эритробластоза, гипербилиру-бинемии. Анемия является нормохромной или гипохромной и относительно микроцитарной. Прогноз благоприятный. Гемолитигеская анемия с желтухой (ж е л т у ш н а я ф о р м а) встречается наиболее часто. Она может иметь легкое течение с умеренным, но длительным повышением уровня билирубина без увеличения печени и селезенки, но часто с последующей умеренной анемией. Легкая форма заболевания чаще наблюдается при несоответствии крови матери и ребенка по групповым антигенам системы АВО. Тяжелая желтушная форма гемолитической болезни иногда выявляется уже при рождении ребенка: его кожные покровы бледно-желтушные, печень и селезенка увеличены, мышечный тонус и рефлексы снижены, недостаточно активен крик. Даже при тяжелом течении болезни ребенок при рождении может выглядеть здоровым, розовым, однако уже в первые часы жизни появляется желтуш-ность кожных покровов, которая быстро усиливается. Ребенок становится сонливым, вялым, снижаются мышечный тонус и рефлексы, нарушается активность сосания и далее, если не начать активное лечение, развиваются отчетливые симптомы билирубиновой энцефалопатии или ядерной желтухи. Первыми симптомами являются снижение активности сосания и изменение мышечного тонуса — появление ригидности затылочных мышц. Затем присоединяются гиперестезия, беспокойство, вскрикивания, глазодвигательные нарушения («симптом заходящего солнца»), судороги, расстройство дыхания, сердцебиения, резкое повышение температуры до 40-41 °С (пирогенное действие билирубина) и наступает смерть. В агональном периоде нередко отмечают геморрагические явления — кровоизлияния в кожу, кишечник, легкие. Перед смертью может развиться отек легких и пневмония, чаще геморрагического характера. В некоторых случаях после ядерной желтухи наступает выздоровление, все симптомы исчезают, ребенок становится активным, хорошо сосет, увеличивается масса тела. Однако в большинстве случаев в дальнейшем выявляются неврологические последствия: от небольших моторных нарушений (координация движений, походка) до значительных расстройств, сочетающихся с глухотой и нарушением интеллекта. В клинической картине тяжелой желтушной формы гемолитической болезни степень анемизации ребенка к моменту рождения не имеет решающего прогностического значения. Основным показателем тяжести заболевания является интенсивность прироста билирубина в крови. При гемолитигеской анемии с желтухой и водянкой (отечная форма) плод чаще погибает внутриутробно. Это наиболее тяжелая форма заболевания. Если плод не погибает, то ребенок рождается преждевременно и имеет характерный внешний вид: бледные слизистые оболочки и кожные покровы, видны петехии и геморрагии. Обращает на себя внимание большой живот вследствие асцита и увеличенных печени и селезенки. В крови число эритроцитов не превышает 1,5 х 1012/л, содержание гемоглобина до 80 г/л, значительно увеличено число ядерных форм эритроцитов («фетальный эритробластоз»). Помогает в диагностике положительный прямой тест Кумбса, доказывающий наличие фиксированных эритроцитами ребенка блокирующих антител, указывает на резус-конфликт. Об этом же свидетельствует уровень билирубина в пуповинной крови, превышающий 51 мкмоль/л (по Ван-ден-Бергу), наличие Раздел 4 Патология плода и новорожденного анемии, нормобластов и ретикулоцитоз. Для постановки диагноза большое значение имеет анамнез матери (указания на самопроизвольные аборты, мертво-рождения, смерть ребенка от желтухи в первые дни после рождения). Лечение желтушной формы гемолитической болезни направлено на борьбу с гипербилирубинемией и предотвращение развития билиру-биновой энцефалопатии. Наиболее эффективным способом снижения уровня билирубина является заменное переливание крови. Показаниями к нему у доношенных детей являются положительная проба Кумбса, содержание гемоглобина ниже 90 г/л, билирубина 342 мкмоль/л, темп нарастания (в час) билирубина выше 6,0 мкмоль/л и уровень его в пуповинной крови 60 мкмоль/л. Сущность его состоит в том, чтобы заменить кровью донора кровь ребенка, содержащую неполноценные, гемолизированные эритроциты, иногда и свободные антитела и, главным образом, продукты распада гемоглобина (билирубин). Кровь донора временно выполняет обычную функцию крови. Собственное кроветворение ребенка в первое время подавляется. Для заменного переливания крови раньше применяли только резус-отрицательную кровь. Далее было показано, что в крови ребенка почти не содержится свободных антител, они преимущественно связаны с эритроцитами и, следовательно, возможно применение для переливания менее дефицитной резус-положительной крови. Это испытано и широко применяется, но в самых тяжелых случаях болезни предпочтительнее применять резус-отрицательную кровь. При АВО несовместимости используется кровь группы 0(1), совпадающая с кровью ребенка по резус-фактору. Количество переливаний крови определяется из расчета 150-160 мл на 1кг массы,, в среднем при операции вводится 500 мл крови донора, выводится такое же количество крови ребенка (или на 50 мл меньше). Если после первого заменного переливания крови желтуха продолжает нарастать, уровень билирубина снова повышается до величин, близких к критическим, требуются повторные заменные переливания крови. Для борьбы с гипербилирубинемией используют гемосорбцию, наибольшая эффективность которой отмечена при выполнении ее через 12-24 ч после за-менного переливания крови в количестве 2 ОЦК. К о н с е р в а т и в н о е л е ч е н и е гемолитической болезни включает внутривенное капельное введение белоксодержащих растворов с глюкозой (раствор альбумина 10%, фенобарбитал, зиксорин, после 5-7-го дня — карболен, витамин Е). При развитии синдрома «сгущения желчи» необходимо назначить внутрь 5-10% раствор магния сульфата по 5 мл 2-3 раза в сутки, облучение ребенка лампами дневного света. Фототерапия — облучение ребенка источниками света с длиной волны 450 нм, что приводит к образованию изомера билирубина, растворимого в воде, поэтому легко элиминируемого из организма ребенка. Кормление детей с гемолитической болезнью молоком матери можно начинать не ранее 5-10-го дня жизни. Дети, получившие лечение своевременно, в дальнейшем хорошо развиваются. При развитии ядерной желтухи в дальнейшем обнаруживается органическое поражение Ц Н С, отставание в психическом развитии. П р о ф и л а к т и к а. В настоящее время общепризнанна необходимость профилактического введения анти-О-гаммаглобулина после родоразрешения (постнаталь-н о) неиммунизированных Rh-отрицательных ж е н щ и н по 300 мкг (1500 M E) в т е ч е -ние 48-72 ч, а также после проведения искусственного аборта, внематочной беременности и инвазивных манипуляций во время беременности. Такая тактика снижает вероятность развития иммунизации родильниц с 7,5 %о до 0,2 %о. 394 ЧАСТЬ 2. ПАТОЛОГИЧЕСКОЕ АКУШЕРСТВО Возможность развития изоиммунизации во время беременности послужила основанием к изучению эффективности антенатального применения анти-D-иммуноглобулина. Исследования показали, что его профилактическое введение при сроке 28 и 34 недели беременности в дозе 150 мкг в сочетании с послеродовой профилактикой снижает вероятность изоиммунизации до 0,06%. Глава 42 РОДОВЫЕ ТРАВМЫ НОВОРОЖДЕННЫХ Родовые травмы в структуре патологии новорожденных занимают значительное место. Под термином «родовая травма» имеют в виду повреждения плода, возникшие спонтанно при прохождении его через родовые пути. Повреждения плода, возникающие вследствие акушерских манипуляций (поворот, щипцы, хирургические вмешательства) при осложненных родах, принято называть акушерской травмой; этот вид травмы встречается значительно реже. Хроническая и острая внутриутробная гипоксия плода является предрасполагающим фактором, увеличивающим вероятность родового травматизма даже при нормально протекающих родах. Повреждения головки плода являются частыми (2 на 1000 новорожденных) и опасными родовыми травмами, так как могут оставлять тяжелые последствия. Кефалогематома — кровоизлияние под надкостницу теменной или затылочной костей, встречается в 0,2—2,5% случаев. Флюктуирующая опухоль никогда не распространяется за пределы кости, над которой она располагается. Она безболезненна, не пульсирует, имеет тенденцию к увеличению в течение первой недели после родов, затем ее размеры постепенно уменьшаются, и полная резорбция происходит к 6—8-й неделе. При больших размерах кефалогематомы и при двусторонней кефалогематоме часто (в 18—20% случаев) имеется трещина костей черепа, для исключения которой следует делать рентгенограмму. Лечения при кефалогематоме не требуется. Пункцию производят только при очень больших, нарастающих кефалогематомах или при нагноившейся гематоме (в сочетании с антибиотикотерапией). Трещины и переломы костей черепа, как правило, являются следствием акушерских вмешательств (щипцы и др.) или результатом сдавления головки при аномалиях таза матери. Хирургическое вмешательство необходимо только в случаях появления неврологических симптомов, свидетельствующих о повышении внутричерепного давления, нарастании кровоизлияния или сдавления мозговой ткани. Внутричерепные родовые травмы сопровождаются повреждением ткани мозга с последующим отеком. К л и н и ч е с к и е п р о я в л е н и я обусловлены степенью нарушения ге-моликвородинамики. В тяжелых случаях смерть ребенка наступает уже в первые часы жизни, тогда как при легких формах изменения могут носить обратимый характер. Различают эпидуральные, субдуральные, субарахноидальные, внутримозго-вые и смешанные кровоизлияния. Наиболее часто при родовой травме кровоиз- Раздел 4 Патология плода и новорожденного лияния происходят из венозных синусов и локализуются над и под наметом мозжечка. При разрыве намета мозжечка (гематома в задней черепной ямке) происходит сдавление мозгового ствола. Состояние новорожденного тяжелое: нарушено сосание и глотание, наблюдаются анизокория, грубый вертикальный или ротаторный нистагм, «плавающие» глазные яблоки, приступы тонических судорог. В тяжелых случаях нарастают расстройства дыхания, сердечной деятельности, и ребенок погибает. У новорожденных с субтенториальной субду-ральной гематомой без повреждения намета мозжечка возможен благоприятный исход, но с последующим развитием гидроцефалии. В остром периоде внутричерепной родовой травмы в клинической картине преобладают общемозговые симптомы, обусловленные нарушением мозгового кровообращения и отеком мозга. На первом этапе преобладают симптомы общего угнетения функций: атония мышц, отсутствие активных движений и реакции на внешние раздражения, угнетение дыхательной функции и замедление сердечного ритма, симптомы поражения центров лицевого, тройничного, подъязычного нервов. Вторая стадия характеризуется состоянием возбуждения: двигательное беспокойство, неадекватная реакция на раздражение, расстройство сна, разгиба-тельная гипертония, резкий тремор конечностей, судороги, нарушение терморегуляции. Если ребенок выживает, наступает период медленного восстановления функций с развитием различных клинических синдромов: вегетовисцеральных дисфункций, двигательных нарушений, мышечной гипотонии, мышечной гипертонии, а также судорожный и гидроцефальный синдромы. Д и а г н о с т и к а внутричерепной родовой травмы основывается на данных клинического обследования, исследовании цереброспинальной жидкости, глазного дна, результатах ЭЭГ, УЗИ, компьютерной томографии. Л е ч е н и е в остром периоде родовой травмы направлено на обеспечение полного покоя, проводится адекватная оксигенотерапия, инфузионная терапия с целью дегидратации и улучшения микроциркуляции, вводят противосудорож-ные препараты. При субарахноидальных и субдуральных кровоизлияниях показаны люмбальные пункции. Дети, перенесшие родовую травму, должны находиться под наблюдением нервопатолога. Родовая травма спинного мозга возникает при форсированной тяге за головку при фиксированных плечиках плода или тяге за плечики при фиксированной головке, а также при чрезмерной ее ротации. При этом могут возникать повреждения позвоночника (подвывихи, смещение тел позвонков, переломы и т. п.), повреждения межпозвоночных дисков, кровоизлияния в спинной мозг, его оболочки и эпидуральную клетчатку, ишемия в бассейне позвоночных артерий. К л и н и ч е с к а я к а р т и н а зависит от локализации и вида повреждения. При травме шейного отдела позвоночника наблюдается выраженный болевой синдром, кривошея. При повреждении шейных сегментов на уровне С,—CIV наблюдаются мышечная гипотония, арефлексия и дыхательные расстройства, симптом «короткой шеи», «поза лягушки», что может сочетаться с симптомами поражения ствола мозга и нарушением функции тазовых органов. В случае травмы спинного мозга на уровне Сш—CIV может развиться парез диафрагмы, чаще правосторонний. Верхний парез и паралиг Дюшенна—Эрба развиваются при поражении спинного мозга на уровне Cv—CVI. При этом рука ребенка приведена к туловищу, ЧАСТЬ 2 ПАТОЛОГИЧЕСКОЕ АКУШЕРСТВО разогнута в локтевом суставе, повернута внутрь, ротирована в плечевом суставе, пронирована в предплечье. Движения кисти и пальцев свободны. Нижний тип паралига Дежерин-Клюмпке встречается реже, поражаются VII и VIII шейные и I грудной сегменты. В этом случае рука свисает, отсутствуют движения кисти и пальцев. Движения в локтевом и плечевом суставах сохранены; чувствительность нарушена. Повреждение шейных симпатических волокон характеризуется появлением птоза, миоза и энофтальма на пораженной стороне. Родовая травма спинного мозга в пояснично-крестцовой области проявляется нижним вялым парапарезом при сохранении нормальных движений в верхних конечностях. Д и а г н о з спинальной травмы устанавливают на основании тщательного изучения анамнеза типичной клинической картины и данных рентгенографического исследования позвоночника, электромиографии и миелографии. Л е ч е н и е направлено на прекращение кровотечения, снятие болевого синдрома и нормализацию мозгового кровообращения. При подозрении на травму шейного отдела спинного мозга необходима иммобилизация с помощью ватно-марлевого воротника. При параличе Дюшенна с помощью гипсовой повязки создается покой для верхней конечности, слегка приподнятой в плечевом поясе, с отведенным в сторону и ротированным кнаружи плечом. С 3-го дня жизни назначают дибазол, витамины В1 и В2, после 2-й недели — массажи, физиотерапевтические процедуры. В течение первых 3 мес. жизни излечиваются от 50 до 90% акушерских параличей. В тяжелых случаях рекомендуется раннее хирургическое лечение. Травмы конечностей наблюдаются чаще у новорожденных с большой массой тела и широкими плечами (например, у детей с диабетической фетопатией), а также при затрудненном извлечении ручек (тазовое предлежание плода). При переломе клюгицы, как правило, отсутствует смещение отломков. При прощупывании в первые часы и дни жизни определяется крепитация, ко 2-й неделе формируется костная мозоль. Общее состояние ребенка не нарушено, активные движения руки не ограничены. Необходима повязка, фиксирующая руку и туловище. Прогноз хороший. Перелом плегевой кости чаще всего локализуется в ее средней или верхней трети. Иногда он комбинируется с отслоением эпифиза — эпифизиолизом или дисторзией плечевого сустава. В этом случае может быть и кровоизлияние в сустав, и незначительное смещение костных отломков. Рука в состоянии аддукции и внутренней ротации. Эти переломы зарастают полностью с помощью иммобилизации конечности. Наиболее частая родовая травма нижних конечностей — перелом бедренной кости — наблюдается при извлечении плода за ножку. Для этого перелома характерно большое смещение костных отломков в результате сильного мышечного напряжения. Субкапсулярную гематому печени или кровоизлияние в надпочечники можно наблюдать в результате родовой травмы. Предрасполагающими факторами являются тазовые предлежания плода, гигантизм, гемолитическая болезнь новорожденного и др. При нарастающей гематоме может произойти ее разрыв, и тогда кровь проникает в брюшную полость. У ребенка наблюдается геморрагический шок и коллапс. Эхотомограмма позволяет правильно поставить диагноз. Кровоизлияния в надпочечники встречаются с частотой 1,7 на 1000 вскрытий новорожденных детей; в 8—10% случаев они двусторонние. Раздел 4. Патология плода и новорожденного Симптомы, появляющиеся в течение первой недели жизни, часто атипичны: анорексия, рвота, диарея, вялость, нарушение ритма дыхания, гематурия, снижение уровня гемоглобина. Внутривенная пиелография позволяет установить диагноз. Дети, перенесшие родовую травму, нуждаются в наблюдении не только педиатра, но и невропатолога, ортопеда. Глава 43 ВНУТРИУТРОБНЫЕ И Н Ф Е Ш И И Внутриутробные инфекции — заболевания, возникающие в результате заражения плода от матери в антенатальном периоде или во время родов. Внутриутробные инфекции встречаются в 0,5—2,5% случаев. Э т и о л о г и я и п а т о г е н е з. Возбудителями внутриутробных инфекционных заболеваний могут быть вирусы, бактерии, простейшие, грибы, мико-плазмы, хламидии и другие микроорганизмы. Источниками инфицирования плода являются кровь матери (бактериемия), очаги воспалительного процесса в матке и придатках, наличие патогенной флоры во влагалище. В антенатальном периоде инфекция может передаваться трансплацентарным путем: 1) в результате проникновения возбудителя из материнской крови в кровь плода при отсутствии воспалительных очагов в плаценте; 2) при попадании возбудителя в материнскую часть плаценты и формировании в ней воспалительного очага с последующим проникновением инфекционного агента в кровь плода; 3) при поражении хориона и развитии воспалительного процесса в фетальной части плаценты, оболочках и инфицировании амниотиче-ской жидкости (рис. 95). Второй путь заражения плода — восходящая инфекция из влагалища и шейки матки через поврежденный или неповрежденный плодный пузырь. Поражение плода во многом зависит от способа инфицирования. При гематогенном пути развитие бактериемии у плода совпадает по времени с появлением таковой у матери и может быть кратковременным. В другом случае бактериемия у плода по времени отсрочена от материнской и более продолжительна, при этом воспалительный процесс может сформироваться в любом органе (чаще в почках), и тогда сам плод, выделяя бактерии с мочой, вторично инфицирует оболочки, плаценту, амниотическую жидкость и сам инфицируется снова при ее заглатывании, при этом поражаются слизистые оболочки желудочно-кишечного тракта, трахеи, бронхов или альвеолы. Во время родов заражение происходит при контакте поверхности тела плода с инфицированными родовыми путями и при аспирации инфицированного секрета родовых путей во время первого вдоха. Характер и тяжесть инфекционного процесса у плода определяются стадией его внутриутробного развития в момент инфицирования. В первые 3 мес. развития эмбриона может нарушаться процесс закладки и дифференцирования органов и систем, что ведет к формированию врожденных пороков развития. В фетальном периоде заболевание протекает в виде нарушения кровообращения, ЧАСТЬ ПАТОЛОГИЧЕСКОЕ АКУШЕРСТВО дистрофических и некробиотических процессов, имеющих генерализованный характер и приводящих к развитию гидронефроза, гидроцефалии. Чем меньше гестационный возраст плода в момент инфицирования, тем острее происходит генерализация процесса и тем тяжелее его последствия. При инфицировании в родах скорость развития и тяжесть инфекционного процесса зависят от интенсивности колонизации микроорганизмов и степени зрелости плода.
К л и н и ч е с к а я к а р т и н а. Проявления заболевания у новорожденного зависят от того, в какой стадии инфекционного процесса он родился. У ребенка могут наблюдаться последствия заболевания, пересенного внутриутробно, или заболевание течет вяло, торпидно. В таких случаях чаще поражаются Ц Н С, печень, почки. Если роды происходят в острой стадии инфекционного процесса,
Раздел 4 Патология плода и новорожденного ребенок может погибнуть интранатально или родиться в асфиксии. У него оказываются пораженными легкие, Ц Н С, печень, сердце. Клинические симптомы заболевания при внутриутробном инфицировании могут проявляться через несколько часов, дней, месяцев и даже лет, если ребенок рождается во время инкубационного периода инфекции. Клиническая картина различных инфекций имеет свои особенности. Краснуха. Широкое распространение вирусоносительства и высокая конта-гиозность вируса краснухи создают серьезную угрозу для беременной и плода. Частота заболевания плодов краснухой составляет 90% при инфекции у матери в первые 12 нед. беременности, 53% — на 13—16-й неделе и 36% — на 17—22-й неделе беременности. Среди заболевших в эти сроки плодов рождаются с пороками развития соответственно 90%, 18% и 0%. Характерные последствия краснухи: отставание плодов в развитии, гипотрофия, катаракта, ретинит, иногда глаукома; врожденный порок сердца (открытый артериальный проток, стеноз легочной артерии), глухота. В острой стадии заболевания в первые 48 ч у новорожденного может наблюдаться тромбоцито-пеническая пурпура (число тромбоцитов 60 000—100 000), гепатоспленомега-лия, поражение ЦНС, реже — легких. На рентгенограмме определяется продольная исчерченность в области метафизов трубчатых костей. В последующем у трети детей, перенесших краснуху, имеется умственная отсталость и глухота. Д и а г н о с т и к а. Диагноз краснухи ставят на основании анамнеза матери (указание на контакт с больными, наличие высыпания во время беременности, легкой ангины, увеличения лимфатических узлов) и клинических признаков заболевания у ребенка, а также обнаружения в его крови специфических IgM-антител. Л е ч е н и е. Симптоматическое. П р о ф и л а к т и к а. Для профилактики внутриутробной краснухи проводят вакцинацию всем детям и подросткам. Беременным в первые дни после заражения вводят специфические иммуноглобулины. Цитомегалия. Цитомегаловирус широко распространен среди людей, он выделяется с мочой, секретом слюнных желез и шейки матки, со спермой и молоком. Частота его выявления в секрете шейки матки увеличивается с возрастанием сроков беременности с 1,6% в I триместре до 11,3 — 27,8% в III триместре. Для цитомегаловирусной инфекции характерно наличие своеобразных гигантских, с внутриядерными включениями клеток, локализующихся главным образом в эпителиальной ткани различных органов, а в тяжелых случаях — в печени, селезенке, легких, почках, поджелудочной железе, мозге. Клинические признаки цитомегаловирусной инфекции: отставание плода в развитии, гипотрофия, микроцефалия, перивентрикулярные мозговые кальци-фикаты, хориоретинит, гепатоспленомегалия, гипербилирубинемия, петехиаль-ная сыпь и тромбоцитопения. Генерализованная форма протекает под видом гемолитической болезни с гепатоспленомегалией и геморрагической сыпью. В большинстве случаев заболеваний выражены симптомы поражения Ц Н С (беспокойство, тремор, судороги), нередко наблюдается картина интерстициальной пневмонии. Цитомегаловирусная инфекция, часто в первые дни жизни протекающая ма-лосимптомно, ведет к формированию воспалительно-дегенеративного процесса в головном мозге и является одной из причин церебральной патологии в детском возрасте. ЧАСТЬ 2 ПАТОЛОГИЧЕСКОЕ АКУШЕРСТВО К л и н и ч е с к а я д и а г н о с т и к а цитомегаловирусных энцефалитов трудна, так как симптомы болезни аналогичны тем, что наблюдаются у детей, перенесших гипоксию, внутричерепную травму, а также гемолитическую болезнь. Д и а г н о с т и к а. Диагноз цитомегаловирусной инфекции у новорожденного может быть подтвержден при получении данных об инфицированное™ матери, обнаружении маркеров вируса в моче ребенка или сведений об увеличении в его крови содержания IgM-антител с момента рождения. Более 80% клинически здоровых детей с маркерами ЦМВ и наличием IgM-антител при рождении требуют многолетнего диспансерного наблюдения у педиатра и невропатолога. Л е ч е н и е. Симптоматическое. П р о ф и л а к т и к а. Необходима ранняя диагностика этого заболевания у беременной и плода, что служит показанием к прерыванию беременности. Наивысшей чувствительностью обладает молекулярно-биологический метод диагностики. Полимеразная цепная реакция (ПЦР) позволяет идентифицировать искомые последовательности генома цитомегаловируса практически по одной молекуле ДНК и тем самым провести определение вируса в любой клетке, если он есть. Установление диагноза у беременной является показанием для соответствующего обследования плода. Материалом для исследования могут служить хорионбиоптаты и кровь плода, полученные с помощью кордо-центеза. Герпетическая инфекция. Частота неонатальной герпетической инфекции составляет 1 случай на 7500 родов. Заболевания плода и новорожденного чаще вызываются генитальным вирусом II типа, который выделяется из шеечного секрета и мочи у 9,4% беременных. При заболевании матери в I триместре беременности вирус, проникая к плоду гематогенным путем, ведет к спонтанному аборту или формированию пороков развития (микроцефалия, микрофталь-мия, кальцификаты в ткани мозга). Герпетическая инфекция в более поздние сроки беременности ведет к мертворождению, а при заражении непосредственно перед родами или во время рождения у детей наблюдаются генерализованная или локальные формы инфекции. К л и н и ч е с к а я к а р т и н а. Первые симптомы герпетической инфекции имеются уже при рождении или появляются на первой неделе жизни. Ребенок становится вялым, плохо сосет, повышается температура тела, появляются одышка, тахикардия, желтуха, иногда наблюдаются рвота и жидкий стул с примесЬю крови. Имеются симптомы поражения Ц Н С (судороги, опистонус). Смертность детей составляет 80%. У выживших детей развиваются микроцефалия, гидроцефалия, умственная отсталость и поражение глаз (хориоретинит, катаракта, слепота). При локализованной форме герпетической инфекции наиболее неблагоприятные исходы дает поражение ЦНС, которое протекает в виде нарушений сна, повышенной возбудимости, тремора конечностей, судорог. Заболевание глаз на первой неделе жизни протекает в виде конъюнктивита, кератоконъюнктивита, хориоретинита, кератита, последствия которых — катаракта, повторяющийся герпетический кератит и рубцы на роговице. Кожные формы герпетической инфекции у новорожденных обычно протекают в виде везикулярной или пятнистой эритемы, высыпаний различной локализации и, как правило, имеют благоприятный исход. Д и а г н о с т и к а. Клинический диагноз при отсутствии у ребенка характерных кожных высыпаний поставить достаточно трудно, поскольку заболевание у Раздел 4 Патология плода и новорожденного большинства детей протекает с неспецифическими симптомами. Важно сопоставить данные клинического осмотра с результатами анамнеза матери. Диагностика герпетической инфекции осуществляется с помощью гистологических, вирусологических и серологических методов. Наиболее чувствительный диагностический тест — это выявление вирусных антигенов в цитологических мазках с помощью иммунофлюоресценции, используя моноклональные и поли-клональные антитела. Многие лаборатории используют специальные ферментные наборы для определения антигенов. Л е ч е н и е. Лечение должно быть комплексным и начато как можно раньше. Эффективно специфическое лечение с помощью ацикловира и других противовирусных препаратов. Учитывая иммунодепрессивное действие этих средств, одновременно назначают антибиотики. П р о ф и л а к т и к а. Профилактика заболеваний плода и новорожденного состоит в прерывании беременности в случае выявления острой генитальной герпетической инфекции в ранние сроки. Если генитальная герпетическая инфекция возникает на 8—9-м месяце беременности, то родоразрешение следует проводить до начала родовой деятельности с помощью операции кесарева сечения. Вирусный гепатит В и С. Вирусом гепатита ребенок заражается от матери, если она переносит острую инфекцию в последние 3 мес. беременности. Реже это происходит при бессимптомном носительстве беременной поверхностного антигена HBsAg, или антител к вирусу гепатита С. У инфицированного внутриутробно ребенка сначала может не быть симптомов заболевания, лишь иногда наблюдается желтуха. Поэтому все новорожденные с неонатальным гепатитом так же, как и дети, матери которых перенесли гепатит во время беременности или являются носителями HBsAg, должны быть обследованы в раннем неонатальном периоде. Диагноз гепатита В может быть подтвержден при выявлении HBsAg в сыворотке крови ребенка, взятой после рождения. О наличии активного процесса свидетельствует высокий уровень трансаминазы в крови ребенка. Л е ч е н и е. Ребенка с гепатитом В лечат симптоматически. П р о ф и л а к т и к а. До настоящего времени профилактика гепатита В основывается на использовании стандартных иммуноглобулинов в первые 48 ч жизни ребенка и далее ежемесячно в течение 6 мес. жизни. К ребенку, у которого имеется положительная реакция на HBsAg, следует относиться как к контагиозному больному, соблюдая особую осторожность при манипуляциях с инъекционными иглами. Токсоплазмоз. При широком распространении токсоплазмоза среди взрослого населения у новорожденных детей эта инфекция встречается сравнительно редко, главным образом в тех случаях, когда женщина остро заболела во время беременности или незадолго до ее наступления. Возбудитель, проникая во все органы, чаще всего в клетки Ц Н С и ретику-лоэндотелиальной системы, образует псевдоцисты, на месте которых образуются некрозы, кистевидные полости, участки рубцевания и очаги обызвествления. Степень распространения и тяжесть поражения структур зависят от вирулентности паразита Т. gondii, массивности инфицирования и сроков беременности, так как в передаче инфекции плоду играют роль проницаемость плацентарного барьера и состояние иммунной системы плода. При инфицировании матери в первую треть беременности около 83% плодов остаются здоровыми, ЧАСТЬ 2. ПАТОЛОГИЧЕСКОЕ АКУШЕРСТВО при заболевании во вторую треть — до 75%, а в последнюю треть — только 35%. К л и н и ч е с к а я к а р т и н а. Клинические проявления внутриутробного токсоплазмоза в значительноей мере обусловлены сроком заражения плода. Если инфицирование произошло в последнюю треть беременности, ребенок рождается в стадии генерализации процесса, заболевание протекает с клинической картиной сепсиса. При более раннем сроке заражения период генерализации инфекции у плода завершается внутриутробно и после рождения преобладают симптомы энцефалита или уже имеются необратимые изменения ЦНС. При токсоплазмозе у плода развивается некротический менингоэнцефалит: имеются милиарные гранулемы в головном и спинном мозге, некроз мозговой ткани, перивентрикулярные васкулиты и язвы на стенках желудочков, клеточная инфильтрация мягкой мозговой оболочки и обструкция водопровода мозга (сильвиева водопровода), мозговые кальцификаты. Клинически это проявляется судорогами, атонией, арефлексией, нарушением терморегуляции и ритма дыхания, парезами, в более поздних стадиях процесса — микроцефалией или гидроцефалией, значительной задержкой психомоторного развития. Отмечают некротический ретинохориоидит с последующим развитием атрофии зрительного нерва, псевдоколобомы, катаракты, парезы глазных мышц и микро-фтальм. Иногда наблюдаются гепатоспленомегалия, явления бронхита, поносы, на коже пятнисто-папулезная и петехиальная сыпь, реже — желтуха с эритроблас-тозом, интерстициальная пневмония, миокардит. Д и а г н о с т и к а. Диагноз ставят на основании клинических признаков и результатов лабораторных исследований. Наличие ксантохромной спинномозговой жидкости с белково-клеточной диссоциацией, внутримозговых кальцификатов, лейкоцитоза с атипичными лимфоцитами и эозинофилией в периферической крови существенно облегчают диагноз. Для диагностики токсоплазмоза используют реакции Сейбина—Фельдмана (сыворотка крови ребенка и матери). Дети с высокими титрами IgG- и IgM-антител или те дети, у матерей которых обнаружены высокие титры антител, должны быть подвергнуты ежегодному серологическому тестированию для выявления специфических антител. Л е ч е н и е. Специфическая терапия в раннем неонатальном периоде рекомендуется при всех формах токсоплазмоза, в том числе и при отсутствии клинических проявлений заболевания, но при установленной острой инфекции у матери. Назначают хлоридин в сочетании с сульфаниламидными препаратами, кортикостероиды, фолиевую кислоту и симптоматические средства. П р о ф и л а к т и к а. Необходимо лечить беременную при выявлении у нее острого токсоплазмоза. Листериоз. Листериоз у беременных и новорожденных представляет наиболее частую форму листериоза. Он может протекать бессимптомно, или у.беременной незадолго до родов появляются катаральные явления в области верхних дыхательных путей, головная боль, боли в области крестца и поясницы, лихорадочная реакция. Генерализация листериозной инфекции у плода превращает его в септический очаг, из которого идет массивное поступление листерий в организм матери. Чаще отмечаются преждевременные роды. После рождения ребенка температура у матери быстро снижается, послеродовой период протекает относительно спокойно. Раздел 4. Патология плода и новорожденного У ребенка листериоз протекает по типу внутриутробного сепсиса с поражением мозга, легких, увеличением печени, селезенки и повышением температуры. Характерно появление мелкоузелковой или мелкорозеолезной сыпи на коже, иногда принимающее геморрагический характер. Септический гранулематоз, как правило, заканчивается летальным исходом. При локализованных формах лис-териозной инфекции, протекающих даже с клинической картиной менингита, прогноз более благоприятный. Д и а г н о с т и к а. Диагноз листериоза подтверждают обнаружением возбудителя в моче, кале, спинномозговой жидкости. Л е ч е н и е. Проводится антибиотикотерапия (пенициллин) в сочетании с симптоматическими средствами. П р о ф и л а к т и к а. Необходимо выявлять очаги инфекции у животных, проводить ветеринарный и санитарно-гигиенический контроль при подозрении на листериозную инфекцию, а также профилактическое лечение беременных при малейшем подозрении на листериоз. Сифилис. У матери сифилис может протекать манифестно или бессимптомно. Заражение плода происходит не ранее 5-го месяца беременности. Чем раньше заражается плод и чем свежее и тяжелее инфекция у матери, тем тяжелее протекает врожденный сифилис у новорожденного. Ребенок рождается преждевременно, имеется выраженная задержка роста и массы тела. При висцеральном сифилисе преобладают поражения внутренних органов (гепатосплено-мегалия, пневмония, поражения почек, сердечно-сосудистой системы). Отмечается генерализованный отек, сочетающийся с гипоальбуминемией, у некоторых детей могут быть протеинурия и гематурия. Часто поражается кожа: сифилитический пемфигус (преимущественно на ладонях и подошвах), макулопапулезные сифилитические экзантемы (на лбу, носу, наружных поверхностях верхних и нижних конечностей), диффузные экзантемы, трещины в области губ. Самым ранним и частым симптомом является сифилитический насморк. У 85% больных имеются поражения костей: остео-хондриты и периоститы, иногда так называемый псевдопаралич Парро. При врожденном сифилисе часто поражаются глаза (иридоциклит, хориоре-тинит). У 60% детей имеются симптомы поражения Ц Н С (беспокойство, тремор, угнетение физиологических рефлексов, изменение мышечного тонуса). Д и а г н о с т и к а. Диагноз труден при висцеральном типе сифилиса, особенно при бессимптомном течении. При малейшем подозрении на сифилис производят серологические реакции Вассермана и Кана, рентгенографию костей и исследование глазного дна. Прогноз зависит от времени заражения плода и начала лечения; важное значение имеет лечение матери во время беременности. Л е ч е н и е. При врожденном сифилисе лечение включает пенициллин и симптоматические средства. Одним из важнейших п р о ф и л а к т и ч е с к и х м е р о п р и я т и й является раннее выявление и адекватное лечение сифилиса у беременной. Кандидоз. Инфицирование плода грибами в период внутриутробного развития встречается редко, хотя дрожжеподобные грибы выделяются у 70—80% беременных с кольпитами. Описаны случаи поражения грибами головного мозга, которые носили характер специфического некротического продуктивного воспаления, содержали нити псевдомицелия и споры грибов. При инфицировании плода и развитии у него генерализованной кандидозной инфекции, как правило, наблюдается преждевременное прерывание беременности. ЧАСТЬ 2. ПАТОЛОГИЧЕСКОЕ АКУШЕРСТВО М и к о п л а з м е н н а я и н ф е к ц и я. Микоплазмы занимают промежуточное место между бактериями и вирусами и часто вызывают у взрослых людей заболевания мочеполовой системы. Из всех известных видов микоплазм наиболее важную роль в инфицировании плода играют М. hominis и U. urealyticum. Попадая на слизистые оболочки глаз, дыхательных путей, желудочно-кишечного тракта и половых органов ребенка, микоплазмы интенсивно размножаются. Внедряясь в клетку, они воздействуют на ее метаболизм и хромосомный аппарат. Микоплазменная инфекция у плода возникает в различных стадиях внутриутробного развития и нередко является причиной спонтанных абортов и преждевременных родов. У новорожденных она проявляется в виде пневмонии, менингита, конъюнктивита, подкожных абсцессов, а Также играет роль в возникновении персистирующей легочной гипертензии и бронхолегочной дисплазии. Микоплазменная пневмония носит, как правило, интерстициальный характер. У недоношенных новорожденных клиническая картина пневмонии сходна с болезнью гиалиновых мембран легких. Пневмония может сочетаться с микоплазменным менингитом и менингоэнцефалитом. Возможно образование абсцессов мозга и гидроцефалии с последующей задержкой нервно-психического развития ребенка. В крови больных детей обнаруживается стойкий лейкоцитоз нейтрофильного характера, а у недоношенных — лейкопения. Возбудитель может быть выделен из крови, из содержимого трахеи, слизи с задней стенки гортани и спинномозговой жидкости. У новорожденных детей с признаками внутриутробной инфекции в крови пуповины повышено содержание IgM, часто обнаруживается IgA. Для подтверждения клинического диагноза внутриутробного микоплазмоза большое значение имеет гистологическое исследование плаценты и оболочек, позволяющее выявить характерные для инфекционного процесса воспалительно-дегенеративные изменения. Л е ч е н и е. Специфическая терапия заключается в применении эритромицина в сочетании с иммуноглобулинами, антиоксидантами и симптоматическими средствами. П р о ф и л а к т и к а. Для профилактики внутриутробного инфицирования плода необходимо проводить обследование на микоплазмоз беременных, имеющих в анамнезе выкидыши, хронический сальпингит, преждевременные роды, пиелонефрит, и проводить им местное лечение. Хламидийная инфекция. Широкое распространение урогенитальных хла-мидиозов вызвало увеличение частоты этой патологии среди беременных и повысило опасность внутриутробного инфицирования плода. Воспалительные заболевания мочеполовой системы у матерей, а также конъюнктивиты и пневмонии у новорожденных детей вызываются одним серотипом Chi. trachomatis, который поражает только цилиндрический эпителий. К л и н и ч е с к а я к а р т и н а. Инфицирование ребенка хламидиями в большинстве случаев происходит еще до прохождения через родовые пути путем заглатывания и (или) аспирации околоплодных вод и оседания возбудителя на конъюнктиве, слизистой оболочке вульвы или уретры. Поэтому в зависимости от времени, прошедшего от момента инфицирования до рождения ребенка, и от гестационного возраста плода в раннем неонатальном периоде имеются различные типы проявлений хламидийной инфекции: 1) внутриутробный сепсис с тяжелым поражением внутренних органов (мозг, легкие, печень, почки, кишечник, селезенка), ведущий к рождению ребенка в глубокой асфиксии и к его гибели в первые минуты и часы жизни; Раздел 4 Патология плода и новорожденного 2) наличие с первых часов жизни неспецифических проявлений заболевания, сходных с постгипоксическим состоянием, и последующее быстрое развитие синдрома дыхательных расстройств (у недоношенных детей) или пневмонии (у доношенных); 3) латентное течение инфекции в первые 4—5 дней жизни, появление неспецифических проявлений заболевания к концу первой и на второй неделе жизни, при отсутствии специфической терапии — развитие пневмонии, конъюнктивита, назофарингита, вульвита и др. Две первые наиболее тяжелые формы заболевания наблюдаются, как правило, у недоношенных детей. Для всех новорожденных первичным проявлением заболевания является нарушение функций Ц Н С: беспокойство, расстройство сна, терморегуляции, изменения мышечного тонуса, угнетение физиологических рефлексов новорожденных, срыгивание. У наименее зрелых недоношенных детей доминирует картина угнетения функций Ц Н С, наблюдается апноэ. Другим проявлением внутриутробной хламидийной инфекции является нарушение центральной гемодинамики, что выражается в раннем появлении систолического шума, гипертензии малого круга кровообращения, перегрузки правых отделов сердца (по данным Э К Г). На рентгенограмме отмечается увеличение размеров сердца за счет его правых отделов и нарушение гемодинамики в легких: «влажные легкие». Выраженное нарушение функции внешнего дыхания появляется позднее, а вначале наблюдается поверхностное жесткое дыхание, иногда необильные мелкопузырчатые хрипы. Воспалительная инфильтрация в легких выявляется лишь к концу 2—3-й недели жизни. Недоношенные дети с внутриутробной хламидийной инфекцией рождаются гипотрофичными, часто с асфиксией, имеют ранние проявления синдрома дыхательных расстройств, который у наименее зрелых детей осложняется развитием бронхолегочной дисплазии. У ряда детей наблюдаются желтуха и ДВС-синдром. В крови отмечается умеренное снижение гемоглобина, к 7—10-му дню жизни увеличивается число эозинофилов и моноцитов. Д и а г н о с т и к а. Хламидийную инфекцию у ребенка можно заподозрить, опираясь на клиническую картину заболевания и данные анамнеза матери (указания на бесплодие, эндометриты после абортов, родов, цервицит и острый уретрит во время беременности, выкидыши и преждевременные роды). Хлами-дийная этиология инфекции подтверждается выявлением антигена Chi. tracho-matis методом иммуноферментного анализа в мазках с задней стенки глотки и конъюнктивы нижних век у ребенка и из цервикального канала у матери. Используют определение антигена методом непрямой иммунофлюоресценции с моноклональными антителами. Обнаружение в крови матери и ребенка анти-хламидийных антител в титре 1:32 также служит подтверждением наличия инфекционного процесса. Л е ч е н и е. При хламидийной инфекции лечение должно быть комплексным и включать антибиотики (эритромицин), интерферон, иммуноглобулины, глутаминовую кислоту, антиоксиданты (витамины Е, А, С) и симптоматические средства. Лечат одновременно мать и отца ребенка. Если детей с хламидийной инфекцией не лечили или провели неполный курс терапии, то в последующем они страдают частыми респираторными заболеваниями, конъюнктивитами, отитами, пневмониями. У них длительно сохраняется персистенция возбудителя. П р о ф и л а к т и к а. Проводят выявление хламидиоза у беременных и лечение супружеской пары. ЧАСТЬ 2 ПАТОЛОГИЧЕСКОЕ АКУШЕРСТВО Врожденные бактериальные инфекции. Бактериальные инфекции занимают значительное место в структуре неонатальной заболеваемости, особенно среди недоношенных детей, составляя около 4%. При экстрагенитальных очагах инфекции, хронической урогенитальной инфекции (пиелонефрит, вульвоваги-нит, кольпит и др.), наличии в половых путях беременной условно-патогенной микрофлоры, при преждевременных и осложненных длительным безводным промежутком родах, оперативных вмешательствах риск внутриутробного инфицирования плода существенно возрастает. Среди возбудителей инфекции наиболее часто встречаются стрептококк группы В, кишечная палочка, реже золотистый и эпидермальный стафилококки, клебсиелла. Риск инфицирования ребенка зависит от количества и вирулентности микроорганизмов, от длительности контакта с ними и свойственной новорожденному восприимчивости к инфекции. Это особенно относится к недоношенным детям, у которых защитные механизмы недостаточно зрелые (снижены фагоцитарная активность, уровни пропердина, комплемента и иммуноглобулинов). Поэтому у них часто наблюдается генерализованный инфекционный процесс, нередко протекающий по типу септицемии. К л и н и ч е с к а я к а р т и н а. При врожденных бактериальных инфекциях (особенно при интранатальном заражении плода) доминируют неспецифические симптомы, позволяющие лишь констатировать наличие у ребенка внутриутробной инфекции. Выявляются общие симптомы: гипотрофия, задержка прибавки массы тела; вялость, сонливость или, напротив, повышенная возбудимость; угнетение физиологических рефлексов новорожденного; снижение мышечного тонуса; склерема, бледность кожи, «сероватый» ее оттенок, желтуха, мелкоточечные и обширные кровоизлияния. Часто наблюдаются поражения желудочно-кишечного тракта (вздутие живота, срыгивание, рвота, гепатоспленомегалия), легких (ослабленное дыхание, мелкопузырчатые хрипы в легких, участие в акте дыхания вспомогательной мускулатуры), сердечно-сосудистой системы и Ц Н С (гид-роцефальный синдром, нарушение регуляции ритма сердечной деятельности и дыхания). Появление и нарастание неврологической симптоматики к концу первой недели жизни при отсутствии данных, свидетельствующих о неблагоприятном влиянии самого родового акта, как правило, обусловлено внутриутробной инфекцией. У недоношенных детей почти 70% внутриутробных бактериальных инфекций протекает в виде быстро развивающейся септицемии, которая представляет собой своеобразный бактериальный шок. Особенно это относится к коли-инфекции (эшерихиоз), поскольку многие серотипы кишечной палочки вырабатывают эндотоксины. При септицемии на передний план выступают признаки тяжелой гипоксии: общий цианоз, атония, снижение температуры, нарушения ритма и «стонущий» характер дыхания, глухость сердечных тонов. Повышена кровоточивость, наблюдается вздутие живота, трактуемое как парез кишечника. В подобных случаях смерть недоношенного ребенка наступает быстро. У доношенных детей проявление внутриутробной инфекции реже связано с инфицированием грамотрицательными бактериями. Если это происходит, то обычно развиваются локализованные процессы в виде пневмонии, диареи, реже — менингита. В последние годы увеличилось число заболеваний, вызванных инфицированием плода стрептококком группы В, носительство которого выявляется у 5— 24% женщин. Инфекция может начаться внутриутробно, и ее симптомы проявляются сразу же после рождения или в первые 48 ч жизни. На первый план Раздел 4. Патология плода и новорожденного выступают нарастающие дыхательные расстройства. Клинические и рентгенографические признаки напоминают таковые при болезни гиалиновых мембран. Состояние ребенка прогрессивно ухудшается, развиваются одышка, повторные апноэ, снижается артериальное давление. У доношенных детей могут наблюдаться судороги, у недоношенных — чаще атония, арефлексия. В крови определяют метаболический ацидоз, часто лейкопению и тромбоцитопению. Летальность достигает 50—60%. В ряде случаев заболевание развивается медленно, к концу первой недели жизни проявляясь вялостью ребенка, слабым сосанием, срыгиваниями, затянувшейся желтухой. На этом фоне повышается температура до 38—39 °С, появляются менингеальные симптомы. Исследование спинномозговой жидкости подтверждает диагноз менингита. Что касается других бактерий, то их роль как возбудителей внутриутробных инфекций не столь значительна. В частности, патогенный стафилококк, доминирующий среди внутригоспитальных инфекций, не занимает существенного места среди возбудителей внутриутробных инфекций. Д и а г н о с т и к а. Диагноз внутриутробных бактериальных инфекций ставить трудно из-за сходства их клинической картины с явлениями, вызванными тяжелой внутриутробной гипоксией. Кроме того, при различной этиологии заболеваний наблюдается однотипная патоморфологическая картина в органах погибших новорожденных детей. В связи с этим особое значение для диагностики имеет совокупность анамнестических, клинических и лабораторных данных. Бактериологические исследования необходимо проводить у всех детей из группы риска внутриутробного инфицирования и их матерей. В родильном зале делают забор околоплодных вод, тканей плаценты, оболочек, пуповинной крови. У новорожденного берут мазки из зева, носа и кожи, посылают на исследование первые порции мекония и содержимое желудка. Определяют содержание иммуноглобулинов в пуповинной крови: повышение концентрации IgM (> 0,2 г/л) и появление IgA являются показателями реакции плода на инфекцию. Для выявления у ребенка активного инфекционного процесса используют 5 тестов: — общее число лейкоцитов < 5,0 х 109/л; — отношение числа палочкоядерных форм к общему числу нейтрофилов > 2; — С-реактивный белок (латексный метод определения) > 8 мг/л; — С О Э в первый час жизни > 15 мм в час; — гаптоглобин (латексный метод определения) > 0,25 г/л. Определяют количество тромбоцитов в крови: тромбоцитопения характерна для внутриутробных бактериальных инфекций. Важное значение для подтверждения инфицирования плода имеют патомор-фологические исследования плаценты, пуповины и оболочек. Л е ч е н и е. Учитывая быстротечность бактериальных внутриутробных инфекций, надо начинать лечение с первого часа жизни. Основным антибиотиком является ампициллин, к которому чувствительны стрептококки и некоторые грамотрицательные микроорганизмы. Пенициллин и ампициллин комбинируют с антибиотиками группы аминогликозидов. Антибиотики назначают в больших дозах. Длительность применения зависит от их эффективности. При подозрении на внутриутробное инфицирование в первые часы жизни вводят витамины Е, А, иммуноглобулины. Далее продолжают терапию, включающую средства, направленные на нормализацию гемодинамики, кислотно-основного состояния крови, дегидратацию, детоксикацию, на профилактику и ЧАСТЬ 2 ПАТОЛОГИЧЕСКОЕ АКУШЕРСТВО лечение ДВС-синдрома. При необходимости осуществляют оксигенотерапию. При отсутствии у матери клинических признаков острого инфекционного процесса ребенка следует кормить сцеженным материнским молоком. Глава 44 ИНФЕКЦИИ Y НОВОРОЖДЕННЫХ Инфицирование ребенка в постнатальном периоде происходит через руки персонала, матери и при непосредственном контакте с источником инфекции в окружающей среде (пеленки, оборудование, инфузионные растворы, питательные смеси и т. д.). Чаще всего инфицирующими агентами являются стафилококки, стрептококки, грамотрицательные микробы (кишечная палочка, клебсиелла, вульгарный протей, синегнойная палочка). Источником кишечной инфекции (например, сальмонеллеза) может быть заболевший ребенок, заразившийся от матери или от бациллоносителя из числа медицинского персонала. Передача возбудителя другим детям происходит оральным путем, главным образом через зараженные руки персонала. Бактериальные инфекции в отделениях новорожденных обычно протекают в виде вспышек, чаще заболевают дети старше 5—6-го дня жизни. Сначала появляются малые формы стафилококковых инфекций: гнойные конъюнктивиты, везикулопустулез, панариции, катаральный омфалит, ринит. Они протекают без интоксикации, без подъема температуры или с коротким субфибрилитетом, без анемизации и продолжаются 3—7 дней. Наиболее легкая форма стафилококкового поражения кожи — пиодермия. На ограниченном участке кожи появляются один или несколько пузырей размером с булавочную головку. При вскрытии их остаются эрозии, которые в течение 1—2 дней полностью эпителизируются. Наиболее частая область поражения — кожа вокруг пупочной ранки, внизу живота, подмышечной впадины, шеи, ягодиц, мошонки. Лечение местное: туалет кожи, купание в ванне с 0,005% раствором калия перманганата, обработка пораженных участков 70° спиртом и раствором бриллиантового зеленого. К локализованным формам гнойных инфекций, протекающим с интоксикацией, относят следующие: 1) поражения кожи — стафилококковая пузырчатка, множественные абсцессы, флегмона; 2) поражения пупочной вены; 3) железистые формы — мастит, орхит, паротит; 4) поражение костей — остеомиелит; 5) пневмонии, энтериты. Дата добавления: 2015-12-15 | Просмотры: 990 | Нарушение авторских прав |