|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Связь оценки состояния плода по шкале Апгар с велигиной рН артериальной крови
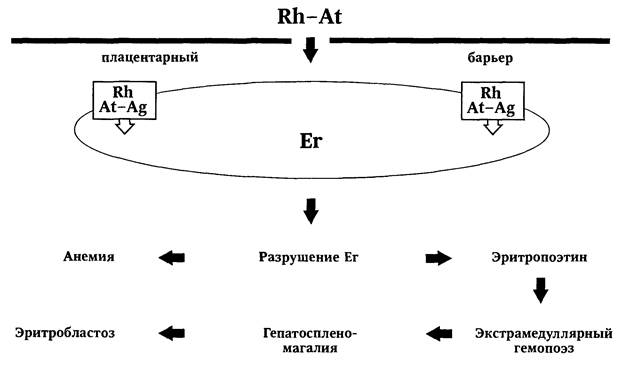
П р и м е ч а н и е. В двух случаях может иметь место несоответствие между оценкой по шкале Апгар и величиной рН крови: 1) низкая оценка по шкале Апгар сочетается с нормальным или лишь незначительным снижением рН, если причиной асфиксии новорожденного является медикаментозная депрессия вследствие проведения матери наркоза или обезболивания родов; 2) относительно высокая оценка по шкале Апгар может сочетаться с низким значением рН у маловесных новорожденных, перенесших хроническую внутриутробную гипоксию. Согласно международной классификации болезней (Женева, 1980), выделяют тяжелую и легкую степени тяжести асфиксии новорожденных. Раздел 4. Патология плода и новорожденного Тяжелая асфиксия: оценка по шкале Апгар в 1-ю минуту жизни 0—3 балла, к 5-й минуте становится выше 6—7 баллов. Легкая асфиксия: оценка по шкале Апгар в 1-ю минуту жизни 4—6 баллов, через 5 минут 8—10 баллов. Реанимация новорожденного при асфиксии. П е р в ы й э т а п. Первичная реанимация при рождении ребенка в асфиксии проводится в родильном зале. Отсасывание содержимого носовых ходов и полости рта производится во время родов после прорезывания головки. После отсечения пуповины новорожденного кладут с наклоном головы (15°) на стол, обогреваемый источником лучистого тепла. Ребенка необходимо быстро обтереть, так как потеря тепла у него в связи с испарением очень велика, а механизм теплообразования в условиях гипоксии оказывается нарушенным. У детей, подвергшихся переохлаждению, усугубляется обменный ацидоз, гипоксия и может развиться гипогликемия. При рождении ребенка в тяжелой асфиксии следует немедленно интубиро-вать трахею и отсосать слизь и околоплодные воды. Необходимо прослушать дыхательные шумы, чтобы убедиться в правильном положении эндотрахеальной трубки и хорошем газовом обмене. В случае брадикардии (80 уд/мин) помощник проводит массаж сердца с частотой 100— 120 движений в минуту, координируя его с ИВЛ 100-процентным кислородом (3 надавливания на грудину — 1 вдох) до тех пор, пока собственный сердечный ритм ребенка не достигнет 100 уд/мин. Одновременно второй помощник катетеризирует пупочную вену и медленно вводит 5—10% раствор глюкозы вместе с кокарбоксилазой (8—10 мл/кг). Последняя не только улучшает метаболизм, увеличивая образование АТФ, но и способствует нормализации состава электролитов в клетках и устранению внутриклеточного ацидоза. Кроме того, устраняя избыток пировиноградной и молочной кислот, она нормализует рН плазмы и тканевой жидкости. Если сердечная деятельность не восстанавливается или сохраняется брадикар-дия, необходимо ввести внутривенно 0,05—0,1 мл 0,1% раствора атропина, а при отсутствии эффекта — 0,1 мл 0,1% адреналина. Последний можно ввести непосредственно в эндотрахеальную трубку. Для точности дозирования 1 мл препарата разводят до 10 мл изотоническим раствором натрия хлорида и вводят 0,5—1 мл. При стойкой брадикардии вводят 1 мл 10% раствора кальция глюконата. Стимуляторы дыхания применяются только в том случае, если известно, что за час до рождения ребенка мать получала наркотические вещества. С целью борьбы с медикаментозной депрессией вводят налоксон (0,01 мл/кг внутривенно или внутримышечно или этимизол 0,1 мл/кг). В тех случаях, когда асфиксия новорожденного возникла на фоне длительной хронической внутриутробной гипоксии (о чем свидетельствует тяжелая экстраге-нитальная патология матери, осложнение беременности поздним гестозом, перенашивание), то для устранения возможного метаболического ацидоза ребенку после восстановления адекватного легочного дыхания следует ввести в вену 5% раствор натрия бикарбоната в дозе 2—2,5 мл/кг. Если через 5 мин после начала реанимационных мероприятий оценка новорожденного по шкале Апгар остается не выше 6 баллов, рекомендуется ввести внутривенно раствор преднизолона (1 мг/кг) или гидрокортизона (5 мг/кг). В случае эффективности проводимых мероприятий частота сердечных сокращений и артериальное давление возрастают, увеличивается пульсовое давление, падает центральное венозное давление и ребенок розовеет. ЧАСТЬ 2 ПАТОЛОГИЧЕСКОЕ АКУШЕРСТВО При рождении ребенка в легкой асфиксии достаточно эффективной оказывается вентиляция 100-процентным кислородом через маску с помощью аппарата или системы Айра. Поток 02 не должен превышать 10 л в минуту, а частота дыхания — 40 в минуту. В т о р о й э т а п реанимации состоит в оценке эффективности ИВЛ и адекватности объема циркулирующей крови. ИВЛ через 3 мин прекращают на 15—30 с, чтобы проконтролировать появление спонтанных дыхательных движений. Однако этот момент не является показанием для прекращения ИВЛ, так как часто сохраняется частичный ателектаз легких, самостоятельное дыхание недостаточно эффективно. В этих случаях ИВЛ должна быть продолжена, причем необходимо подобрать такую минимальную концентрацию кислорода, при которой нет цианоза, а напряжение кислорода в тканях составляет 60—70 мм рт. ст. Используют И В Л с положительным давлением в конце выдоха 2—5 см вод. ст. При синдроме массивной аспирации перед ИВЛ необходимо провести санацию трахеобронхиального дерева 2% раствором натрия гидрокарбоната и отсосать содержимое желудка. Т р е т и й э т а п реанимации включает переход на самостоятельное дыхание, профилактику вторичной гипоксии, коррекцию нарушений метаболизма. Если через 20 мин от начала реанимации самостоятельное дыхание не восстанавливается, оживление ребенка следует прекратить. Глава 41 ГЕМОЛИТИЧЕСКАЯ БОЛЕЗНЬ П Л О Д А И НОВОРОЖДЕННОГО Гемолитическая болезнь (ГБ) плода и новорожденного является патологическим состоянием, возникающим в результате несовместимости крови матери и плода по некоторым антигенам, при котором происходит гемолиз эритроцитов плода под влиянием изоантител матери, проникающих через плацентарный барьер. Чаще всего заболевание развивается в результате резус-конфликта или конфликта по системе ABO (1 случай на 250-300 родов). Удельный вес ГБ в структуре перинатальной смертности составляет 3,5%. Существуют т р и о с н о в н ы х в и д а R h - ф а к т о р а: антигены D (Rh), С (Rhj) и Е (Rhn) и т р и р а з н о в и д н о с т и а н т и г е н а Hr: d, с, е. Наиболее выраженными антигенными свойствами обладает фактор D. Из Нг-факторов большей способностью вызывать образование антител отличается фактор с. Э т и о л о г и я и п а т о г е н е з. Конфликт вследствие изосерологической несовместимости матери и плода чаще всего развивается по эритроцитарным антигенам Rh-Hr и AB0. В зависимости от этнической принадлежности, частота резус-отрицательной принадлежности крови в популяции варьирует от менее 1% у китайцев, до 30% и более у басков. У европейцев частота в среднем составляет 15%. Изоиммуни-зация может явиться следствием двух основных причин: Раздел 4 Патология плода и новорожденного — первая, к счастью, все реже и реже встречающаяся — ятрогенная. Она связана с введением в организм женщины резус-положительной крови при проведении ей в прошлом переливаний крови или при аутогемотера-пии; — вторая является основной — это плодово-материнский трансплацентарный перенос эритроцитов плода в кровоток матери во время беременности и родов. Rh-изоиммунизация — это иммунный ответ организма матери на попадание в него чужеродных для него антигенов, находящихся на мембране эритроцитов плода. Размеры и формы эритроцитов плода и взрослого человека различны, поэтому путем количественного определения в циркуляции матери эритроцитов плода можно косвенно судить об объеме плодово-материнских трансплацентарных кровотечений. Их частота и объем существенно увеличиваются по мере прогрессирования беременности. Если в течение I триместра беременности они регистрируются только у 3% беременных (их объем составляет около 0,03 мл), то в III триместре они выявляются у 45% беременных женщин и расчетный объем трансплацентарных кровотечений достигает 25 мл. Первичный иммунный ответ после попадания D-антигена в кровоток матери проявляется через определенное время — от 6 недель до 12 месяцев. Он состоит в появлении иммуноглобулинов класса М, молекулы которых имеют значительные размеры и не проникают к плоду через плацентарный барьер. Это объясняет отсутствие гемолитической болезни у плодов большинства первобеременных резус-отрицательных женщин. Попадание D-антигена в кровоток матери при повторной беременности вызывает быстрый вторичный иммунный ответ в виде образования небольших по своему размеру иммуноглобулинов класса G, которые, свободно проникая через плацентарный барьер, осаждаются на мембране эритроцитов резус-положительного плода, приводя к их гемолизу. Rh-антигены обнаруживаются на мембране эритроцита плода уже к 30-му дню беременности. Циркулирующие при повторной беременности анти-Б-антитела (иммуноглобулины G) проникают через плацентарный барьер, связываются с соответствующими антигенами на мембране эритроцитов, что вызывает ускоренное разрушение последних в органах ретикулоэндотелиальной системы. Массивное разрушение эритроцитов приводит к развитию анемии у плода (анемическая форма), появление которой вызывает повышение концентрации эрит-ропоэтина в кровотоке у плода. Эритропоэтин, в свою очередь, стимулирует гемопоэз, в результате которого появляются очаги экстрамедуллярного кроветворения, в основном в печени и селезенке плода, которые существенно увеличиваются (рис. 94) Экстрамедуллярный гемопоэз характеризуется незавершенностью развития эритроцитов и появлением в циркуляции эритробластов. Хотя непрямой билирубин, образующийся при гемолизе эритроцитов плода, интенсивно выводится через плаценту, повышение его концентрации нарушает синтез белков в печени плода, уже измененный за счет появления экстрамедуллярного гемопоэза. Следствием этого патологического процесса становится гипопротеинемия, снижение онкотического давления плазмы крови плода и портальная гипертензия. Развитие анемии у плода приводит к снижению кислородной емкости его крови. Это, в свою очередь, влечет за собой усиление анаэробного гликолиза в тканях, ацидоз, снижение буферных резервов крови, повреждение эндотелия капилляров и развитие хронической гипоксии. На фоне хронической гипоксии и ацидоза возникает компенсаторное увеличение 13 Зак 384
Рис. 94. Механизм развития анемии у плода Раздел 4 Патология плода и новорожденного сердечного выброса и минутного объема, приводящее к гипертрофии миокарда и постепенному развитию сердечной недостаточности, и как следствие, к повышению центрального венозного давления (ЦВД). Повышение ЦВД затрудняет ток лимфы по магистральным лимфатическим сосудам, вызывая нарушение оттока интерстициальной жидкости и увеличение ее онкотического давления. Весь комплекс происходящих патологических процессов вызывает накопление жидкости в тканях и серозных полостях плода, что клинически проявляется развитием у него генерализованного отека (отечная форма ГБ) и при отсутствии соответствующего лечения приводит к внутриутробной гибели плода. Понимание патофизиологии развития гемолитической болезни плода позволило разработать методы профилактики изоиммунизации Rh-отрицатель-ных беременных женщин, методы диагностики и легения гемолитической болезни плода и новорожденного. Всем беременным женщинам при первом же визите к врачу следует провести т и п и р о в а н и е по группе крови и R h - ф а к т о р у, а также опреде-л е н и е а н т и р е з у с н ы х антител. При выявлении Rh-отрицательной принадлежности крови беременной, имеющей Rh-положительный фактор у мужа, показано повторное определение антирезусных антител каждые 4 недели вплоть до родов. Следует помнить о том, что резус-положительные лица могут быть гомозиготными или гетерозиготными, тогда как резус-отрицательные — только гомозиготными. Это имеет практическое значение, поскольку потомство гомозиготного резус-положительного отца и резус-отрицательной матери будет резус-положительным в 100% случаев. Если отец гетерозиготный, вероятность для плода быть резус-положительным составит только 50%. Анамнез Rh-изоиммунизированной беременной женщины имеет большое значение в оценке риска развития тяжелых форм гемолитической болезни. Титр антител в крови беременной женщины и его динамика могут быть использованы для оценки степени тяжести гемолитической болезни. При этом границей, после которой возможно развитие клинически значимых форм гемолитической болезни плода, является титр 1: 8. При последующих беременностях величина титра Rh-антител в крови матери не имеет корреляции со степенью тяжести гемолитической болезни плода и, кроме того, отек у плода может развиться при минимальной величине титра антител — 1: 2. Опыт применения у л ь т р а з в у к о в о г о с к а н и р о в а н и я для диагностики и определения степени тяжести гемолитической болезни плода показывает его высокую чувствительность и специфичность при развитии у плода только тяжелой — отечной формы заболевания, о чем свидетельствует определение свободной жидкости в его серозных полостях. При других формах гемолитической болезни плода чувствительность и специфичность однократного ультразвукового исследования низки. Однако ценность ультразвукового исследования может быть увеличена при динамическом наблюдении за состоянием плода одним и тем же исследователем. При этом уделяется внимание размерам печени, селезенки, толщине плаценты и эхогенности кишечника, что имеет особое значение для выявления самых начальных стадий развития отека у плода и его разрешения на фоне внутриматочного лечения. Кроме того, косвенным показателем наличия анемии у плода, не имеющего отека, может служить увеличение скорости кровотока в средней мозговой его артерии и аорте, определяемой при д о п п л е р о м е т р и и с использованием цветного допплеровского картирования. Изменение скорости кровообращения связано с формированием гипердинамического типа циркуляции у плода, формирующейся на фоне развивающейся анемии, а также обусловленным Ч А С Т Ь 2. ПАТОЛОГИЧЕСКОЕ АКУШЕРСТВО возрастанием сердечного выброса на фоне увеличения венозного возврата, являющегося следствием снижения вязкости крови. Этот критерий, оцененный в динамике, может быть использован как дополнительный маркер для определения оптимальных сроков начала инфузий и их повторов при анемической форме гемолитической болезни. Т а к т и к а в е д е н и я беременности при Rh-изоиммунизации беременной женщины зависит от Rh-принадлежности плода. Существует возможность определения Rh-генотипа плода при помощи моле-кулярно-генетических методов с использованием л ю б ы х клеток плодового происхождения, что дает уникальную возможность определять тактику ведения Rh-иммунизированных женщин уже в начале беременности. Полимеразная цепная реакция имеет 100% чувствительность и специфичность при определении Rh-генотипа плода. Амниоцентез является наиболее безопасным инвазивным вмешательством для плода в период с 14-й по 18-ю неделю беременности, так как это наилучший срок для Rh-типирования плодов у Rh-иммунизированных беременных женщин. Очевидно, в ближайшем будущем совершенствование методов выделения клеток крови плода в периферической крови матери (а клетки крови плода всегда присутствуют в кровотоке матери за счет плодово-маточных трансфузий) постепенно вытеснит из клинической практики инвазивные вмешательства во время беременности для определения Rh-генотипа плода. В настоящее время оценка степени тяжести гемолитигеской болезни плода базируется на инвазивных вмешательствах. Начиная с 1961 г. анализ оптической плотности околоплодной жидкости, полученной при амниоцентезе, был основным методом диагностики степени тяжести гемолитической болезни. Однако этот метод имеет очевидные недостатки. Речь идет, прежде всего, о весьма высокой частоте ложноположительных и ложноотрицательных результатов, особенно во II триместре беременности, и о необходимости повторных, 2-4-кратных операций амниоцентеза. Все это послужило толчком для поиска методов получения крови плода и ее прямого исследования. Разработка в 1983 г. метода получения крови плода при помощи кор-доцентеза — пункции сосудов пуповины под ультразвуковым контролем — открыла новую страницу в диагностике и лечении гемолитической болезни плода. Этот метод может быть использован уже в конце первой половины беременности, что имеет принципиальное значение при необходимости диагностики раннего развития тяжелых форм гемолитической болезни плода (см. рис. 36, с. 118). Анализ гематологических показателей у плодов при неосложненном течении беременности позволил определить границы нормального распределения величин всех показателей крови в зависимости от срока беременности. Все основные показатели, позволяющие оценить степень анемии у плода, такие как величина гемоглобина и гематокрита, а также содержание эритроцитов, повышаются по мере прогрессирования беременности. При этом в начале второй половины физиологически протекающей беременности уровень гемоглобина составляет 120 г/л и возрастает к 37-й неделе до 140 г/л. Средний уровень гематокрита крови повышается с 36 до 43%. Классификация степеней тяжести гемолитической болезни плода зависит от величин гематокрита и гемоглобина его крови, полученной при кордоцентезе (табл. 25). Раздел 4. Патология плода и новорожденного Таблица 25 Дата добавления: 2015-12-15 | Просмотры: 908 | Нарушение авторских прав |