 |
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Примеры решения типовых задач.Задача 1. Какова молярная концентрация эквивалента раствора HCl, если на титрование 10,00 мл его расходуется 12,50 мл 0,08000 н. раствора KOH? Решение: используем формулу C1.V1 = C2V2 ;
Задача 2. Чему равен титр 0,05000 н. раствора H2SO4? Решение: по формуле Т = Задача 3. Сколько моль эквивалентов содержится в 800,0 мл 0,1500 н. раствора? Решение: число моль эквивалентов может быть найдено по одной из формул:
В нашем случае возможно вычисление: Задача 4. Сколько граммов Na2CO3 содержится в 450,0 мл 0,08000 н. раствора? Решение: используем формулу:
Задача 5. Сколько граммов KOH содержится в растворе, если на его титрование расходуется 21,35 мл 0,2000 н. раствора HCl? Решение: т.к. n(KOH) = n(HCl), то m(KOH) = n(HCl) ·1/z·M(КОН) = = Задача 6. Какова молярная концентрация эквивалента, если фиксанал «0,05 эквивалента» HCl растворён в мерной колбе объемом 500,0 мл? Решение: используем формулу Тема: Кислотно-основное титрование (метод нейтрализации). Домашнее задание для подготовки к занятию. Выучите расчётные формулы и правила титрования. Письменно решите задачи: 1.Сколько граммов HNO3 содержится в 500 мл раствора, если титр его равен 0,006302 г/мл? (Ответ: 3,151 г). 2.Титр раствора HCl равен 0,003600 г/мл. Вычислите его молярную концентрацию эквивалента. (Ответ: 0,09874). 3. На титрование 20,00 мл раствора HNO3 затрачено 15,00 мл 0,1236 н раствора NaOH. Вычислите молярную концентрацию эквивалента, титр и массу HNO3 в 250 мл раствора. (Ответ: С = 0,09764; Т = 0,006154 г/мл, m = 1,5384 г). 4.Какой объем 0,1586 н раствора NaOH пойдет на титрование: а) 21,00 мл 0,1133 раствора HCl; б) 21,00 мл раствора HCl с титром 0,00381? (Ответ: а) 15,00 мл; б) 13,84 мл). 5.Определите молярную концентрацию эквивалента раствора хлорида железа (III), если в 0,3 л раствора содержится 32,44 г его. (Ответ: С[1/3(FeCl3)] = 2 моль/л). 6.Вычислите молярную концентрацию эквивалента 10%-го раствора CuSO4, плотность которого 1,107 г/мл. (Ответ: С(1/2 CuSO4) = 1,4 моль/л). Дата добавления: 2015-12-16 | Просмотры: 3674 | Нарушение авторских прав |
 моль/л
моль/л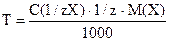
 г/мл.
г/мл.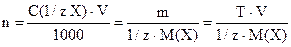
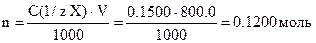
 ;
;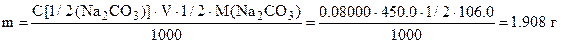
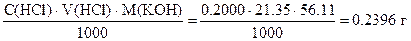
 , откуда
, откуда 