|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология
|
ПРЕНАТАЛЬНАЯ ПАТОЛОГИЯ
ПОНЯТИЕ О ПЕРИОДИЗАЦИИ И ЗАКОНОМЕРНОСТЯХ
ПРОГЕНЕЗА И КИМАТОГЕНЕЗА
В понятие «пренатальная (синоним: антенатальная) патология» включают-
ся все патологические процессы и состояния человеческого зародыша, начиная
с оплодотворения и кончая рождением ребенка. Пренатальный период челове-
ка исчисляется длительностью беременности — 280 днями, или 40 нед, по ис-
течении которых наступают роды.
Учение о внутриутробной патологии (уродствах и пороках развития) возникло очень давно.
В арабской медицине XI, XII и XIII веков имелись уже подробные описания различных вро-
жденных пороков. Амбруаз Паре (1510—1590) написал о них специальную книгу. Однако науч-
ное изучение этого вопроса началось в начале XX века (Швальбе). При этом большинство иссле-
дователей считали, что основное значение в развитии врожденных пороков у человека имеет
наследственность. Большое значение для понимания влияния факторов внешней среды на фор-
мирование пороков развития имело открытие австралийского офтальмолога Грегга, который
в 1951 г. опубликовал свои данные о значении вируса краснухи (рубеолы) в возникновении мно-
жественных врожденных пороков развития у человека. Он показал, что при заболевании матери
краснухой в первую треть беременности у 12 % детей развиваются врожденные пороки и в 7,2 %
отмечается мертворожденность, во вторую треть беременности — 3,8 и 4,6 % соответственно,
в последнюю треть беременности пороков развития у плода не возникает, а мертворожденность
имеет место в 1,7 % случаев. С этого момента сформировалось учение о возможности проявле-
ния пороков развития у человека, обусловленных воздействием экзогенных факторов, и под-
твердились данные об основном значении времени воздействия этих факторов на развивающий-
ся зародыш.
В настоящее время пренатальная патология человека выросла в проблему,
имеющую не меньшее значение в медицине, чем проблема сердечно-сосу-
дистых заболеваний, опухолей и психических болезней.
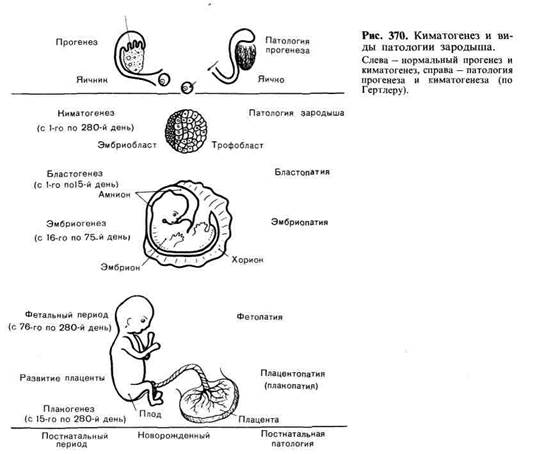
Все развитие, начиная от созревания половой клетки (гаметы) до рождения
зрелого плода, делят на два периода — период прогенеза и период киматоге-
неза (от греч. kyema — зародыш) (рис. 370). Периоду прогенеза соответ-
ствует созревание гамет (яйцеклетки и сперматозоида) до оплодотворения.
В этот период возможно возникновение патологии гамет— гамето-
п а т и и. В зависимости от того, в каких структурах наследственного аппарата
гаметы произошла мутация, различают генные, хромосомные и геномные му-
тации. Наследственные болезни, в том числе и пороки развития, могут быть
следствием мутаций гамет родителей ребенка (спонтанные мутации) или его
отдаленных предков (унаследованные мутации).
Период киматогенеза исчисляется с момента оплодотворения
и образования зиготы до родов и делится на три периода. Первый период —
бластогенез — продолжается с момента оплодотворения до 15-го дня бере-
менности, когда идет дробление яйца, заканчивающееся выделением эмбрио-
и трофобласта. Второй период — эмбриогенез — охватывает отрезок вре-
мени с 16-го по 75-й день беременности, когда осуществляется основной органо-
генез и образуются амнион и хорион. Третий период — фетогенез — продол-
жается с 76-го по 280-й лень, когда идут дифференцировка и созревание тка-
ней плода, а также образование плаценты, заканчивающиеся рождением
плода. Период фетогенеза делят на ранний фетальный (с 76-го по 180-й
день), к концу которого незрелый плод приобретает жизнеспособность, и п о -
зднийфетальный(с 181-го по 280-й день), когда завершается созревание
плода с одновременным старением плаценты. С периодом киматогенеза со-
впадает киматопатия. Соответственно периодам киматогенеза разли-
чают:бластопатию, эмбриопатию, раннююипозднюю фето-
п ати и.
Этиология. После открытия рубеолярной эмбриопатии расширились пред-
ставления о влиянии экзогенных факторов, приводящем к киматопатиям. Это
нашло свое подтверждение в многочисленных экспериментальных исследова-
ниях.
По современным' данным, 20 % пороков развития (основная патология пе-
риода киматогенеза) связано с генными мутациями, 10%—с хромо-
сомными аберрациями, 1О % — с влиянием экзогенных факто-
ров, 60 %— с невыясненной этиологией. Полагают, что в патологии человека
часто имеет место комбинация наследственных и экзогенных факторов, когда
влияние экзогенных факторов оказывается лишь провоцирующим.
К экзогенным факторам, способным вызывать киматопатии у че-
ловека, относятся вирусы и некоторые другие микроорганизмы, а именно ви-
русы краснухи, кори, ветряной оспы herpes simplex, инфекционного монону-
клеоза, эпидемического паротита и гепатита, полиомиелита и гриппа, а также
микоплазма, листерелла, трепонема, токсоплазма, реже микооактерия тубер-
кулеза и др. Кроме инфекционных агентов, киматопатии могут быть обусло-
влены влиянием лучевой энергии (у-лучи), ионизирующей радиа-
ции, некоторыми лекарственными препаратами — талидомидом,
гидантоином, цитостатическими средствами, гормонами, витаминами (в част-
ности, витамином D), хинином и др., алкоголем, гипоксией различно-
го генеза, эндокринными заболеваниями матери — сахарным диа-
бетом, тиреотоксическим зобом. Употребление во время беременности
алкоголя приводит к развитию алкогольной эмбриофетопатии, ха-
рактеризующейся общей гипоплазией, умеренной недоношенностью, микроце-
фалией, сочетающейся с птозом век, эпикантом, микрогенией. Реже встре-
чаются врожденные пороки сердца.
В настоящее время в связи с новыми методами лечения получили особое
значение диабетические и тиреотоксические фето- и эмбриопатии. До лечения
инсулином у женщин, страдающих сахарным диабетом, беременность наблю-
далась редко. В настоящее время способность к деторождению у этих женщин
такая же, как и у здоровых. Однако у детей, матери которых больны са-
харным диабетом, пороки развития отмечаются чаще. К так называемой
диабетической эмбриопатии относятся пороки развития скелета,
сердечно-сосудистой, центральной нервной и мочеполовой систем. Диабе-
тическая фетопатия проявляется в виде недоношенности или рождения
гигантского плода кушингоидного вида. При повышенной и пониженной
функциях щитовидной железы наблюдается склонность к абортам и выкиды-
шам. Среди пороков развития при тиреотоксикозах преобладают анэнцефа-
лия, пороки сердца, гипотиреозы с умственной отсталостью — так называемые
тиреотоксические эмбриофетопатии.
Патогенез. Механизм развития киматопатии изучен пока недостаточно, так
как методов изучения киматопатии в динамике мало. Кроме того, приходится
иметь дело с двумя биологическими объектами — матерью и зародышем, на-
ходящимися в сложных взаимоотношениях.
Первая закономерность, характерная для патологии внутриутроб-
ного периода при любом патогенном воздействии, — обязательное искажение
нормального хода развития зародыша. Поэтому для понимания патогенеза
пренатальной патологии большое значение имеет изучение реактивности за-
родыша в разные периоды киматогенеза, так как основной жизненной функ-
цией зародыша является беспрерывно идущий процесс морфогенеза. На про-
цессах формообразования в первую очередь и сказывается влияние пато-
генных факторов.
Нарушение хода морфогенеза называется дизонтогенезом. Однако
в разные периоды киматогенеза расстройства дизонтогенеза возникают на
разных уровнях — от грубых нарушений развития зародыша, несовместимых
с жизнью на ранних его этапах, до нарушения тонких ультраструктур клеток
и тканей на поздних этапах. По мере созревания зародыша у него постепенно
развивается способность реагировать на различные патогенные влияния не
только нарушением морфогенеза, но и развитием других патологических про-
цессов — альтерации тканей, воспаления, иммуноморфологических и компен-
саторно-приспособительных сдвигов, полной и неполной регенерации тканей.
Второй закономерностью, характерной для патологии особенно
поздних периодов киматогенеза, является сочетание нарушений морфогенеза
с другими патологическими процессами, например пороков формирования
сердца с гиперплазией мезенхимальных тканей, пороков формирования голов-
ного мозга с наличием некрозов, кровоизлияний и др.
Третьей закономерностью, определяющей патогенез любого из
периодов киматогенеза и имеющей большое значение в развитии того или
иного патологического состояния зародыша, является время воздей-
ствия на него патогенного агента.
Так, в период бластогенеза зародыш на любое воздействие отвечает нару-
шением имплантации оплодотворенного яйца или развития эмбрио- и трофо-
бласта в бластоцисте. В период эмбриогенеза, когда осуществляется основной
морфогенез внутренних органов и частей тела зародыша, почти любое повре-
ждение приводит к развитию того или иного врожденного порока или к гибе-
ли эмбриона.
По данным советских эмбриологов П. Г. Светлова и А. П. Дыбана, пренатальная гибель за-
родыша чаще наблюдается в определенные сроки его внутриутробной жизни. Для эмбриона
млекопитающих и человека такими периодами особо высокой чувствительности к патогенным
агентам являются имплантация оплодотворенного яйца в слизистую оболочку матки, что со-
ответствует 14 дням внутриутробного развития, и плацентация — начало формирования пла-
центы, что соответствует 3-6 нед внутриутробного развития. Эти два периода наибольшей чув-
ствительности зародыша к воздействию повреждающих агентов получили название первого
ивторогокритическихпериодов. Однако гибель эмбриона в большинстве случаев на-
ступает не сразу после повреждения, а через некоторое время, так как сроки пренатальной
смертности запаздывают по отношению к названным срокам критических периодов. Так, оказа-
лось, что для первого критического периода наибольшая пренатальная смертность приходится
на 4-ю неделю беременности, а для второго — на 8 —11-ю неделю. Такое запаздывание соответ-
ствует клиническим наблюдениям, по которым преобладающая часть самопроизвольных абор-
тов у женщин зарегистрирована именно в сроки от 4 до 10—11 нед беременности.
Оказалось, что различные тератогенные агенты могут привести
кодномуитомужепорокуразвитияв зависимости от времени воз-
действия на эмбрион; например, влияние лучевой энергии и хинина на 3-й не-
деле внутриутробного развития приводит к нарушениям формирования нерв-
ной трубки зародыша.
Вместе с тем один и тот же тератогенный агент может вызвать разные по-
роки развития, воздействуя в различные сроки эмбриогенеза.
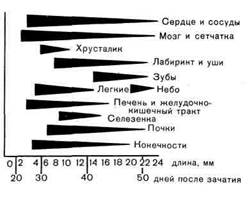
Рис. 371. Схематическое изображение терато-
генного терминационного периода отдельных
органов и частей тела (по Гертлеру).
Известно, что при поражении эмбриона виру-
сом краснухи возникает рубеолярная эмбриопа-
тия (синдром Грегга), которая заключается в по-
роках развития глаз, сердца, мозга, зубных за-
чатков и внутреннего уха. При этом пороки раз-
вития глаз (катаракта, микрофтальмия и др.) по-
являются в тех случаях, если мать переносит крас-
нуху в последнюю декаду I месяца или в
первые две декады II месяца беременности,
пороки развития мозга (микроцефалия) — в тече-
ние всего II месяца, внутреннего уха — в тре-
тью декаду II и в первую декаду III месяца
беременности.
Для каждого органа существует определенный отрезок времени, в течение
которого при воздействии тератогенного агента возникает порок развития
этого органа. Этот отрезок времени получил название тератогенного
терминационного периода (от лат. teratos — уродство и terminus —
предел, граница), т. е. предельного срока, в течение которого тератогенный
фактор может вызывать врожденный порок (рис. 371). Пользуясь данными
эмбриологии, можно судить о сроках возникновения того или иного порока
развития и составить так называемые тератологические календари для поро-
ков развития различных органов. Как показывают данные экспериментальной
тератологии, чувствительность развивающегося органа к повреждающим
агентам определяется степенью его митотической активности: чем выше ми-
тотическая активность развивающихся тканей, тем чувствительнее они к тера-
тогенным агентам.
Необходимо учитывать, что повреждающий агент может обладать боль-
шим или меньшим сродством к тем или иным тканевым зачаткам, что обус-
ловливает иногда некоторые специфические черты, характерные для опреде-
ленного патогенного агента.
Так, с 1957 по 1964 г. в ФРГ и других странах имела место так называемая талидомидная
катастрофа. Талидомид применялся в качестве успокаивающего (снотворного) средства. Оказа-
лось, что малые дозы этого препарата опасны для человеческого эмбриона; на животных они не
действуют. У многих женщин, принимавших талидомид на II месяце беременности, рождались
дети с тяжелыми пороками развития конечностей — амелией, фокомелией. В 40 % случаев пора-
жались верхние конечности, в 10% —нижние, в 20% —верхние и нижние конечности, в 20% —
конечности (верхние и нижние), органы слуха и зрения (данные 1961 и 1962 гг.). По данным 1964 г.,
в 45 % случаев талидомидные эмбриопатии протекали с пороками развития внутренних орга-
нов. Из приведенного наблюдения видно, что талидомид имеет особый тропизм к развиваю-
щимся закладкам конечностей.
Кроме нарушений морфогенеза, удалось показать, что у эмбриона могут
наблюдаться резорбция его некротизированных тканей, отек тканей, кровоиз-
лияния и в конце эмбриогенеза даже неполная регенерация с образованием
рубцов. Следует учитывать, что отмирание тканевых зачатков наблюдается
и при нормальном ходе морфогенеза, например при слиянии отдельных за-
чатков, образовании полостей в них, разрывах мембран (глоточной, клоакаль-
ной) и др. Однако по объему и характеру процесс физиологического отмира-
ния клеток отличается от некрозов в условиях патологии, он не сопрово-
ждается рубцеванием, а главное, не приводит к нарушению процессов
формирования. Обширные некрозы тканей эмбриона с рубцеванием по-
являются, вероятно, при эмбриопатиях, обусловленных действием экзогенных
агентов. При генотипических пороках развития значительной альтерации за-
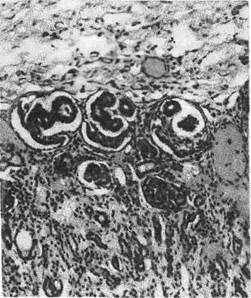
Рис. 372. Клубочки зародышевого типа в коре
почки у мальчика в возрасте 7 дней.
чатков органов, вероятно, не бывает,
а имеется задержка процессов диф-
ференцировки зачатков.
Конкретных данных по патогене-
зу наследственно обусловленных по-
роков развития человека пока очень
мало. Указанная разница в патогене-
зе генетических и экзогенных поро-
ков развития лишь предположитель-
ная. В подавляющем большинстве
случаев морфология сложившегося
порока развития неспецифична. По-
этому отличить по внешнему виду
генотипический порок от
фенокопии1 невозможно. Осно-
вным проявлением патоло-
гии эмбрионального пе-
риода является дизонтоге-
нез в виде врожденных пороков развития органов или частей тела заро-
дыша.
К фетальному периоду основной органогенез заканчивается и происходят
дальнейший рост и дифференцировка тканей плода.
В раннем фетальном периоде еще продолжается органогенез полушарий
большого мозга, поэтому в этом периоде могут возникать пороки развития
головного мозга.
Кроме дизонтогенеза, у плода иногда встречаются и другие патологиче-
ские процессы, так как его реактивные возможности по сравнению с эмбрио-
ном возрастают. У плода наблюдаются альтеративные изменения, редуциро-
ванное воспаление (см. «Воспаление»), иммуноморфологические изменения
(см. «Иммунопатологические процессы», с. 143), расстройства крово- и лим-
фообращения, гиперплазия и регенерация. Поэтому в фетальном периоде на-
блюдаются болезни, сходные с болезнями внеутробного периода. Для болез-
ней плода —фетопатий — характерны следующие особенности.
1. Любая болезненная форма в плодном периоде сочетается с нарушением
онтогенеза, но на тканевом уровне. При этом могут быть или неправильные
соотношения тканей органов, или задержка их созревания. Например, при ше-
gaduodenum, megacolon имеется избыточное развитие мышечной ткани в стен-
ке кишки при отсутствии в ней достаточно развитых нервных приборов; на-
блюдается задержка созревания почек с обилием зародышевого типа
клубочков (рис. 372) и т. д.
2. При инфекционных фетопатиях всегда отмечается генерализованное по-
вреждение тканей и органов плода. Типично наличие множественных очагов
преимущественно альтеративного воспаления в паренхиматозных органах или
генерализованного гранулематоза (например, при врожденном сифилисе,
листериозе).
1 Фенокопия — порок развития, возникающий под влиянием экзогенных агентов, морфоло-
гически идентичный генотипическому пороку.
Пороки, гены которых локализованы в Х-хромосоме, в свою очередь могут наследоваться
по рецессивному или доминантному типу. Пороки, сцепленные с Х-хромосомой, передающиеся
по рецессивному типу, наблюдаются как правило у мальчиков, так как единственная у них X-
хромосома является пораженной. Мутантный ген передает мать, не являющаяся больной. Очень
редко носительницей порока может быть девочка. Это бывает в том случае, если отец являлся
больным, а мать — носительницей мутантного гена.
Кроме локального поражения генетического аппарата ядра гаметы вслед-
ствие мутации генов, в период гаметогенеза может появляться мутация хро-
мосом в виде изменений их числа и структуры. Мутации хромосом получили
название хромосомных аберраций. Хромосомные аберрации возни-
кают чаще всего в момент редукционного деления гамет. Их следствием
являются хромосомные болезни, которые, однако, в большинстве случаев не
наследуются, так как их носители чаще умирают в детстве или являются
бесплодными.
Типичными примерами хромосомных болезней являются болезнь Дауна (трисомия по 21-й
паре аутосом), синдром Патау (трисомия по 13—15-й паре аутосом), синдром Шерешевского-
Тернера (моносомия половой хромосомы — 45 ХО) и др.
Наиболее часто встречается болезнь Дауна, наблюдающаяся у новорожденных в соот-
ношении 1: 600, 1: 700. Клинически у детей с рождения отмечается выраженная задержка ум-
ственного и физического развития. Больные имеют типичный внешний вид — косой разрез глаз,
западающая спинка носа, высокое небо, низкое расположение маленьких ушных раковин, выра-
женная гипотония мышц. Дети редко доживают до возраста взрослого человека и погибают ча-
ще от интеркуррентных заболеваний. У большинства из них обнаруживаются пороки развития
сердца и магистральных сосудов (тетрада Фалло и др.), реже — пороки развития пищеваритель-
ной и мочеполовой систем. У этих детей отмечаются недоразвитие полушарий большого мозга,
особенно лобных его долей с задержкой дифференцировки нейронов, нарушения процессов мие-
линизации, архитектоники кровеносных сосудов мозга.
Синдром Патау у новорожденных и мертворожденных встречается
с частотой 1: 5149 рождений. Характерны выраженная общая гипоплазия,
аномалии черепа и лица — низкий скошенный лоб, узкие глазные щели, запав-
шее переносье, широкое основание носа, гипотелоризм, «дефекты скальпа»,
низко расположенные деформированные ушные раковины, типичны расще-
лины верхней губы и неба. Отмечается полидактилия и флексорное положение
кистей, микрофтальмия, колобома и помутнение роговицы. Со стороны го-
ловного мозга отмечается микроцефалия, аринэнцефалия (отсутствие обоня-
тельного мозга), аплазия или гипоплазия червя мозжечка и др. Отмечаются
также врожденные пороки сердца, органов пищеварения, мочевой системы
и др. Дети нежизнеспособны.
Бластопатии
Бластопатия — патология бластоцисты, возникающая в период нида-
ции и дробления в первые 15 дней от момента оплодотворения до выделения
эмбрио- и трофобласта.
Этиология и патогенез. Причиной бластопатии чаще всего являются хромо-
сомные аберрации в сочетании с влияниями среды (эндокринными заболева-
ниями матери, гипоксией и др). Патогенез зависит от вида поражения бласто-
цисты. Так, например, патогенез двойниковых уродств связан с появлением во
время дробления двух или более самостоятельно растущих центров. Пола-
гают, что если эти центры разобщены друг с другом, то развиваются два н е -
зависимо растущих однояйцевых близнеца, нормальное развитие ко-
торых не следует относить к бластопатиям. Если центры роста расположены
близко и имеют общую для двух близнецов промежуточную зону, то разви-
ваются два сросшихся близнеца. В обоих случаях возможно развитие
симметричных и асимметричных близнецов (рис. 373).
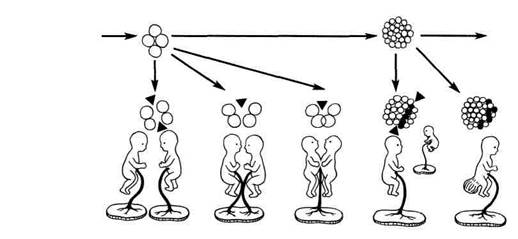
Рис. 373. Схематическое изображение возможных нарушений развития в период бласто-
генеза (по Гертлеру).
Морфология бластопатий разнообразна. К ним относятся нарушения им-
плантации бластоцисты, а именно: эктопическая беременность, поверхностная
или очень глубокая имплантация бластоцисты в эндометрий, нарушение
ориентации формирующегося эмбриобласта в бластоцисте по отношению
к эндометрию, аплазия или гибель развивающегося эмбриобласта с образова-
нием пустого зародышевого мешка, пороки развития всего эмбриона, неко-
торые одиночные пороки, двойниковые уродства и, наконец, аплазия или ги-
поплазия формирующегося трофобласта — амниона, амниотической ножки,
желточного мешка (В. П. Кулаженко). Поверхностная или чрезмерно
глубокая имплантация бластоцисты приводит к порокам разви-
тия формы, локализации, а также приращению плаценты (см. с. 541), которые
чреваты гибелью плода во время акта родов. Нарушения ориентации
эмбриобласта при полной топографической инверсии заканчиваются ги-
белью эмбриобласта. При неполной инверсии наблюдаются пороки развития
пуповины (см. с. 541), которые могут приводить кчгибели плода во время ро-
дов. Пустые зародышевые мешки представляют собой бластоцисты,
не содержащие эмбриобласт или содержащие его остатки. Иногда в них мож-
но обнаружить амниотические оболочки, пуповину, желточный мешок.
Патология развития всего эмбриона представляет собой об-
щие тяжелые нарушения, несовместимые с жизнью.
Одиночные и множественные пороки развития, возникаю-
щие в период бластулы (в первые 8—12 нед), встречаются в 14,3 — 22,9% всех
спонтанно абортированных зародышей. При этом в 46,2 % случаев они сопро-
вождаются аномалиями последа. Такое сочетание часто приводит к гибели
зародыша.
Двойниковые уродства встречаются в виде сросшейся двойни. Если срос-
шаяся двойня состоит из равных симметрично развитых компонентов, она на-
зывается диплопагусом (diplopagus от греч. diplos — двойной, pagus —
соединять); если же она состоит из асимметрично развитых
компонентов — гетеропагусом (heteropagus от греч. heteros — другой),
при этом недоразвитый близнец, находящийся в зависимости от другого, раз-
витого, получил название паразита. К асимметричным двойниковым срос-
шимся уродствам некоторые исследователи относят тератомы. Для обо-
значения локализации сращения близнецов к анатомическому названию места
сращения добавляют также слово пагус; например, сращение в области го-
ловы называют краниопагусом, в области груди — торакопагусом,
в области таза —ишиопагусом и др.
Двойниковые уродства сочетаются с нежизнеспособностью, в редких слу-
чаях описана значительная продолжительность жизни таких близнецов до зре-
лого возраста. В легких случаях сращений только мягких тканей возможна
хирургическая коррекция.
Эмбриопатии
Эмбриопатия — патология эмбрионального периода с 16-го дня бере-
менности до 75-го дня включительно, в течение которого заканчивается ос-
новной органогенез и формирование амниона и хориона. К основным видам
эмбриопатии относят врожденные пороки развития. Врожденным поро-
ком развития называют стойкое морфологическое изменение органа, ча-
сти тела или всего организма, выходящее за пределы вариаций нормального
строения определенного биологического вида, возникающее внутриутробно
в результате нарушений морфогенеза. Так как органогенез завершается в ос-
новном в эмбриональный период, большинство пороков развития появляется
именно на этом этапе внутриутробного существования. Однако, кроме вро-
жденных пороков с нарушениями основного морфогенеза органов или частей
тела, имеются врожденные пороки, при которых нарушения развития наблю-
даются на уровне тканевой дифференцировки. Они часто бывают системны-
ми, например пороки развития поперечнополосатой мускулатуры (врожден-
ная миатония Оппенгейма), соединительной ткани (болезнь Марфана), кожи
(врожденный ихтиоз), костей хрящевого генеза (врожденная хондродисплазия)
и др. Пороки развития могут касаться также тканей одного органа, например
гипоплазия гладкой мышечной ткани при megaureter, нервного интрамураль-
ного аппарата — при megacolon, легочной ткани — при кистозном легком и др.
По срокам возникновения эти пороки относятся к ранним фетопатиям. Ран-
ние фетопатии часто сочетаются с эмбриопатиями; например, врожденный
ихтиоз и хондродисплазия — с пороками развития лица, болезнь Марфана — с
пороками развития лица и аорты и др. Частота врожденных пороков, по
данным ВОЗ, составляет 1,3 % от общего числа рождений.
Любой врожденный порок может проявляться в виде: 1) отсутствия како-
го-либо органа или части тела (агенезия, аплазия); 2) недоразвития органа
(гипоплазия); 3) чрезмерного развития (гиперплазия) или наличия избыточно-
го числа органов (удвоение и др.); 4) изменения формы (слияние органов,
атрезия, стеноз отверстий, каналов, дизрафия — незаращение эмбриональных
щелей, экстрофия — выворот и др.; 5) изменения в расположении органов (эк-
топия); 6) персистирование эмбриональных провизорных (предсуществовав-
ших) органов.
Классификация. Врожденные пороки развития разделяют по степени рас-
пространенности в организме, по локализации в том или ином органе, по
этиологии. По распространенности врожденные пороки могут быть:
1) изолированными — с поражением одного органа; 2) системными — с пора-
жением нескольких органов одной из систем; 3) множественными — с пораже-
нием органов разных систем. По локализации различают пороки развития
центральной нервной, сердечно-сосудистой, пищеварительной, мочеполовой
и других систем. Врожденные пороки развития названной локализации имеют
наибольшее значение в патологии. Чаще всего встречаются пороки развития
центральной нервной и сердечно-сосудистой систем, так как именно эти си-
стемы имеют наибольший тератогенный терминационный период (см. рис. 371).
Изолированные пороки развития встречаются чаще множественных, несмотря
на то что тератогенный терминационный период для многих органов во вре-
мени совпадает.
Наиболее совершенной является классификация пороков развития п о
Этиологии, однако уровень современных знаний пока не позволяет ее при-
держиваться. Известны лишь отдельные виды системных и множественных
врожденных пороков, связанных с определенной этиологией, например рубео-
лярная эмбриопатия, алкогольная, талидомидная эмбриопатия и др., а также
наследственно обусловленные генотипические врожденные пороки и вро-
жденные пороки вследствие хромосомных аберраций; последние, как правило,
носят характер множественных..>;
Разграничение генотипических врожденных пороков от их фенокопий возможно с помощью
генеалогического метода изучения родословной, цитогенетического метода,
позволяющего изучить кариотип тканей носителя порока при их культивировании, с помощью
близнецового метода, основанного на частоте выявления врожденных пороков у однояй-
цевых близнецов и метода дерматоглифики — изучения комплекса кожных узоров, рас-
положенных на ладонях, подошвах и сгибательной поверхности пальцев, который используется
для срочной диагностики хромосомных болезней.
Дата добавления: 2015-11-26 | Просмотры: 1403 | Нарушение авторских прав
|