 |
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
В РЕЗУЛЬТАТЕ ТРАВМЫ
операции, изготовлении фиксирующих аппаратов, если оно вхо- дит в план лечения, определении последующей тактики лечения больного. Продолжительность предоперационного периода обычно 1—2 нед. Эти мероприятия можно проводить и в амбулаторных условиях, до госпитализации больного. Основной задачей врача- ортопеда является изготовление фиксирующего аппарата, так как при костной пластике нижней челюсти необходимо обеспечить жесткую фиксацию фрагментов для создания нормальных усло- вий трансплантату. Оперативные способы фиксации фрагментов могут решить эту задачу, но их следует применять лишь тогда, когда возможности консервативного закрепления исчерпаны (недостаточное количе- ство зубов или полное их отсутствие, обширные дефекты за зуб- ным рядом). При достаточном количестве зубов на фрагментах челюсти фиксацию можно обеспечить при помощи внутри-вне- ротовых межчелюстных аппаратов жесткой несъемной конструк- ции. Из съемных аппаратов пригодна для этих целей лишь шина Ванкевич, которая может быть использована при обширных де- фектах и отсутствии зубов. Типичным примером несъемных фик- сирующих конструкций является аппарат, состоящий из ряда металлических коронок, укрепленных на зубах нижней челюсти и на их антагонистах. К щечной поверхности коронок припаяны четырехгранные втулки, в которые устанавливают П-образную скобку в сомкнутом состоянии челюсти. Этот аппарат был пред- ложен А. И. Бетельманом, модифицирован И. М. Оксманом. Изго- товление подобных аппаратов и фиксацию на зубах проводят за 2—4 дня до операции, а закрепление фрагментов с помощью П-образной скобки осуществляется после пересадки трансплан- тата в конце операции. Фиксирующими аппаратами пользуются до полного приживления трансплантата. Сроки их снятия совпа- дают со сроками начала протезирования. Послеоперационные ортопедические мероприятия. Послеопера - ционные ортопедические мероприятия включают в себя наблю- дение за состоянием фиксирующих аппаратов, снятие их, изго- товление зубных протезов в соответствующие сроки и динами- ческое наблюдение за больными совместно с хирургом-стомато- логом. Сроки начала протезирования после костной пластики ниж- ней челюсти зависят от вида опухоли, объема и вида хирурги- ческого вмешательства. Если при удалении доброкачественной опухоли одномоментно производится костная пластика, то про- тезирование проводят в интервале от 2 до 4 мес в зависимости от приживления трансплантата. При удалении злокачественной опухоли в день операции пер- вичная остеопластика производится редко, поэтому показано не- посредственное протезирование. Сроки начала костной пластики могут быть различными. Они определяются специалистами по он- костоматологии. Если через определенный промежуток времени
проведена костная пластика, то протезирование следует начать не ранее чем через 6 мес. При этом необходимым условием яв- ляется отсутствие воспалительных явлений в области костного трансплантата. Наличие свищей, отека служит противопоказани- ем к протезированию. Каковы основные задачи протезирования после костной пла- стики нижней челюсти? Во-первых, создание благоприятных условий для окончательного приживления и функциональной пе- рестройки трансплантата, защита его от влияния стягивающих рубцов и деформации. Во-вторых, формирование полноценного протезного ложа для последующего протезирования. В-третьих, восстановление функции жевания, речи, внешнего вида и умень- шение патологических проявлений, обусловленных стрессовым воздействием. Все эти задачи решаются в процессе пользования полноценными протезами. Клинико-лабораторные этапы протезирования после костной пластики осуществляются в соответствии с общими принципа- ми ортопедического лечения больных с дефектами и деформа- циями зубочелюстной системы. Однако имеются и свои особен- ности. К ним следует отнести: 1) необходимость частой замены протезов, особенно в первое время после костной пластики, поскольку форма протезного ложа изменяется в связи с интен- сивной перестройкой костного трансплантата и перестает соот- ветствовать форме базиса протеза; 2) сложности фиксации про- теза и рационального распределения нагрузок на опорные зубы и ткани протезного ложа, особенно при малом количестве зубов и Рубцовых изменениях вокруг трансплантата; 3) трудности ана- томической постановки искусственных зубов в протезах вследствие отсутствия места в межальвеолярном промежутке, которое свя- зано со смещением трансплантата или фрагментов нижней че- люсти. Достижение оптимальной эффективности протезирования после костной пластики возможно лишь при учете указанных особенностей. Например, своевременная тактика, коррекция или полная замена протезов может быть успешно выполнена при динамическом наблюдении за больными со сроками осмотров в первое время после операции через 1—-3—6—12 мес. В последую- щем периодичность осмотров может быть 2 раза в год. Показанием к замене протеза новым является резкое несоот- ветствие базиса протезному ложу. Оно проявляется плохой устой- чивостью протеза, попаданием пищевых комков под базис и перегрузкой опорных зубов или воспалительными изменениями слизистой оболочки протезного ложа. При незначительных несо- ответствиях можно добиться успеха путем перебазировки и кор- рекции окклюзионных взаимоотношений. Все эти меры прово- дятся с учетом описанной выше первой особенности протезиро- вания. Учитывая вторую особенность (трудность фиксации) проте- 53В зирования, после костной пластики следует по возможности шире применять цельнолитые бюгельные протезы с шинирующими многозвеньевыми кламмерами. Их количество и расположение на зубах, способ соединения с базисом должны быть подчинены двум основным требованиям: обеспечению максимальной устой- чивости протеза во время функции и распределению нагрузок адекватно состоянию опорных тканей и в том числе и трасплан- тата. При малом количестве зубов или полном их отсутствии для обеспечения фиксации протеза нужно использовать ретенцион- ные возможности протезного ложа или создавать их оперативным способом (углубление преддверия полости рта, иссечение руб- цовьгх тканей и т. д.). Третья особенность — трудности конструирования протезов вследствие недостатка места для зубов и базиса — требует при- менения методов, описанных при ортопедическом лечении не- правильно сросшихся переломов. Создания места и условий для полноценного протезирования можно добиться дополнительным хирургическим вмешательством. Однако это нежелательно, поскольку многократные операции тяжело переносятся больными. Поэтому вполне допустимо кон- струирование протезов с определенными отклонениями от об- щепринятой анатомической формы искусственных зубов, их по- ложения в базисе. А сами базисы с целью упрочнения их могут быть литыми.
Дефекты лица Причиной дефектов лица являются в основном огнестрель- ные ранения, ожоги, оперативные вмешательства по поводу новообразований, специфические инфекционные заболевания (нома, сифилис). Дефекты лица бывают изолированными, напри- мер носа, уха, и сочетанными — с разрушением нескольких ана- томических областей лица и челюстей. Это особая категория боль- ных. Обезображивание лица причиняет им тяжелые психические страдания. Основным методом лечения является хирургическое восста- новление лица. Ортопедические методы при этом используются как вспомогательные. Лишь в отдельных случаях, когда имеются противопоказания к оперативным вмешательствам, протезирова- ние является единственным способом устранения дефектов лица. Ортопедические мероприятия при восстановительных операци- ях носа. Пластические операции при неполных или полных де- фектах носа всегда заканчивают наложением формирующей по- вязки. В носовые ходы вводят резиновые трубки, обернутые йодо- формной марлей, а на боковые скаты носа с обеих сторон укла- дывают плотные валики из марли. Все это закрепляют полос- 19-3384 529 ками лейкопластыря (см. учебник по хирургической стомато- логии). Эту задачу более рационально можно решить с помощью ортопедических аппаратов, которые представляют собой индиви- дуально изготовленные приспособления для формирования по- лости носа и воздухоносных путей, а также наружных контуров носа. Примером такого формирующего аппарата является конст- рукция, предложенная 3. Я. Шуром. Она состоит из паяной ко- ронковой шины, укрепленной на верхних зубах, съемной дуги с внеротовыми стержнями и формирующего приспособления. По- следнее включает в себя каркас в виде полой пластмассовой пи- рамиды, открытой к дефекту, и пелот, который состоит из двух половин, соединенных с помощью проволоки. Каркас служит для формирования внутренней поверхности носа, а пелоты — его наружных контуров. Протез носа. В редких случаях, когда отсутствуют возможнос- ти хирургического восстановления носа, или на этапе ожидания операции применяют метод протезирования, который включает моделирование, выбор материала, создание фиксирующих при- способлений, лабораторное изготовление, припасовку протеза по отношению к тканям, ограничивающим дефект носа. Моделирование искусственного носа проводится на маске лица из глины или воска. Для изготовления точной маски (моде- ли) лица слепок следует снимать эластической массой, укрепив его снаружи гипсом непосредственно на лице больного. При этом надо пользоваться имеющимися фотографиями лица больного до повреждения. Конфигурацию профиля наружного носа можно построить на боковой телерентгенограмме головы, используя ма- тематические методы (М. 3. Миргазизов). В качестве конструкционного материала используются элас- тические и твердые пластмассы. Последние имеют определенные преимущества: они пропускают свет, легко принимают желаемые форму и цвет. Для укрепления протеза носа учитывают ретенци- онные свойства самого дефекта и механические приспособления: очковая оправа, пружины и соединительные устройства. Внутренняя поверхность протеза содержит продольные и по- перечные эластичные отростки в соответствии с ретенционны- ми углублениями и нишами, имеющимися или созданными хи- рургическим способом в области дефекта. У корня искусственно- го носа монтируется фиксирующее устройство для соединения с очковой оправой. Если дефект носа сочетается с дефектом верхней челюсти и неба, искусственный нос укрепляют к челюстному протезу. При таком способе фиксации происходит взаимное укрепление про- тезов, что значительно улучшает их стабильность во время фун- кции. При припасовке протеза особое внимание должно быть уде- лено границам прилегания его к поверхности лица. Нужно доби-
ваться плотного, малозаметного перехода границ протеза на кожу лица и их стабильности при сокращении мимической мускула- туры. Протез ушной раковины. Врожденные и приобретенные дефек- ты уха устраняются, как правило, хирургическим способом. Существует возможность протезирования ушной раковины. Искусственное ухо изготавливают из эластической пластмассы. Моделируют его по форме противоположной ушной раковины. Укрепляют при помощи пружин и используют ретенционные свойства наружного слухового прохода. Если эти способы укреп- ления окажутся недостаточными, то создают защепки из микро- стебля в области сосцевидного отростка. Протезирование дефектов орбиты. Пр и разрушениях или хирур- гическом удалении глазного яблока его заменяют искусственным глазом. Глазное протезирование осуществляется в рамках офталь- мологической помощи. Необходимость участия врачей стомато- логов-ортопедов возникает при сочетанных повреждениях верх- ней челюсти и области орбиты. При дефектах орбиты глазной протез соединяют с протезом орбиты. Для дополнительного укрепления протезов используют очковую оправу. При сочетанных дефектах конструкция протеза может быть довольно сложной, поскольку она рассчитана на одновременное замещение утраченных зубов, альвеолярного отростка, тела че- люсти, неба, орбиты и глаза. Соответственно этому в протезе можно выделить зубную, челюстную, лицевую и глазную части. Такой сложный, многофункциональный протез бывает раз- борным. Глазная часть протеза соединяется с челюстно-лицевой частью с помощью шарниров.
19* Глава 10 ОРТОПЕДИЧЕСКОЕ ЛЕЧЕНИЕ АДЕНТИИ С ИСПОЛЬЗОВАНИЕМ ИМПЛАНТАТОВ Стоматологическая имплантология — относительно новый раз- дел стоматологической науки и практики. Использование клас- сических методов протезирования съемными или несъемными конструкциями иногда невозможно. Много трудностей возника- ет при протезировании больных с полной вторичной адентией, особенно если она осложнена значительной атрофией альвеоляр- ных отростков. Поэтому многие годы во всем мире и в нашей стране предпринимаются попытки создать полноценную замену утраченным зубам. В России первое сообщение об имплантации зубов было сде- лано в 1891 г. Н.Н.Знаменским на IV Пироговском съезде врачей в Москве, где он доложил о приживлении искусственных зубов из фарфора и металла. Однако это было единичное сообщение, и в широкую практику стоматологии этот метод не вошел. Рабо- ты продолжались, но до открытия в начале 60-х годов проф. Бре- немарком принципа остеоинтеграции (оссеоинтеграции) говорить о широком внедрении в повседневную стоматологическую прак- тику имплантологии было преждевременно. Новые подходы позволили в 70—80-х годах значительно обо- гатить теорию и практику стоматологической имплантологии, определить ее роль и место в клинике ортопедической стомато- логии. Этому способствовали работы по созданию новых матери- алов, изучению их биологической совместимости, исследованию реакций костной ткани и слизистой оболочки на введение им- плантата; усовершенствование оперативной техники и инструмен- тария; разработка новых конструкций имплантатов и зубных про- тезов; изучение биомеханических закономерностей распределения напряжений в костях; уточнение показаний и противопоказаний к протезированию с использованием имплантатов; создание объективных критериев оценки результатов лечения.
ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ИМПЛАНТОЛОГИИ Фундаментом имплантологии являются современные представ- ления о реакции организма на введение имплантатов, понима- ние процессов регенерации. Замещение тканей и инкапсуляция инородных материалов, получившие название процессов организации, являются частными случаями регенеративных процессов. Конечным исходом процес- сов организации являются рассасывание и замещение инородного субстрата соединительной тканью либо отделение его посредством фиброзной капсулы от окружающих тканей, а также образова- ние спаек вплоть до зарастания серозных полостей. В отношении инородного тела процесс организации выражается в развитии вокруг него грануляционной ткани, инкапсуляции (образование капсулы вокруг инородного тела). В непосредственной близости от инородных тел из элементов грануляционной ткани иногда образуются гигантские клетки в виде крупных протоплазматичес- ких тел с многочисленными ядрами. Они облегают инородные тела, а в отдельных случаях захватывают и фагоцитируют их. Эти клетки принято называть гигантскими клетками инородных тел. Приведенные закономерности характерны для случаев, когда инородное тело случайно оказалось в организме, полностью на- ходится внутри тканей и не сообщается с внешней средой. Имплантат, установленный по определенным правилам, не может рассматриваться как случайное инородное тело, и харак- тер его взаимоотношений в системе имплантат — кость в зави- симости от свойств и структуры материала гистологически мо- жет определяться тремя видами реакций (табл. 20).
Т а б л и ц а 20. Реакция тканей на имплантат
Контактный остеогенез был назван Бренемарком оссеоинтег- рацией (остеоинтеграцией). Дистантный остеогенез получил на- звание фиброинтеграции. Интегративные процессы связаны с репаративным остеоге- незом. Схематически репаративный остеогенез при приживлении
дентальных имплантатов может быть представлен следующим образом:
• травма и повреждение целостности слизистой оболочки, надкостницы, кортикальной и губчатой кости при форми- ровании костного ложа под имплантат; • выделение двух зон в костной ткани: — зона репаративного остеогенеза, — зона ремоделирования костной ткани (зона, где вмеша- тельство не проводилось); • кровотечение из зоны вмешательства, высвобождение сы- вороточных и клеточных медиаторов воспаления и других продуктов секреции макрофагов; • образование фибробластами экстрацеллюлярного протеино- вого матрикса (коллаген, гликопротеин, эластин, протео- гликан, гликозаминогликан); • образование фосфатной пленки на оксидном слое имплан- тата из титана и его сплавов (возможны процессы эпитак- сии гидроксилапатита); • адгезия протеогликанов, остеобластов на поверхности им- плантата и его элементов; клеточная активность остеоблас- тов; • окончательное формирование экстрацеллюлярного матрик- са с образованием его неорганических компонентов в кост- ной ране, а также на поверхности и внутренних структурах имплантата; • образование костного регенерата, тесно связанного со струк- турой имплантата; • минерализация костного регенерата и окончательное фор- мирование костной ткани, непосредственно связанной с им- плантатом (остеоинтеграция имплантата); • ремоделирование костной ткани (в первой зоне с участием любых имплантатов, во второй зоне с участием только ме- ханически активных имплантатов).
Из всех видов реакций костной ткани лишь остеоинте- грация обеспечивает стабильность имплантата, достаточную для его применения в качестве опоры для ортопедических конструк- ций. При всей сложности структурных связей окружающих тканей с имплантатом (инородным телом) эта связующая система ос- тается лишь биотехнической имитацией натурального соедине- ния тканей пародонта с естественным зубом. До настоящего времени не удалось решить главную проблему стоматологической имплантации — создать систему, воспроиз- водящую действие периодонтальных связок, выполняющих одну из важнейших функций во время акта жевания — амортизаци- онную (табл. 21). Таблица 21. Сравнительные данные о морфологии и функции пародонта и его модели имнлантат — кость — десна
Сравни- ваемые признаки
Пародонт Модель пародонта (имплантат с окружаю- щими тканями)
Общая характери-
Строение лунки
Характер связи корня с костью альвеолы
Структура зубодесне- вого соедине- ния Морфологическая и функцио- нальная общность комплекса тканей: периодонта, кости, альвеолы, десны с надкостни- цей и тканей зуба
Лунка образуется в процессе формирования корня зуба. Внутренняя поверхность стенок альвеол состоит из компактной кости. Здесь находятся много- численные отверстия, особен- но вблизи дна, через которые проходят кровеносные сосуды и нервы Волокна периодонта с одной стороны переходят в цемент корня, с другой — в альвеоляр- ную кость, образуя связочный аппарат, состоящий из боль- шого числа коллагеновых воло- кон, собранных в пучки, меж- ду которыми располагаются сосуды, нервы. Основной фун- кцией волокон периодонта яв- ляется поглощение механичес- кой энергии, возникающей при жевании, равномерное распределение ее на костную ткань альвеолы, нервно-рецеп- торный аппарат и микроцирку- ляторное русло периодонта В норме имеется зубодесневое соединение, структуру которо- го объясняют по-разному. Пер- вый вариант объяснения: по- верхностные клетки соедини- тельного эпителия имеют геми- десмосомы и связаны с крис- Искусственно созданная биотехническая система, состоящая из биоинертно- го или биоактивного ма- териала, структурно и функционально вступаю- щая в связь с костной тканью, надкостницей и слизистой оболочкой (биотехническая система имплантат — кость — дес- на) В большинстве случаев со- здается хирургическим путем. Внутренние стенки костного ложа состоят из губчатого вещества, резко отличающегося по меха- ническим свойствам от компактной кости
Соединительная ткань проникает в поверхност- ный слой имплантата; ко- стная ткань и имплантат образуют соединение по типу анкилоза на неболь- шом расстоянии от повер- хности имплантата; кост- ная ткань и имплантат об- разуют анкилоз за счет прорастания тканей в тол- щу имплантата
Существует мнение о воз- можности образования эпителиального прикреп- ления в пришеечной об- ласти имплантата. Геми- десмосомы обнаружены в пограничной зоне им-
Продолжение
Сравни- ваемые признаки Пародонт Модель пародонта (имплантат с окружаю- щими тканями)
Функции пародонта Барьерная
Трофиче- ская таллами апатита поверхности зуба через тонкий зернистый слой органического материала. Второй вариант: между эпите- лием и поверхностью зуба су- ществует физико-химическая связь. Адгезия эпителиальных клеток к поверхности зуба осу- ществляется за счет макромоле- кул десневой жидкости
Барьерная функция заключает- ся в обеспечении надежной за- щиты и устойчивости к инфек- циям и интоксикациям. Она определяется: 1) способностью эпителия десны к ороговению; 2) большим количеством и особенностями направления пучков коллагеновых волокон; 3) тургором десны; 4) состоя- нием мукополисахаридов со- единительнотканных образова- ний пародонта; 5) особеннос- тями строения и функции фи- зиологического зубодесневого кармана; 6) антибактериальной функцией слюны в связи с на- личием в ней биологически активных веществ (лизоцим, ингибин); 7) наличием лабро- цитов и плазматических кле- ток, играющих важную роль в выработке аутоантител Трофическая функция паро- донта состоит в обеспечении нормального питания и обме- на веществ в тканях за счет нейрогуморальных механизмов, где капилляр с участком кон- тактирующей с ним ткани рас- плантат — десна при при- менении зубных имплан- татов из виталиума, тита- на, карбона, эпоксидной смолы, сапфира. Есть дан- ные о том, что эта тонкая структура формируется в течение 48 ч после им- плантации (Swope, James). Закономерности форми- рования эпителиального прикрепления и его на- дежность как биологичес- кого барьера нуждаются в дальнейшем изучении
Барьерная функция тка- ней, окружающих имп- лантат и вступающих с ним во взаимодействие, существует, поскольку способность эпителия дес- ны к ороговению сохра- няется, тургор десны име- ется, мукополисахариды соединительнотканных образований в зоне около имплантата выявляются, эпителиальное прикреп- ление существует, анти- бактериальная функция слюны не нарушается, лаброциты и плазматичес- кие клетки встречаются
Трофическая функция тканей, связанных с им- плантатом, резко отлича- ется от трофической фун- кции пародонта. Она обес- печивается системой кро- воснабжения и иннерва-
Продолжени е
Сравни- ваемые признаки
Рефлек- торная регуляция жеватель- ного давления
Пласти- ческая
Аморти- зирующая Пародонт
сматривается как структурная и функциональная единица тро- фики тканей Осуществляется за счет много- численных нервных оконча- ний, имеющихся в пародонте. Раздражение рецепторов пере- дается по разнообразным реф- лекторным магистралям
Пластическая функция паро- донта заключается в постоян- ном воссоздании его тканей, утраченных в ходе физиологи- ческих или патологических про- цессов. Выполняют эту функцию цементо- и остеобласты. Опре- деленную роль играют и другие клеточные элементы: фибро- бласты, лаброциты, а также со- стояние транскапиллярного об- мена Амортизирующая функция па- родонта состоит в ослаблении и смягчении жевательного дав- ления и защите от травмы тка- ней зубной альвеолы, сосудов и нервов периодонта. Она обес- печивается за счет физико-ме- ханических свойств волокон териодонта, жидкого содержи- мого и коллагенов межткане- вых щелей и клеток, а также изменения объема сосудов Модель пародонта (имплантат с окружаю- щими тканями)
ции костной ткани и дес- ны
Следует полагать, что реф- лекторная регуляция жева- тельного давления тканя- ми, окружающими им- плантат, существует, но снижена, поскольку отсут- ствует периодонт с его ре- цепторным аппаратом. Од- нако предполагается, что нервные сплетения, нахо- дящиеся в костной ткани, могут участвовать в выпол- нении этой функции Пластическая функция тканей, окружающих им- плантат, сохранена. Остео- бласты обнаруживаются в костной ткани, прилегаю- щей к имплантату
Амортизирующая функ- ция тканей, окружающих имплантат, практически отсутствует, ее можно со- здать лишь искусственно путем введения в конст- рукцию имплантата амор- тизаторов. Некоторую амортизирующую функ- цию приписывают соеди- нительнотканной капсуле, окружающей имплантат, но роль ее в этом процес- се ничтожна
Примечание. Данные, касающиеся морфологии и функции пародонта, приведены по В.С.Иванову (1981).
КЛИНИЧЕСКИЕ ОСНОВЫ ИМПЛАНТОЛОГИИ
Противопоказания и показания При осмотре пациента следует обратить особое внимание на признаки заболеваний, признанных имплантологами абсолютны- ми (общими и местными) или временными противопоказания- ми к имплантации. К общим противопоказаниям относят:
• любые основания для отказа от хирургического вмешатель- ства; • любые противопоказания к местной анестезии; • заболевания, на которые может отрицательно повлиять им- плантация (например, эндокардит, искусственный сердеч- ный клапан или водитель ритма, трансплантация органов, ревматические заболевания и др.); • формы терапии, которые могут отрицательно повлиять на заживление и сохранение имплантата, а также на его ложе (например, иммуноподавляющие средства, антидепрессан- ты, противосвертывающие средства, цитостатики); • психические заболевания; • ситуации, связанные с тяжелым психологическим или фи- зическим стрессом; • недостаточное желание пациента, а также кахексия, старческий возраст, недостаточная привычка к общей гигиене. Возраст не является абсолютным противопоказанием, исклю- чающим дентальную имплантацию. Выделяют также местные противопоказания: • недостаточная склонность к гигиене полости рта; • ограничение мануальных способностей, в частности двига- тельной активности; • болевой синдром в челюстно-лицевой области неясного ге- неза; • не поддающиеся коррекции дисфункции височно-нижнече- люстного сустава, которые могут обусловить избыточную на- грузку на имплантат; • не поддающийся лечению генерализованный маргинальный гингивит; • дольчатые фибромы, фибромы протезного края; • недостаточное наличие костной ткани, неподходящая струк- тура костной ткани, потеря более чем трети массы альвео- лярной ткани (для непосредственной имплантации); • неблагоприятное расстояние до nervus alveolaris inferior, до верхнечелюстной и носовой пазух. Противопоказания временного характера: • острые заболевания; • стадии реабилитации и выздоровления; • беременность; • наркотическая зависимость; • состояние после облучения (в течение минимум года). Ретенированные зубы, кисты, опухоли костных тканей и вос- палительные процессы в области челюстных костей также явля- ются противопоказаниями к имплантации. Определить общее состояние организма больного и возмож- ную реакцию на имплантат можно с помощью обследования, а также анкетирования пациента. Если этих данных окажется не- достаточно, следует направить больного на консультацию к со- ответствующим специалистам. Несомненно, большую помощь окажет заключение участкового терапевта или семейного врача о состоянии здоровья больного. Особое значение при планировании стоматологической им- плантации приобрели в настоящее время правовые вопросы. Пе- ред началом вмешательства (лечения) необходимо заключение и подписание договора, предусматривающего возможные послед- ствия и действия сторон. Пациент должен быть детально озна- комлен с планом лечения, прогнозом, возможными осложнени- ями, предупрежден о вероятности отторжения имплантатов. Кроме того, пациенту должна быть предоставлена объективная инфор- мация о возможных альтернативных методах лечения. Следует обсудить с больным ожидаемый результат лечения. При плани- ровании стоматологической имплантации и для прогнозирования ее результатов рекомендуется выяснять функциональные качества ранее изготовленных протезов. Современный уровень стоматологической имплантологии ог- раничен, к сожалению, узким кругом показаний к проведению ортопедического лечения с использованием имплантатов. Основной предпосылкой применения зубных протезов с опо- рой на имплантаты является невозможность использования тра- диционных методов протезирования. Это может быть связано как с объективными факторами (условия для традиционного проте- зирования), так и субъективными (категорический отказ паци- ента от съемных конструкций). В связи с этим желание многих больных иметь несъемные зубные протезы вместо съемных или улучшить фиксацию съемных протезов за счет имплантатов очень часто не совпадает с возможностями метода. Показаниями к клиническому применению стоматологических (дентальных) имплантатов являются: 1) беззубые челюсти (особенно нижняя) с высокой степенью атрофии альвеолярной части; 2) одиночный дефект зубного ряда при интактных соседних зубах; 3) наличие дистально не ограниченного дефекта (I и II клас- сов по Кеннеди); 4) наличие большого по протяженности дистально ограни- ченного дефекта (III класс по Кеннеди); 5) наличие большого по протяженности дефекта во фронталь- ном отделе (IV класс по Кеннеди). Следует отметить, что во всех случаях, кроме 1-го, примене- ние имплантатов чаще всего может быть связано с психоэмоци- ональным настроем больных, когда они категорически отказы- ваются от съемных конструкций. Надо помнить, что применение имплантатов типа Бренемарка, кроме 2-го случая, все равно требует изготовления перед операцией временных съемных кон- струкций, которые закрывают дефект зубного ряда над местом имплантации. Известны случаи, когда пациенты соглашаются оставить хорошо изготовленный съемный протез и отказываются от имплантации. Однако отказ больного от съемного протеза, желание его иметь несъемную конструкцию с использованием имплантатов не следует рассматривать как некий каприз или прихоть. В каждом случае врачу необходимо глубоко проанализи- ровать мотивации пациентов, выяснить причины отказа от съем- ных конструкций и тщательно оценить возможность использова- ния имплантатов. Больные, у которых по разным причинам не удалось добиться удовлетворительных результатов традиционного протезирования, нередко испытывают чувство разочарования и безысходности. В этих случаях использование имплантации (в отсутствие противопока- заний) может явиться единственным способом, позволяющим выйти из сложившейся ситуации. С этим обстоятельством связаны огромный интерес к имплантации определенной части больных и глубокое разочарование, когда из-за общих или местных противо- показаний использование имплантатов невозможно. Разъяснение противопоказаний к имплантации таким боль- ным необходимо проводить очень продуманно, со строгим со- блюдением деонтологических принципов. Обязательно следует подчеркнуть, что с развитием имплантологии противопоказания будут сужаться и съемные конструкции следует рассматривать как этап, имеющий важное лечебно-профилактическое значение. Теоретически любой беззубый участок челюсти может быть восстановлен при помощи дентального имплантата. Для успешной установки имплантатов необходимо учитывать следующие основные требования. 1. Ширина костной ткани в щечно-язычном отделе не менее 6 мм. 2. Расстояние между корнями соседних зубов не менее 8 мм. 3. Толщина кости над нижнечелюстным каналом и ниже гай- моровой пазухи 10 мм (или необходима специальная опе- ративная подготовка).
4. Для изготовления супраконструкции с опорой на имплан- таты расстояние между зубными дугами 5 мм. Минимальная толщина кортикальной пластинки и низкая плотность губчатой кости костного ложа ставят под сомнение успех остеоинтеграции имплантата. Объем и структуру костного ложа определяют при рентгено- логическом исследовании (панорамная, аксиальная, прицельная рентгенограммы). Окончательное решение о проведении стоматологической имплантации зависит от согласия всех участвующих сторон: де- тальный осмотр больного рекомендуется проводить вместе с хи- рургом-имплантологом для выбора места и количества имплан- татов; при выборе ортопедической конструкции желательно уча- стие зубного техника.
ОСОБЕННОСТИ ОБСЛЕДОВАНИЯ БОЛЬНЫХ Проводя обследование больных по традиционной схеме (жа- лобы, анамнез, осмотр, пальпация, перкуссия и лабораторно- инструментальные исследования), необходимо обратить внима- ние на следующие особенности. Опрос больных следует сочетать с анкетированием, которое позволит получить ответы на вопро- сы, имеющие первостепенное значение для определения общих показаний и противопоказаний к имплантации. Вначале проводят тщательное клиническое и рентгенологи- ческое обследование больных. Осуществляют строгий отбор боль- ных в соответствии с принятыми показаниями бригадой специ- алистов (стоматолог-хирург, ортопед, рентгенолог и др.). Среди инструментально-лабораторных исследований зубоче- люстной системы обязательными являются обзорная рентгеногра- фия, ортопантомография или телерентгенография лицевого че- репа. Снимки должны быть получены в стандартных условиях и пригодны для проведения измерений с целью определения вер- тикальных размеров от альвеолярного гребня до носовой полос- ти и верхнечелюстных пазух на верхней челюсти и до нижнече- люстного канала — на нижней. Перед началом рентгенологического исследования нужно из- готовить специальные пластмассовые каппы или пластинки. Внутрь помещают металлические шарики диаметром 5—7 мм (рис. 273) таким образом, чтобы эти шарики не давили на слизистую обо- лочку полости рта. Количество шариков и их место примерно соответствуют числу будущих имплантатов. Каппы вводят в рот, после чего делают рентгеновский снимок, на котором по расстоянию между рент- геноконтрастными шариками и костью четко определяется тол- щина слизистой оболочки, костной ткани до гайморовых и но- совых пазух, расстояние до нижнечелюстного канала и т.д.
Рис. 273. Пластмассовая пластинка, изготовленная методом вакуумной компрессии, с закрепленными в ней металлическими шариками (диа- метром 5 мм) для рентгенографического исследования костной ткани в области предполагаемой имплантации.
Рис. 274. Схематическое изображение ортопантомограммы с проекцией металлических шариков.
(рис. 274). В дальнейшем необходимо изготовить шаблоны буду- щих протезов, которые позволят точно определить количество и место расположения имплантатов, смоделировать окклюзионные контакты. С помощью этих шаблонов выбирают ортопедическую конструкцию и определяют количество опор. Для точного опре- деления толщины альвеолярного отростка в месте предполагае -
Рис. 275. Зондовый толщиномер.
мой имплантации необходимо использовать специальный тол- щиномер (рис. 275, 276). Для выбора количества опор- ных элементов при конструиро- вании мостовидных протезов с опорами на имплантаты жела- тельно использовать одонтопа- родонтограмму по В.Ю.Кур- ляндскому. Условно можно счи- тать, что коэффициент одного зуба со здоровым пародонтом приблизительно равен двум хороию прижившимся внутри- костным цилиндрическим им- плантатам.
МАТЕРИАЛЫ, ПРИМЕНЯЕМЫЕ В ИМПЛАНТОЛОГИИ В стоматологической имплантологии применяют большое ко- личество материалов. Различают биотолерантные, биосовмести- мые, биоинертные и биоактивные материалы. К биотолерантным относят сплавы благородных металлов, сплавы кобальта, хрома и молибдена; к биоинертным и биосовместимым — титан и его сплавы, А1О3, углерод, цирконий; к биоактивным — стеклокера- мику с биоактивной поверхностью, СаРО4-керамику, гидрокси- апатит. Имплантационные материалы должны отвечать определенным требованиям: • не коррозировать, не вызывать воспалительных процессов в окружающих тканях; • не вызывать аллергических реакций; • не являться канцерогенными; • не изменять физических свойств в организме; • обладать достаточной механической прочностью; • легко поддаваться обработке; • хорошо стерилизоваться; • быть дешевыми. Наиболее соответствуют этим требованиям титан и керами- ческие материалы. Особенно широкое распространение получи- ли имплантаты из титана и его сплавов, из керамических мате- риалов, титановые с керамическим покрытием или с покрыти- ем из гидроксиапатита. М.З.Миргазизов на основании анализа биомеханических свойств различных имплантационных материалов предложил си- стематизировать имплантационные материалы и конструкции с позиции их биомеханической совместимости, условно выделив три ее уровня: низкий, средний и высокий. Общая классифика- ционная схема выглядит следующим образом: 1) материалы и конструкции с низким уровнем биомехани- ческой совместимости (НБС-материалы); 2) материалы и конструкции со средним уровнем биосовме- стимости (СБС-материалы); 3) материалы и конструкции с высоким уровнем биомеха- нической совместимости (ВБС-материалы). Низкий уровень биомеханической совместимости характеризу- ется полным несоответствием между физико-механическими свой- ствами, механическим поведением материала и биологических тканей, взаимодействующих с конструкцией, изготовленной из этого материала. Более того, интеграционные процессы, проис- ходящие при взаимодействии материала с тканями организма, не повышают уровень биомеханической совместимости. Свойства материала и тканей организма подчиняются разным законам. Средний уровень биомеханической совместимости характеризу- ется такими же признаками, как и низкий уровень, но имеется принципиальное различие: материал способен повышать уровень биомеханической совместимости конструкции после интеграции с тканями организма. Например, биомеханические свойства по-
ристого титана улучшаются после прорастания в нем костной ткани. Остеоинтегрированные имплантаты из титана приобрета- ют способность нести функциональную нагрузку, хотя титан ха- рактеризуется довольно низким уровнем биомеханической совме- стимости. Высокий уровень биомеханической совместимости предполагает максимальную близость физико-механических свойств материа- ла и конструкций к свойствам тканей организма, с которыми они функционально взаимодействуют. Физико-механические свойства материала и тканей организма подчиняются единому закону де- формирования и восстановления формы. Металлы и сплавы применяют в имплантологии наиболее широко. В стоматологических учреждениях в нашей стране, в ко- торых производят имплантацию, используют нержавеющую сталь, КХС, титан, никелид титана, серебряно-палладиевый сплав, цир- коний. Перспективными материалами являются титан и его спла- вы, сапфир, гидроксиапатит. Доказано, что такие материалы, как нержавеющая сталь, сплавы на основе Co-Cr-Mo, CO-Cr-W-Ni, титан и его сплавы: Ti6A14V, TiNi, благородные металлы и спла- вы на их основе являются коррозионно-устойчивыми. Способность этих материалов противостоять химическому и электрохимическому воздействию среды (полость рта и ткани, окружающие имплантат) связана с пассивацией металлов, обус- ловленной образованием на поверхности металла пленок труд- норастворимых соединений, например оксидов. Металлургичес- кие, технологические, конструкционные погрешности и другие причины могут привести к повреждению защитной пленки, вы- зывая процессы коррозии и ответную реакцию тканей. Возмож- ны следующие типы коррозии: общая, гальваническая, ямочная, щелевая, коррозия напряжения, включая усталостную коррозию. Из всех перечисленных металлических материалов самой вы- сокой коррозионной стойкостью обладают титан и его сплавы, что позволяет осуществлять пожизненную имплантацию титано- вых конструкций в организм больного. Высокая биосовместимость обусловлена значительно сниженным ионным обменом на поверх- ности раздела имплантат—живая ткань, что обеспечивает стабиль- ную регенерацию клеток. Особый интерес вызывают сплавы на основе никелида титана.
КОНСТРУКЦИИ ИМПЛАНТАТОВ Существует множество систем имплантатов, многообразие которых обусловило необходимость их систематизации. Если взять за основу тот или иной признак, можно создать довольно строй- ную классификацию имплантатов. Например, в зависимости от формы различают цилиндрические (сплошные, полые), винто- образные, листовидные (пластинчатые), конусовидные формы
Рис. 277. Субмукозные имплантаты на полном съемном протезе верх- ней челюсти.
корня естественного зуба; по структуре материала — беспорис- тые, поверхностно-пористые, со сквозной пористостью, комби- нированные; по свойству материала — без эффекта «памяти» формы, с эффектом «памяти» формы; по конструкции внутри- костной части — разборные, неразборные; по конструкции со- единения имплантата с супраструктурой — неразъемное, разъем- ное соединение, винтовое и с помощью магнитных систем. Наиболее известна классификация, основанная на положении имплантата по отношению к костной ткани и мягким тканям полости рта. 1. Внутрислизистые имплантаты (субмукозные). Внутрислизис- тая имплантация применяется для улучшения фиксации протеза при атрофии альвеолярного отростка на верхней челюсти, осо- бенно при дефектах развития неба. Имплантат представляет со- бой двусторонний колпачок, одна часть которого жестко фикси- рована в базисе съемного пластиночного протеза, другая часть (грибовидной формы) вводится в созданное (под анестезией) шаровидным бором отверстие в слизистой оболочке верхней че- люсти. Внутрислизистые имплантаты изготавливают из титана, высоко коррозионно-стойкой стали, КХС. Обычно применяют два ряда: один — по альвеолярному гребню, другой — на небном скате, но не более 14 (рис. 277). 2. Поднадкостничные имплантаты (субпериостальные) представ- ляют собой литые металлические каркасы из благородных спла-
ВОВ или нержавеющей стали. Их изготавливают индивидуально на основании анатомического слепка, снятого со скелетированного участка альвеолярного отростка челюсти. После припасовки и установки на место каркас покрывают заранее отсепарированным слизисто-надкостничным лоскутом и ушивают. Сквозь лоскут в полость рта выступают металлические штифты, которые могут служить опорой для несъемных мостовидных протезов или допол- нительными ретенционными элементами для съемных протезов. Их можно использовать как на верхней, так и на нижней челю- сти, но в большинстве случаев субпериостальные имплантаты применяют на нижней челюсти (рис. 278). 3. Чрескостные имплантаты (трансоссальные). Наиболе е рас- пространенной формой таких имплантатов является трансманди- булярная скоба, состоящая из пластинки, прилежащей к ниж- нему краю нижней челюсти во фронтальном отделе, ограничен- ном ментальными отверстиями, и штифтов, выступающих из этой пластинки. Одни из штифтов (винты) внедряются в челюстную кость, осуществляя внутрикостную фиксацию конструкции; дру- гие, проходя сквозь нее и через слизистую оболочку, выходят в полость рта, где и служат опорными или дополнительными ре- тенционными элементами для фиксации протезов. Имплантаты изготавливают из виталлия, титана или золотосодержащих спла- вов (рис. 279). 4. Эндодонтические имплантаты (эндодонто-эноссальные) — это штифты, выводимые по предварительно расширенным каналам корней фронтальных зубов через апикальные отверстия в кость на глубину от 3 до 5,5 мм. Они служат для закрепления (шини- рования) подвижных зубов при заболеваниях пародонта. Внутри- корневая поверхность имплантата ровная, внутрикостная может быть с резьбой для ввинчивания. Эндодонто-эноссальные им- плантаты изготавливают из титана, тантала, КХС, окиси алю- миния (рис. 280). 5. Внутрикостные имплантаты (эндоссальные, эноссальные). В на - стоящий момент это наиболее широко применяемый тип им- плантатов. В отличие от других типов внутрикостные имплантаты фиксируются не только за счет механических сил, но и благода- ря процессам остеоинтеграции. Различают внутрикостные им- плантаты по Линкову — пластинчатые (рис. 281) и по Бренемарку — цилиндрические, винтовые (рис. 282); последние благодаря приближенной к корню естественного зуба форме получили наи- большее распространение во врачебной практике. После вживле- ния имплантата, если соблюдены все условия, начинается про- цесс остеоинтеграции, т.е. имплантат, который может иметь как цилиндрическую, так и винтовую форму с отверстиями или без них, закрепляется в кости не только за счет формы, но и за счет образования костной ткани непосредственно на поверхности имплантата, «отложения» костной ткани на поверхности имплан- тата и «внедрения» ее в структуру поверхности.
Рис. 278. Субпериостальные имплантаты. а — каркас одностороннего субпериостального имплантата на модели; б — кар- кас двустороннего субпериостального имплантата на модели.
Внутрикостные имплантаты состоят из внутрикостной части, которая обеспечивает фиксацию всей конструкции имплантата в костной ткани. Для фиксации опорной части к имплантату ис- пользуют винт. В некоторых системах эти компоненты составля- ют единое целое.
Конструктивно в имплантате выделяют три основные части: корневую часть, шейку и головку (опорная головка). Применяют и другие термины: корневую часть называют внугриальвеолярнои, или внутриопорной конструкцией, шейку — пришеечной обла- стью имплантата, шейку и головку вместе — внеальвеолярной коронковой частью имплантата. В отдельных конструкциях выде- ляют плечи, ножки имплантата, каркас и т.д.
Рис. 280. Схема эндодонто-эноссального имплантата (а); рентгеновский
Рис. 282. Имплантаты: цилиндри- ческий (а); винтовой (б).
В зарубежной литературе конструкции имплантатов объеди- няют в системы, давая им определенные названия: CBS (рис. 283,а), диск-имплантат по Скортеччи (рис. 283,6), имплантат по Линкову (рис. 283,в), фриолит-имплантат по Шульту (рис. 283,г), AMS (рис. 283,д), IMZ по Киршу, система «Biolox» и др. Каждая система имеет свое инструментальное обеспечение. В связи с тем что стоматологическая имплантация находит все более широкое применение и врачам предлагается большое ко- личество разнообразных имплантационных систем, в 1991 г. на Международном съезде имплантологов были выработаны следу- ющие обязательные требования, предъявляемые к дентальным имплантационным системам:
• подтвержденная клиническим опытом гарантия успеха в от- даленный период; • адекватный материал имплантата; • соответствующий дизайн имплантата; • наличие специальных инструментов для подготовки соответ- ствующих костных полостей под имплантат; • адекватная система охлаждения для предупреждения терми- ческих поражений; • точность форм составляющих частей имплантата; • гарантия поставок составных частей и принадлежностей при изменении системы со стороны фирмы-производителя; • простая и надежная операционная техника и ортопедичес- кая конструкция; • стерильная упаковка с возможностью имплантации без при- косновения к поверхности имплантата; • указание даты стерилизации и срока гарантированной сте- рильности.
Следует более подробно остановиться на некоторых системах. Система CBS представляет собой набор внутрикостных имплан- татов из алюминийоксидной керамики и инструментов для их имплантации. Корневая часть имплантата имеет винтообразную форму, коронковая — круглую форму со шлицами. Размеры: об- щая длина 15—20 мм, диаметр 4 —5 мм. Система AMS — набор пластиночных имплантатов из сплава Ti6A14V и инструментов для имплантации. Конструктивно им- плантат состоит из пластиночной решетчатой внутрикостной ча- сти и головки. Разновидности внутрикостной части различаются по величине пластинки, ее форме (выпуклая и вогнутая), лока- лизации (тело, ветвь нижней челюсти). Диск-имплантат по Скортеччи — это цилиндрический стер- жень с основанием в форме диска и головной частью с винто- вой нарезкой, на которую навинчивают коронковую часть им- плантата. Имплантат изготавливают из чистого титана; выпуска- ется в виде набора, состоящего из трех типоразмеров импланта-
a — CBS; б — Disk-имплантат; в — пластиночный имплантат; г — Frialit-им- плантат; д — AMS.
тов и трех типоразмеров режущих инструментов, соответствую- щих по форме диск-имплантату. Система «Biolox» содержит внутрикостные и эндодонтичес- кие имплантаты из алюминииоксидной керамики как для одно- фазной, так и для двухфазной имплантации, а также инструменты для их установки в челюстных костях. При однофазной имплан- тации в качестве боковой опоры на нижней челюсти используют имплантаты с анкерными крыльями, на верхней челюсти (в пе- реднем отделе) — имплантаты цилиндрической формы с ретен- ционной прорезью в корневой части. Коронковая часть имплан- тата повторяет форму препарированного зуба с уступом под ке- рамическую коронку. Для беззубой нижней челюсти выпускают винтовой цилиндрический имплантат с граневой коронковой частью. В комплект для двухфазной имплантации входит разбор- ный имплантат с винтовой нарезкой и внутренним отверстием для соединения с коронковой частью имплантата.
В настоящее время наиболее широкое применение нашли цилиндрические внутрикостные имплантаты как результат раз- вития системы Бренемарка. По статистическим данным, свыше 80 % всех видов имплантатов, используемых в настоящее время за рубежом во врачебной практике, составляют именно такие имплантаты. Применяется также классификация дентальных имплантатов по их «поведению» в костной ткани: 1) пассивные; 2) механически активные (с памятью формы); 3) химически активные (ГАП). Пассивными называют имплантаты с инертным поведением в зонерепаративного остеогенеза; химически активными — участву- ющие в процессе остеогенеза; механически активными — участву- ющие как в процессе репаративного остеогенеза, так и в ремо- делировании костной ткани на всем протяжении функциониро- вания имплантата. Типичным механически активным имплантатом является кон- струкция, предложенная М.З.Миргазизовым, В.Э.Понтером, В.И.Итиным, получившая название МГИ (рис. 284). Этот им- плантат в своей конструкции содержит механически активные элементы из сплавов с «памя-
• Обеспечение способнос- ти костной ткани генери- ровать электрические по- тенциалы под влиянием механических воздей- ствий. • Поддержка квазипостоян- ной электрической актив- ности кости за счет внут- ренних механических на- пряжений в костной тка- ни.
Рис. 284. Цилиндрический им- плантат с памятью формы.
5БЗ • Регуляторное влияние сил сжатия на пролиферацию и вы- работку компонентов внеклеточного матрикса в костной ткани. • Стимуляция функциональной активности костной ткани. • Возрастание уровня костной перестройки в зонах повышен- ной нагрузки как за счет количества циклов ремоделирова- ния, так и за счет усиления репаративных процессов в ответ на появление микроповреждений вследствие перегрузки. • Активация процессов резорбции в зонах сниженной нагрузки в результате увеличения частоты циклов ремоделирования. Многообразие конструкций имплантатов затрудняет их выбор. С целью облегчения этой задачи можно пользоваться следующи- ми рекомендациями. Конструкцию имплантата следует выбирать в соответствии с клиническими условиями с учетом: • переносимости организмом пациента материала; • степени атрофии альвеолярных отростков на тех участках, где отсутствуют зубы; • анатомо-топографических соотношений альвеолярных греб- ней и верхнечелюстных пазух, носовой полости и нижне- челюстного канала; • толщины слизистой оболочки, покрывающей альвеолярные отростки; • толщины нижней челюсти в переднем и боковых отделах. Например, при выраженной атрофии альвеолярных отрост- ков и близком расположении к гребню пазух и канала показано применение поднадкостничного имплантата, при небольшой толщине нижней челюсти в боковых отделах целесообразно ис- пользовать пластиночные имплантаты. В остальных случаях отда- ют предпочтение цилиндрическим имплантатам. Если ожидается значительная жевательная нагрузка на им- плантат, необходимо сделать выбор в пользу имплантатов с амор- тизаторами. Кроме того, выбор конструкции имплантата может быть обусловлен методом имплантации, который планируется использовать в том или ином случае. Например, для двухфазной имплантации может быть применена только разборная конструк- ция; для непосредственной имплантации предпочтительнее ке- рамические имплантаты, имеющие форму корня естественного зуба. Выбор конструкции имплантата зависит также от возмож- ностей их приобретения или изготовления в конкретном учреж- дении и инструментального обеспечения. В связи с этим большую ценность для врача представляют готовые комплекты импланта- тов и инструментов, которые облегчают выбор имплантата и его применение, поскольку эти комплекты создают для решения кон- кретных задач ортопедического лечения с использованием имп- лантатов. После выбора типа имплантата подбирают конструкционные элементы, лабораторные приспособления и инструменты. МЕТОДЫ ИМПЛАНТАЦИИ Существующие методы имплантации могут быть сгруппиро- ваны по следующим классификационным признакам: по сроку имплантации — непосредственно после удаления зуба (имплан- тация в свежую лунку удаленного зуба), отсроченные (после полного заживления лунки зуба); по признаку сообщения с по- лостью рта в период приживления имплантата — сообщающиеся (однофазная имплантация), несообщающиеся (двухфазная мето- дика с «закрытым» приживлением корневой части имплантата в первой фазе). В зависимости от выбора этих методик приживле- ние имплантата происходит в условиях функциональной нагруз- ки или без нее. Сущность методики непосредственной имплантации заключа- ется в том, что операцию имплантации проводят одновременно с удалением зуба. Этот метод целесообразно применять для за- мещения передних зубов, но он противопоказан после удаления зубов при заболеваниях пародонта. По мнению сторонников методики непосредственной имплан- тации, она обеспечивает плотный охват шейки имплантата во- локнами маргинальной связки, если их аккуратно отсепариро- вать и сильно не травмировать при удалении зуба. Классическим примером для непосредственной имплантации являются тюбингенские непосредственные имплантаты (Frialit) из алюминийоксидной керамики ступенчато-цилиндрической формы с лакунами по всей корневой поверхности. В пришеечной области этих имплантатов имеется гладко отполированная бороз- дка для десны. Головка имплантата разборная, она фиксируется в корневой части после введения ее в костное ложе. Тюбингенс- кие имплантаты применяют для замещения резцов, клыков и премоляров, подлежащих удалению вследствие травмы, резорб- ции корней и других причин, кроме заболеваний пародонта. Операция заключается в удалении зубов или их корней, пос- ледовательной обработке лунки конусовидным, цилиндрическим и ступенчатым сверлом, введении имплантата в костное ложе, фиксации имплантата с помощью лигатурного связывания, за- щиты раны эластичной повязкой на 6 дней. После этого прово- дят временное протезирование, а через 3 мес — постоянное; обычно изготавливают металлокерамические протезы. Методика отсроченной имплантации заключается в формиро- вании искусственной лунки (костного ложа) для имплантата после окончательного заживления костной раны после удаления зубов. Сроки здесь могут быть разными — от 1,5 мес до 1 года в зависимости от интенсивности репаративных процессов. Имплан- тологи справедливо считают, что только при полном заживле- нии костной ткани возможно создание искусственной лунки, обеспечивающей плотный контакт имплантата с костью и его устойчивость. Этот способ применяют наиболее часто, посколь-
5ББ ку у большинства больных, обращающихся по поводу имплан- тации, как правило, зубы давно отсутствуют. Операция имплантации включает четыре последовательных этапа: 1) иссечение и отслаивание слизисто-надкостничного лоскута; 2) создание костного ложа для имплантата; 3) введение имплантата в костное ложе; 4) закрытие послеоперационной раны. Первый этап может быть выполнен двумя способами: иссе- чением слизисто-надкостничного лоскута с помощью пробойника (компостера) или скальпеля с последующей отслойкой и отки- дыванием его. Костное ложе для имплантата (второй этап) может быть со- здано разными способами: сверлением, с помощью долота или комбинированным методом (сверление и формирование ложа с помощью долота). Сверление можно производить бормашиной на низких оборотах или ручным способом, что полностью исклю- чает перегревание костной ткани. Оптимальные условия для свер- ления кости возникают при применении локальной гипотермии с помощью аппарата «Ятрань» [Миргазизов А.М., 1988]. Третий этап — введение имплантата в костное ложе — также может быть выполнен разными способами: вкручиванием (при использовании винтообразных имплантатов), вколачиванием и свободным размещением имплантата в костное ложе. Последний этап — закрытие послеоперационной раны — зак- лючается в укладывании слизисто-надкостничного лоскута и фиксации его швами. При иссечении слизисто-надкостничного лоскута с помощью компостера швы не накладывают: достаточ- но закрыть рану тампоном или защитной базисной пластинкой. Далее рассмотрим методы однофазной и двухфазной имплан- тации. Методика однофазной имплантации состоит в том, что корне- вую часть имплантата плотно устанавливают в костном ложе, а головка при этом выступает в полость рта. Пришеечная часть имплантата вступает в контакт со слизистой оболочкой. Этот способ прост и доступен для широкого применения, не требует сложных разборных конструкций имплантатов. Однако при его применении высока вероятность неудач, поскольку при сообще- нии с полостью рта процессы регенерации замедляются. Методика двухфазной имплантации предусматривает прижив- ление сначала только корневой, внутрикостной части импланта- та в условиях изоляции от полости рта. Лишь после успешного решения этой задачи к корневой части имплантата присоединя- ют его головку. Классическим примером двухфазной методики имплантации является система Бренемарка, применяемая при полном отсутствии зубов. Показания к этой системе: 1) не- достаточная фиксация полных съемных протезов из-за выражен-
ной атрофии альвеолярных отростков; 2) неспособность больно- го адаптироваться к съемным протезам независимо от степени их фиксации; 3) функциональные расстройства (тошнота, рво- та), связанные с применением съемных протезов, при этом воз- раст больных колеблется в больших пределах — от 20 до 77 лет. Для большинства больных необходим примерно год пользования полными съемными протезами, чтобы произошла окончательная функциональная перестройка кости после удаления зубов. В некоторых источниках встречается утверждение о необходи- мости применения числа имплантатов, соответствующего коли- честву удаленных зубов. К сожалению, в подавляющем большин- стве случаев это невозможно. Наиболее приемлемой следует счи- тать конструкцию, когда двум прижившимся имплантатам соот- ветствует один искусственный зуб (фасетка). Оперативные вмешательства производят в два этапа (фазы): введение корневой части имплантата (первая фаза) и подсоеди- нение головки (вторая фаза). Дата добавления: 2015-12-16 | Просмотры: 1080 | Нарушение авторских прав |
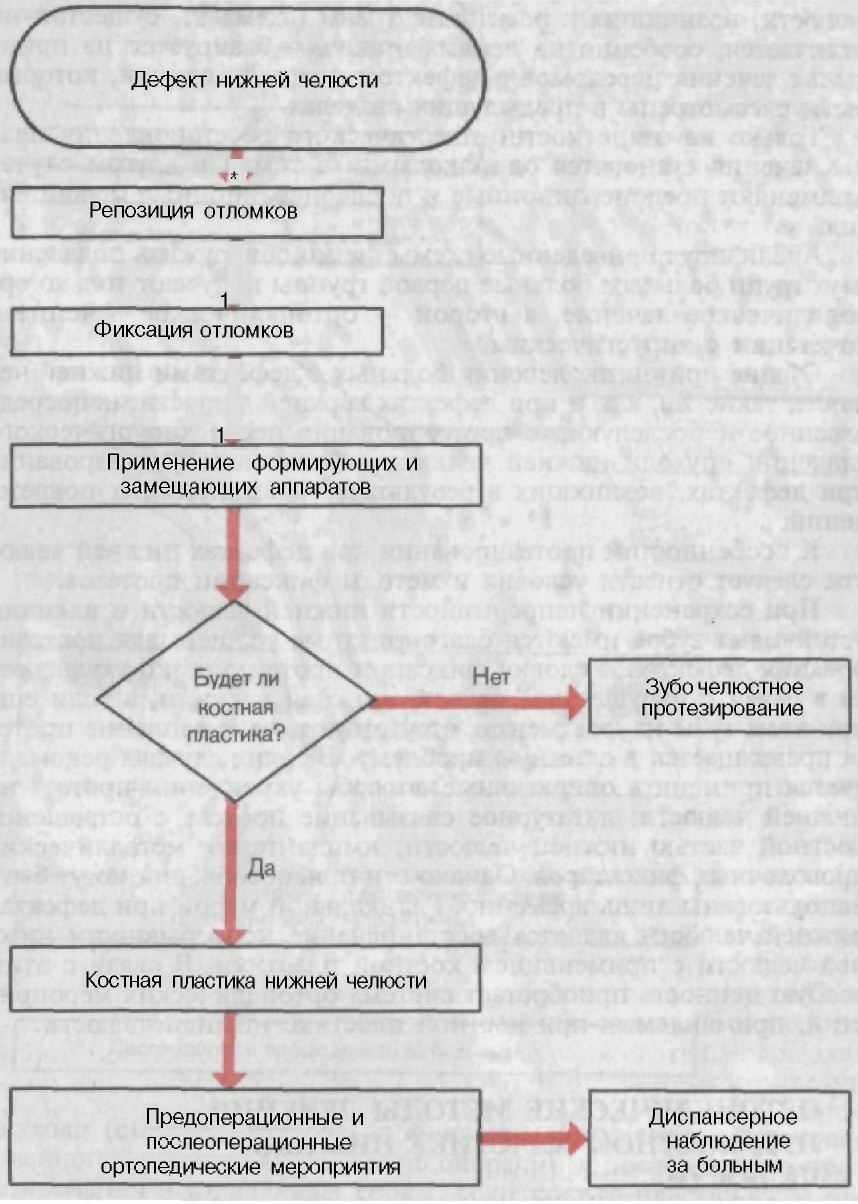
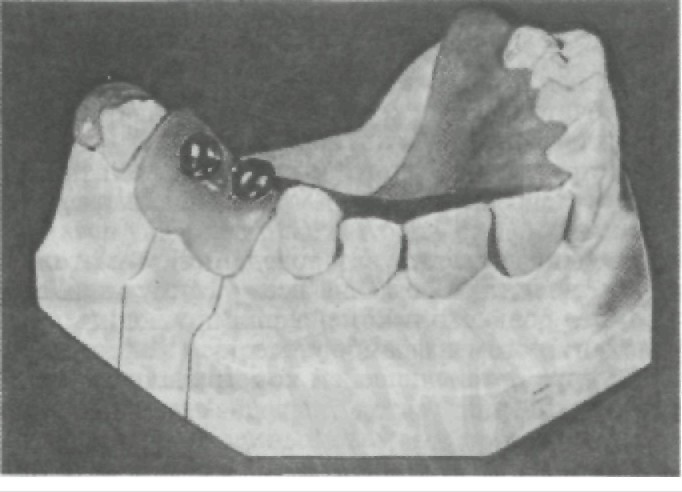
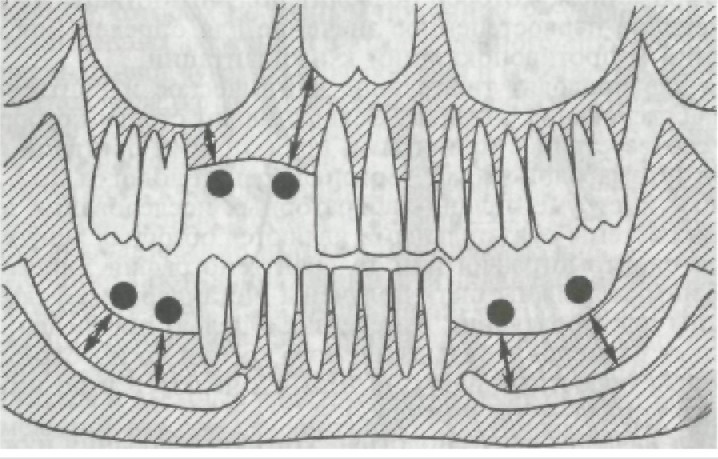
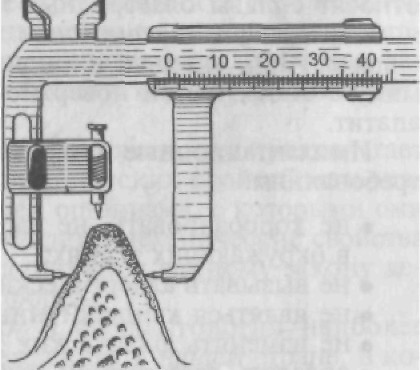
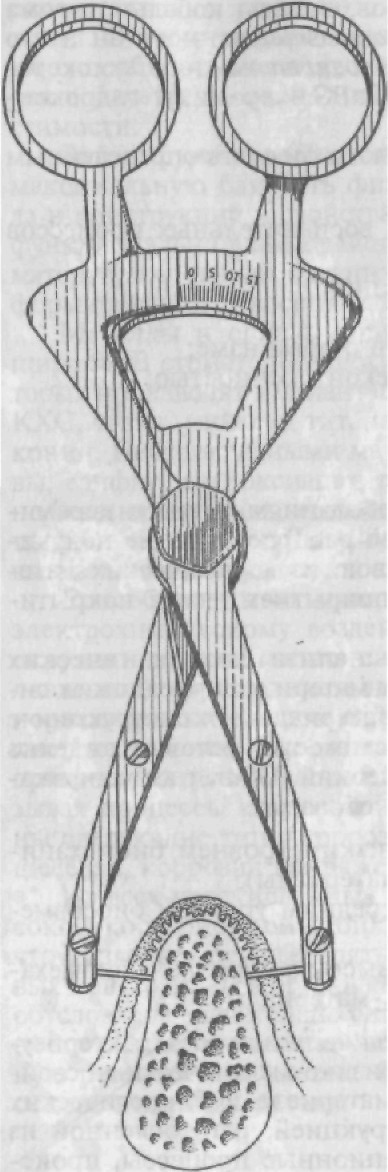 Рис. 276. Специальный штанген- циркуль.
Рис. 276. Специальный штанген- циркуль.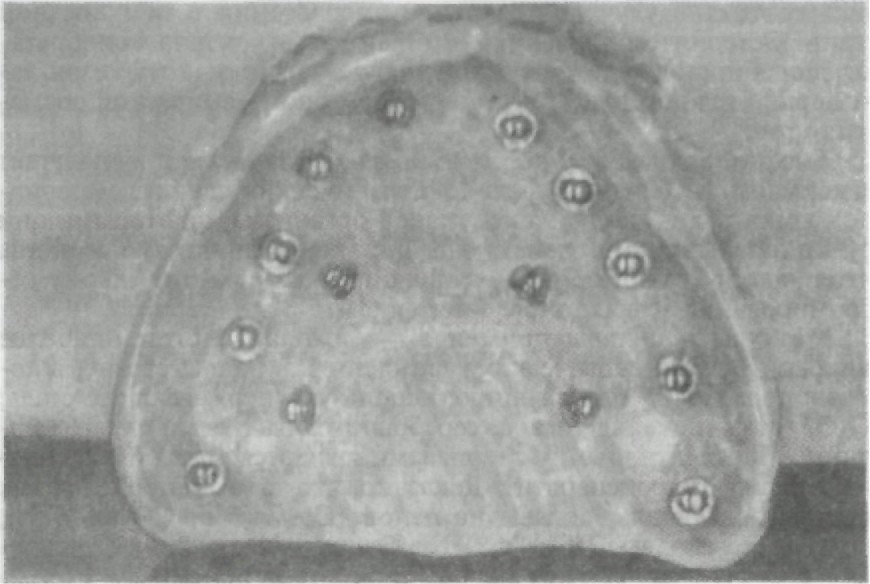
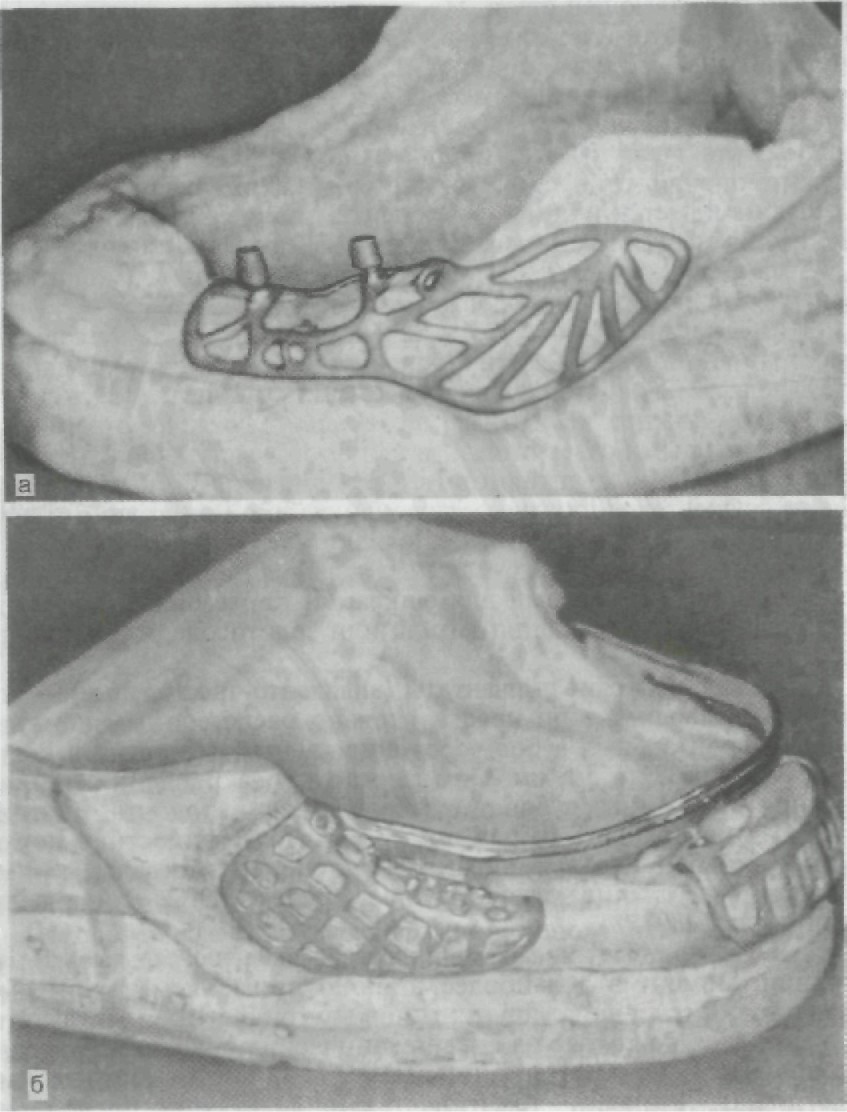
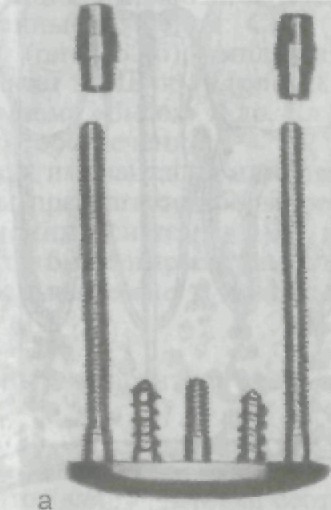 Рис. 279. Чрескостный имплантат (а); рентгеновский снимок (б).
Рис. 279. Чрескостный имплантат (а); рентгеновский снимок (б).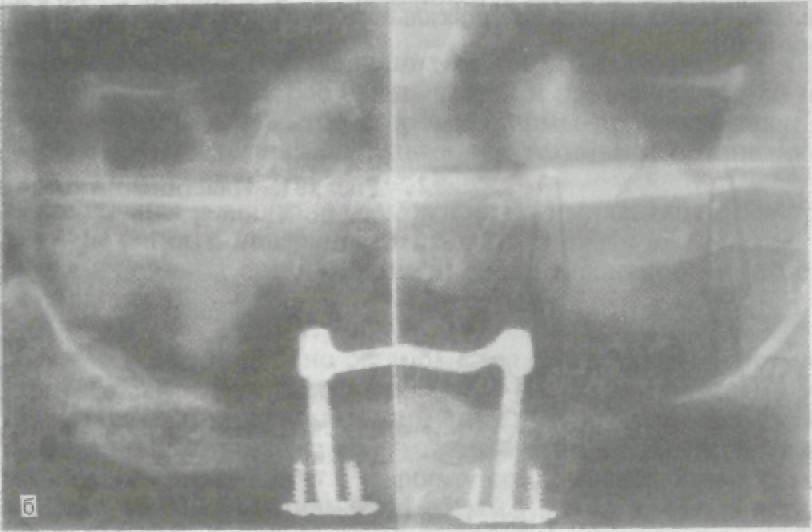
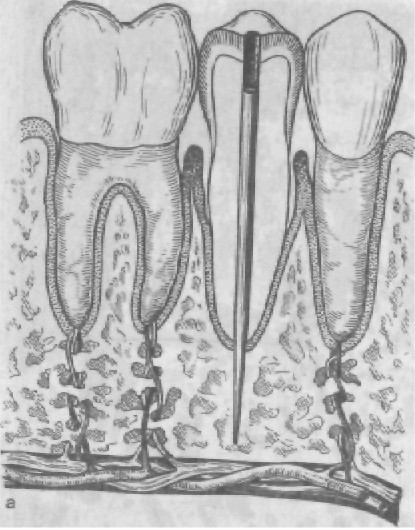
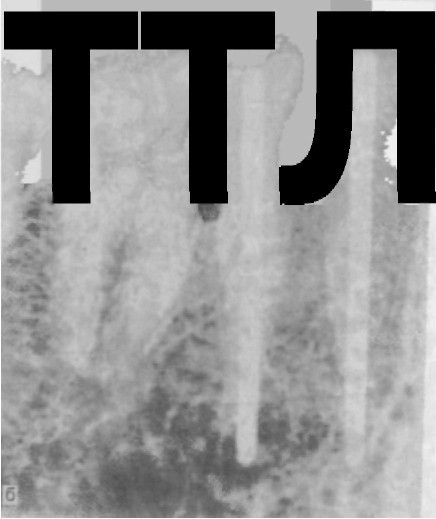
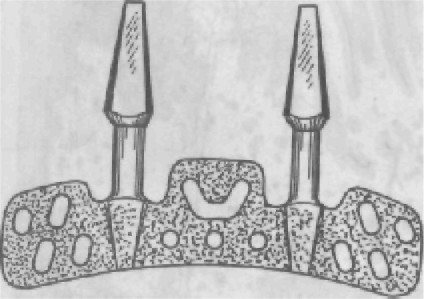 Рис.281. Пластиночныйимплан- тат по Линкову.
Рис.281. Пластиночныйимплан- тат по Линкову.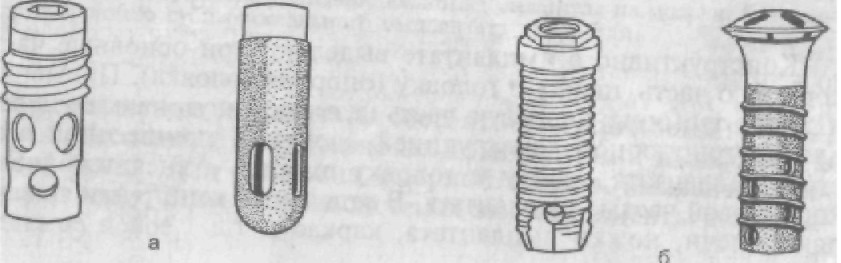
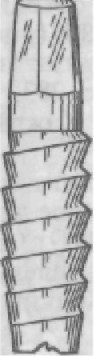
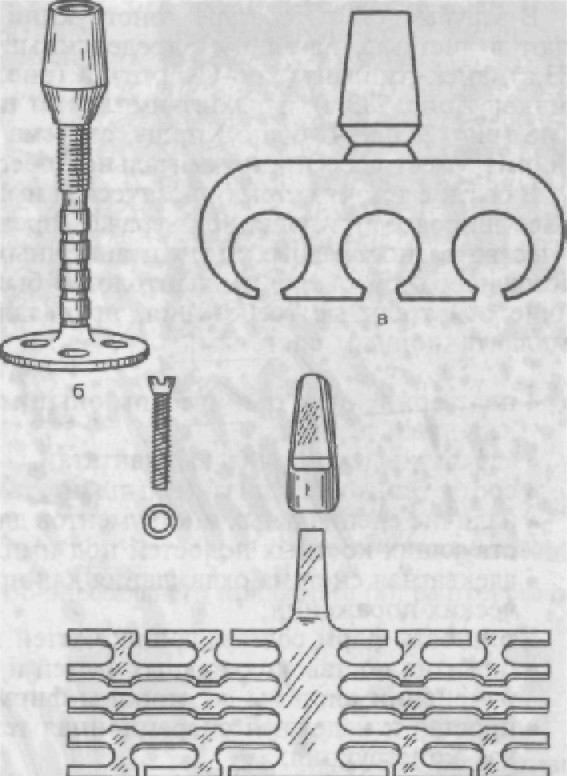

 Рис. 283. Виды имплантатов.
Рис. 283. Виды имплантатов.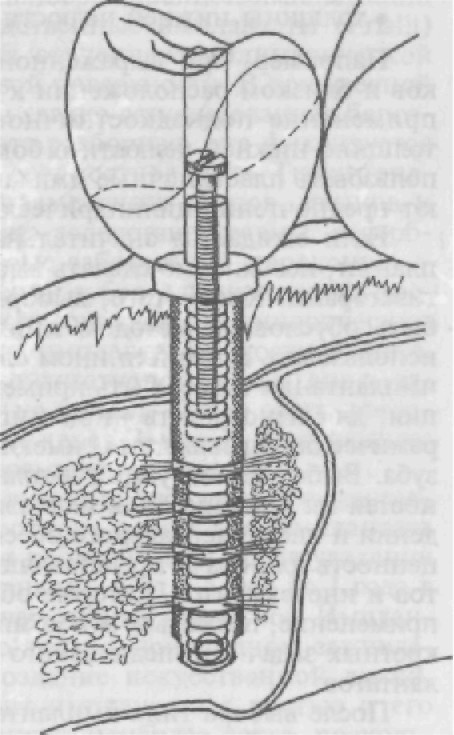 тью» формы в виде тонких ни- тей, имитирующих периодон- тальные связки. Конструкция построена с учетом роли меха- нических факторов в процессах моделирования, ремоделирова- ния и репаративной регенера- ции костной ткани, которая состоит в следующем.
тью» формы в виде тонких ни- тей, имитирующих периодон- тальные связки. Конструкция построена с учетом роли меха- нических факторов в процессах моделирования, ремоделирова- ния и репаративной регенера- ции костной ткани, которая состоит в следующем.