|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Защитные механизмы дыхательных путей и респираторных отделов легкихЛегкие уникальны по своему строению и еще более уникальны по функциональным возможностям. Для обеспечения респираторной функции через легкие за сутки проходит 8000–20000 литров воздуха, содержащего различные полютанты: механические частицы, химические соединения в виде газов, микроорганизмы. Респираторные повреждающие факторы контактируют с огромной поверхностью проводящих дыхательных путей – 60000 терминальных бронхиол, 500000 респираторных бронхиол и 80000000 альвеол, площадью 50–70 квадратных метров, что создает условия для повреждения бронхов и легких. Комплексная эффективная защита дыхательных путей осуществляется с помощью естественных механизмов (аэродинамическая фильтрация, мукоцилиарная транспортная система, кашель) и факторов неспецифической и специфической противоинфекционной защиты. Совершенные, согласованно функционирующие механизмы защиты позволяют обеспечивать очистительную дренажную функцию дыхательных путей, стерильность респираторных отделов, восстановление нарушенных структур и функций респираторной системы. Эпителий слизистой оболочки верхних дыхательных путей - один из основных защитных барьеров. Под влиянием цитокинов и продуктов микробного происхождения эпителиальные клетки экспрессируют молекулы адгезии, цитокины и другие молекулы, важные для реализации иммунных процессов. Слизистая оболочка респираторного тракта обладает местным иммунитетом - MALT (Мucosal Associated Lymphoid Tissues). Лимфоциты, активированные в лимфоидной ткани слизистых оболочек, мигрируют через региональные лимфатические узлы и возвращаются через грудной проток и кровеносное русло обратно в слизистые оболочки. В формировании местного иммунитета берут участие мононуклеарные фагоциты, система комплемента, интерферон (ИФН), лизоцим, концентрация которого в миндалинах в 300 раз выше, чем в сыворотке крови и др. Лимфоэпителиальный комплекс в общей системе иммунокомпетентных органов принимает активное участие в формировании местного и системного иммунитета, продуцируя антитела, образуя клетки иммунной памяти (малые лимфоциты с крупными ядрами, которые являются носителями закодированной информации), выполняет информативную, защитную, нейрорефлекторную и кроветворную функции.
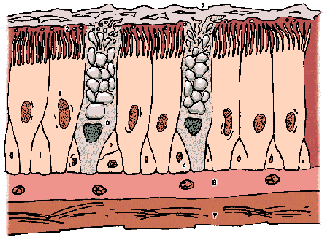
Для эффективного и, что еще важнее, длительного функционирования респираторная система обладает высокоэффективной системой защиты, при этом мукоцилиарный транспорт является самым важным механизмом. Мукоцилиарный клиренс (МЦК) (англ. clearance - очищение) - выведение трахеобронхиального секрета/слизи, обусловленное колебательными движениями ресничек однослойного многорядного мерцательного эпителия слизистой оболочки. Мукоцилиарный клиренс является важнейшим механизмом, обеспечивающим санацию дыхательных путей, одним из основных механизмов системы местной защиты и обеспечивает необходимый потенциал барьерной, иммунной и очистительной функции респираторного тракта. Очищение дыхательных путей от чужеродных частиц и микроорганизмов происходит благодаря оседанию их на слизистых оболочках и последующему выведению вместе со слизью. Диагностическое и клиническое значение имеет состав трахеобронхиального секрета, который по физико-химической структуре представляет собой многокомпонентный коллоидный раствор, обеспечивающий эффективность мукоцилиарного клиренса. Трахеобронхиальный секрет следует рассматривать как постоянно обновляющийся фильтр. В соответствии с концепцией двухслойности секрета слизь состоит из наружного гелеобразного слоя толщиной 2 мкм (гель) и лежащего под ним более жидкого слоя (золь) толщиной 2–4 мкм. Согласованные биения ресничек (16–17 раз в секунду) способствуют продвижению и выведению секрета в проксимальном направлении. Пропорции в соотношении слоев слизи: геля и золя, пропорции в соотношении бокаловидных и реснитчатых клеток (1:3,1:5), частота колебаний ресничек (200 колебаний в минуту) являются залогом нормального функционирования мукоцилиарного клиренса (рис.11).
Рисунок 11. Мукоцилиарный клиренс (транспорт).
Суточный объем ринобронхиального секрета колеблется в широких пределах, составляя в среднем 0,1–0,75 мл/кг массы тела. Благодаря нормальной деятельности мукоцилиарной транспортной системы бактерии в секрете движутся со скоростью 10 клеток слизистой бронхов за 1 с, что сводит время контакта микроорганизма с клеткой до 0,1 с и затрудняет его прикрепление к эпителию слизистой оболочки. Скорость мукоцилиарного транспорта у здорового человека колеблется от 4 до 20 мм в минуту. В норме за сутки транспортируется от 10 до 100 мл секрета, который, попадая в глотку, проглатывается или выкашливается. Трахеобронхиальный секрет представляет собой многокомпонентный коллоидный раствор, состоящий из двух фаз: растворимой, жидкой – золь и нерастворимой, вязкоэластичной – гель. Золь непосредственно лежит на слизистой и является средой, в которой функционируют реснички. В состав золя входят электролиты, сывороточные компоненты, местно секретируемые белки, биологически активные вещества, ферменты и их ингибиторы. Гель – наружный слой бронхиального секрета толщиной 2 мкм, состоит из капель и комков слизи, осевших на поверхности золя. Гликопротеины геля формируют фибриллярную структуру, представляющую собой ячеистую сеть, «прошитую» водородными связями. Гель способен перемещаться только после превышения предела текучести, т.е. тогда, когда разрываются связанные между собой ригидные цепи (поперечные дисульфидные и водородные связи). Слой слизи соответствует длине ресничек – 7 мкм. В дыхательных путях взрослого человека продуцируется от 10–15 до 100–150 мл бронхиального секрета. Мукоцилиарный клиренс представляет собой важнейший механизм, обеспечивающий санацию дыхательных путей. Он осуществляется с помощью цилиарных клеток, каждая из которых содержит около 200 ресничек, совершающих 230–260 колебательных движений в минуту. Скорость мукоцилиарного транспорта у здорового человека колеблется от 4 до 20 мм/мин., создавая минимальные временные условия (0,1 с) для контакта эпителиальной клетки с повреждающим фактором. Эвакуация слизи по спирали столь равномерна, что не раздражает кашлевые рецепторы и слизь подсознательно заглатывается.
Очищение воздухопроводящих путей происходит за 3–5 дней, что клинически проявляется синдромом элиминации аллергена при бронхиальной астме. В респираторных отделах легкого мукоцилиарный аппарат отсутствует, и их очищение происходит отчасти за счет экспираторных движений воздушной струи (в особенности при кашле), отчасти за счет фагоцитарной функции клеточных элементов. В зависимости от фагоцитированного материала макрофаги легких получают различные специальные названия: сидерофагов, или «клеток сердечных пороков» (при поглощении эритроцитов), «пылевых клеток» (при фагоцитозе частиц пыли), ксантомных клеток (при накоплении липоидов). Скорость очищения различных отделов дыхательного аппарата неодинакова. Показательны данные Nadel и Gamsu (1973), полученные на добровольцах, которым вдували танталовый порошок в дыхательные пути. Время половины очищения, которое определяли по уменьшению контрастности бронхограмм на 50%, составило в среднем для трахеи и главных бронхов — 5,5 ч, для бронхов диаметром от 1 до 6 мм — 13,5 ч, для проксимальных отделов бронхиол — 33,5 ч, для дистальных — 90 ч. В терминальных же отделах очищение от танталового порошка не наступало даже через 15 мес. Среди факторов гуморального звена значительная роль принадлежит иммуноглобулинам (IgG, IgA, IgM). Наиболее важное значение среди них имеют иммуноглобулины класса А, содержание которых в бронхоальвеолярном смыве больше, чем в сыворотке крови. IgA синтезируется лимфоидными клетками костного мозга, селезенки, лимфоузлов, БАЛТ, плазматическими клетками подслизистого слоя бронхов. Выработку IgA стимулирует антиген, попавший в просвет бронхиального дерева. Синтезируемый местно мономер IgA с помощью гликопротеида, молекулярная масса которого составляет 1500 кД, преобразуется в димер. Последний соединяется с пептидным фрагментом, синтезируемым эпителиальными клетками слизистой оболочки бронхов и обозначается как секреторный компонент. Этот компонент способствует проникновению димеров IgA в бронхоальвеолярное пространство и защищает молекулу секреторного IgA (sIgA) от разрушения протеолитическими ферментами. Только 5% IgA поступает в бронхоальвеолярное пространство из сыворотки крови. IgA проявляет наибольшую функциональную активность в проксимальных отделах респираторного тракта, оказывая противовирусное и антимикробное действие, уменьшая адгезивную способность микроорганизмов к слизистой оболочке. IgA принимает участие в активации комплемента по альтернативному пути, способствуя тем самым лизису микробов, усиливает антимикробное действие лизоцима и лактоферрина, антителозависимую клеточную цитотоксичность. Кроме того, этот иммуноглобулин предотвращает размножение вируса в месте внедрения, препятствует образованию аутоантител. В противомикробной защите мелких бронхов немаловажную роль играет IgG. Источник IgG легких – сыворотка крови и БАЛТ. Одним из факторов гуморального звена МЗ является комплемент – система белков сыворотки крови, включающая 9 компонентов (С). Описаны классический (иммунный) и альтернативный (пропердиновый) пути активации комплемента. Биологическое значение комплемента связано с его участием в воспалительных и иммунных реакциях легочной ткани. Комплемент оказывает опсонирующее действие, участвует в хемотаксисе и адгезии, оказывает влияние на секрецию гликопротеинов слизи, движение ресничек мерцательного эпителия бронхов, регулируя таким образом мукоцилиарный клиренс. Признается, что дефицит С3 приводит к частым инфекционным заболеваниям, имеет большое значение в патогенезе аспириновой бронхиальной астмы. Важным биологическим свойством лизоцима (мурамидазы) является антимикробное действие, связанное с его способностью расщеплять полисахаридную часть клеточной мембраны, вызывая лизис бактерий (стрептококки группы А, грамотрицательные бактерии и грибы). Кроме того, лизоцим угнетает хемотаксис нейтрофилов и продукцию ими токсичных кислородных радикалов, увеличивает скорость поглощения бактерий и пролиферацию лимфоцитов. Другими словами, лизоцим регулирует воспалительные реакции и оказывает влияние на процессы фагоцитоза. Основными источниками лизоцима являются моноциты крови, нейтрофилы, АМ, серозные клетки бронхиальных желез. В связи с тем, что концентрация лизоцима в легких больше, чем в других органах, его относят к факторам защиты легких. При хроническом бронхите в результате гиперплазии и гипертрофии бронхиальных желез происходит снижение секреции лизоцима, что приводит к угнетению антимикробной функции. Альвеолярные макрофаги (АМ) секретируют в 10 раз большее количество лизоцима, чем нейтрофилы, и обладают большей бактерицидной способностью. Лизоцим оказывает влияние также на реологические свойства слизи в просвете бронхов, прежде всего на структуру геля. При дефиците лизоцима нарушается мукоцилиарный клиренс. Выработка альвеолярными макрофагами и интерферонов имеет важное значение в противовирусной защите легких. На протяжении бронхиального дерева и респираторной ткани выделяют БАЛТ в виде скопления лимфоидных клеток, лимфоидных узлов и узелков. Эта ткань является резервуаром иммунокомпетентных клеток и способствует развитию местных иммунных реакций при попадании антигенов в дистальные отделы легких. В составе БАЛТ на долю Т-лимфоцитов приходится около 73%, В-лимфоцитов – 7%, 0-лимфоцитов – 20%.
Дата добавления: 2015-02-05 | Просмотры: 1425 | Нарушение авторских прав |