 |
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Общий осмотр. Состояние больных (удовлетворительное, средней тяжести и тяжелое) определяется тяжестью заболеванияСостояние больных (удовлетворительное, средней тяжести и тяжелое) определяется тяжестью заболевания. Положение больных может быть активным, пассивным и вынужденным. К последнему, например, относится положение ортопноэ (от греческого orthos – стоя, pnoe – дыхание). Из других вынужденных положений следует назвать: положение на больном – боку при сухом плеврите, что приводит к уменьшению боли за счет снижения трения плевральных листков и ограничения участия в акте дыхания пораженной стороны; платипноэ (от греческих слов platy – плоско, pnoe – дышать) – улучшение дыхания в положении лежа; встречается при двустороннем поражении легких, например, при множественной рецидивирующей тромбоэмболии ветвей легочной артерии, двусторонней нижнедолевой пневмонии, когда в вертикальном положении одышка усиливается за счет прилива крови и ухудшении вентиляционно-перфузионного соотношения в нижних долях; – положение на здоровом боку, когда больному легче дышать за счет улучшения кровоснабжения непораженного легкого при односторонних обтурационном и компрессионном ателектазах; однако, в ряде случаев (пневмония), это положение становится опасным из-за возможности попадания гноя из пораженной стороны в здоровую. Изменение цвета кожи и видимых слизистых оболочек имеет важное диагностическое значение. Цианоз (синюшность) – наиболее часто встречаемое изменение окраски кожи при заболеваниях органов дыхания, обусловленное альвеолярной гипоксией и увеличением содержания восстановленного гемоглобина. Бледность кожного покрова связана с развитием сопутствующей анемии и имеет место при хронических нагноительных заболеваниях легких, раке и легочном кровотечении. На лице может выявляться herpes labialis et nasalis, гиперемия щеки на стороне поражения при пневмококковой пневмонии. Поражение легких при системных заболеваниях соединительной ткани сопровождается появлением на коже геморрагической сыпи. При многих хронических нагноительных заболеваниях легких (абсцесс, бронхоэктазы) может встречаться симптом «барабанных палочек» – булавовидное утолщение концевых фаланг пальцев рук. При осмотре шеи определяют степень участия в акте дыхания вспомогательных мышц (кивательной, трапециевидной и др.) и наличие их гипертрофии (увеличение работы при хронических заболеваниях легких). Следует оценить состояние шейных вен, расширение и пульсация свидетельствуют о повышении давления в них и развитии сердечной недостаточности, осложняющей течение заболеваний органов дыхания. Дыхание через плотно сжатые губы указывает на наличие дыхательной недостаточности у больных с обструктивными заболеваниями легких (увеличивается сопротивление выдоху и повышается давление в дыхательных путях, что предотвращает экспираторный коллапс мелких бронхов). Осмотр грудной клетки. Оценивается форма грудной клетки, симметричность расположения ключиц, лопаток, обеих половин грудной клетки, выраженность над- и подключичных ямок, ширина межреберных промежутков, величина эпигастрального угла, частота и глубина дыхания, участие вспомогательной дыхательной мускулатуры в акте дыхания. В норме форма грудной клетки соответствует конституциональному типу телосложения. При различных заболеваниях форма грудной клетки может изменяться. Выделяют следующие патологические формы: – Бочкообразная или эмфизематозная форма характеризуется увеличением передне-заднего размера грудной клетки, находится как бы в положении максимального вдоха; само название говорит о том, что она встречается при синдромах бронхиальной обструкции и эмфиземе легких, при которых имеет место снижение эластических свойств стенок альвеол и нарушение спадения легочной ткани на выдохе, что приводит к затруднению дыхания; при осмотре обнаруживается выбухание над- и подключичных ямок, участие вспомогательной мускулатуры в акте дыхания, расширение межреберных промежутков, втяжение их во время вдоха. – Для паралитической формы свойственны выраженные признаки астенической грудной клетки: преобладание поперечного размера, атрофия мышц грудной клетки, асимметричное расположение ключиц и лопаток, ребра сильно наклонены книзу, западение надключичных ямок, находится в положении максимального выдоха; эта форма грудной клетки встречается при длительно протекающих и приводящих к истощению хронических воспалительных заболеваниях легких и плевры, туберкулезе, раке легкого. – Рахитическая или «килевидная» грудная клетка (pectus carinatum) может встречаться при рахите, она напоминает кури-ную грудь или киль корабля за счет того, что грудина выдается вперед; в области соединения ребер с грудиной можно обнаружить четкообразные утолщения («рахитические четки»). – Воронкообразная форма грудной клетки (pectus excavatum) характеризуется наличием вдавления в нижней трети грудины («впалая грудь» или «грудь сапожника»), она встречается при аномалиях развития, рахите, синдроме Марфана, деформация грудной клетки может механически оказывать влияние на сокращения сердца, вызывать аритмии. – Ладьевидная грудная клетка в отличие от воронкообразной имеет углубление в области верхней и средней трети грудины, по форме схожее с углублением лодки и описана при сирингомиелии (поражении боковых столбов спинного мозга). – Аномалии развития позвоночника в сагиттальной и фронтальной плоскостях могут приводить к развитию кифосколиотической грудной клетки; при этом следует различать деформацию выпуклость в сагитальной плоскости: кпереди – лордоз, кзади –кифоз; искривление в боковую сторону (во фронтальной плоскости) называется сколиозом; в большинстве случаев встречается их сочетание, особенно кифосколиоз – искривление позвоночника кзади и в сторону; данная деформация приводит к нарушению лёгочной вентиляции, формированию легочной гипертензии и хронического легочного сердца; причинами кифосколиоза являются туберкулез и травмы позвоночника, полиомиелит, рахит, торакопластика. Важную информацию при осмотре грудной клетки можно получить при определении ее симметричности. В отличие от нормы, когда она симметрична, в патологии выявляют асимметрию грудной клетки в виде увеличения или уменьшения одной из половин. Увеличение объема одной из половин грудной клетки встречается при синдроме гидроторакса (наличие жидкости в плевральной полости воспалительного или не воспалительного характера), пневмоторакса (наличие воздуха в плевральной полости), гидропневмоторакса (одновременном скоплении и жидкости и воздуха в плевральной полости). Параллельно пораженная сторона отстает в акте дыхания и имеет сглаженность межреберных промежутков. Уменьшение одной из половин грудной клетки наблюдается при уменьшении объема легочной ткани вследствие пневмосклероза или оперативного вмешательства (удаление доли или всего легкого), развитии локального или распространенного фиброзного процесса в плевральной полости, при синдроме обтурационного ателектаза (спадение всего или части легкого вследствие закрытия просвета бронха опухолью или инородным телом). Диагностическое значение имеет определение симметричности расположения ключиц, надключичных ямок и лопаток. Так, при развитии туберкулезного инфильтрата в области верхушки легкого, верхнедолевой пневмонии, сухом плеврите, переломе ребер может наблюдаться более высокое расположение ключиц и лопаток вследствие рефлекторного спазма грудных мышц при раздражении болевых рецепторов. Осмотр больного позволяет оценить основные параметры дыхания – тип, частоту, глубину и ритм. Существуют различные физиологические варианты дыхания: грудной тип (реберный), когда дыхательные движения осуществляются за счет сокращения межреберных мышц, присущ женщинам; брюшной тип (диафрагмальный), когда дыхательные движения осуществляются преимущественно за счет сокращения диафрагмы, чаще встречается у мужчин; смешанный тип, когда дыхательные движения происходят за счет сокращения межреберных мышц и диафрагмы, встречается у лиц пожилого возраста. Для нормального дыхания в среднем характерна частота от 16 до 20 в минуту, физиологическое урежение частоты дыхательных движений до 12-14 в минуту наблюдается во время сна, средняя глубина (по дыхательному объему 500 – 800 мл) и правильный ритм. Изменения частоты дыхания бывают в виде учащения или тахипноэ (tachypnoe) и урежения или брадипноэ (bradypnoe). Физиологическое тахипноэ встречается в основном при значительной физической нагрузке, а брадипноэ – во время сна. В патологии тахипноэ свидетельствует о развитии дыхательной недостаточности и вызывается следующими причинами: обструкция дыхательных путей при бронхиальной астме или бронхиолите, хроническом бронхите; снижение объема дыхательной поверхности легких при развитии пневмококковой пневмонии, обтурационном или компрессионном ателектазе, пневмотораксе; ограничение глубины дыхания в результате возникновения болевых ощущений (межреберная невралгия, миозит, сухой плеврит, переломы ребер), при высоком стоянии диафрагмы из-за повышения внутрибрюшного давления (метеоризм, асцит). Брадипноэ обычно наблюдается при поражении центальной нервной системы, нарушении функции дыхательного центра, при гипотиреозе, интоксикациях (почечная и печеночная недостаточность), прием наркотических и седативных препаратов. Изменения глубины дыхания. В физиологических условиях глубина дыхания определяется дыхательным объемом, который в среднем равен 500 – 800 мл. В патологии может наблюдаться гиперпноэ – глубокое и шумное дыхание. Классическим примером служит патологическое дыхание Куссмауля, возникающее при диабетическом кетоацидозе, отравлении метанолом, уремии. Гипопноэ – поверхностное дыхание может встречаться у тучных людей вследствие гиповентиляции (синдром Пиквика) и служить предвестником дыхательной недостаточности. Апноэ – отсутствие дыхания в течение 20 сек в бодрствующем состоянии или 30 сек во время сна. Может возникать при обструкции дыхательных путей во время сна или при поражении ЦНС. В любом случае, апноэ является конечным этапом дыхательной недостаточности. Нарушение ритма дыхания. Как уже подчеркивалось, нормальное дыхание характеризуется ритмичным чередованием одинаковых по глубине и продолжительности фаз вдоха и выдоха. Ритм дыхания чаще изменяется вследствие нарушения регуляции деятельности дыхательных мышц нервной системой. В большинстве случаев изменение ритма дыхания сопровождается нарушениями его частоты и глубины. Поражения центров регуляции процесса дыхания могут вызывать следующие виды патологического дыхания: – дыхание Чейн-Стокса характеризуется постепенным увеличением, а затем уменьшением амплитуды дыхательных движений и возникновением пауз (апноэ) продолжительностью до 1 минуты, встречается при тяжелых нарушениях мозгового кровообращения и интоксикациях; – дыхание Грокка напоминает дыхание Чейн-Стокса, но его отличительной особенностью является регистрация слабого поверхностного дыхания вместо пауз, возникает при тех же патологических процессах, что и дыхание Чейн-Стокса, только в более ранних стадиях; – дыхание Биотта характеризуется одинаковыми по амплитуде ритмическими глубокими дыхательными движениями, возникающими через одинаковые паузы (до 30 сек); – агональное дыхание имеет разные по глубине и продолжительности неритмичные дыхательные движения, наблюдается, как правило, в состоянии клинической смерти. Пальпация или ощупывание как метод исследования дополняет данные, полученные при осмотре. Этот метод требует хорошей профессиональной подготовки и знания анатомии и физио-логии человека. Пальпация позволяет в короткие сроки, уже при первом контакте с больным, выявить патологические изменения в различных органах, которые в дальнейшем можно уточнить, применяя современные инструментальные методы визуализации. Пальпация проводится в теплом помещении, с хорошим, желательно естественным освещением. Положение больного зависит от исследуемого органа и тяжести состояния. Факторы, влияющие на результат исследования: мышечное напряжение, болевые ощущения следует избегать. Исследователь занимает удобное для него положение, позволяющее с максимальной эффективностью использовать метод, основанный на знании опознавательных знаков и топографических линий грудной клетки. Проведение пальпации имеет следующие цели – определение резистентности грудной клетки, выявление болезненности в области грудной клетки, определение голосового дрожания. Резистентность или эластичность грудной клетки определяется путем ее сдавления ладонями рук в предне-заднем и боковом направлениях. То сопротивление грудной клетки, которое ощущает исследователь при пальпации и характеризует эластичность и резистентность. Увеличение резистентности и снижение эластичности грудной клетки встречаются при экссудативных плевритах, эмфиземе легких. Проведение пальпации позволяет выявить участки болезненности грудной клетки, ребер, грудины. Локальная болезненность наблюдается при переломе ребер и ушибе мягких тканей, а по ходу межреберий – при межреберной невралгии. Во время пальпации можно уточнить: Подвижность 1. и смещение трахеи – смещение трахеи книзу на вдохе, как правило, свидетельствует о хронической обструкции дыхательных путей, этот симптом выявляется, если кончик указательного пальца поместить на щитовидный хрящ во время вдоха. 2. Нарушения дыхательной экскурсии, асинхронность движения одной из половин грудной клетки; это возможно сделать с помощью следующего приема: врач находится сзади от больного, обхватывая ладонями с разведенными пальцами обе половины грудной клетки, противопоставив при этом большие пальцы, сначала больной делает глубокий выдох и ладони врача сжимают грудную клетку исследуемого, а затем вдох, по смещению больших пальцев кнаружи определяется симметричность движения обеих половин грудной клетки. 3. Форму грудной клетки. Кроме указанной информации при заболеваниях органов дыхания с помощью пальпации можно выявить увеличение лимфоузлов в над- и подключичных ямках, подмышечной впадине; участки крепитации при подкожной эмфиземе; шум трения плевры. Голосовое дрожание (fremitus pectoralis) это пальпируемая вибрация грудной клетки, обусловленная проведением голоса обследуемого. Пациент произносит слова, содержащие громкие согласные, и исследователь пальпаторно ощущает вибрацию грудной клетки. Непременным условием определения голосового дрожания является исследование его на симметричных участках. Любая патология на пути распространения звука изменяет его проведение, вследствие чего дрожание усиливается или ослабляется. Следует сказать, что для оценки голосового дрожания необходим достаточный навык и опыт. Физиологические различия голосового дрожания заключаются в том, что у детей и женщин оно слабее, чем у мужчин. Кроме того, в правой верхней части грудной клетки голосовое дрожание выражено сильнее из-за широкого и короткого главного бронха, а в нижних отделах слева – слабее. Ослабление голосового дрожания связано с возникновением препятствия для распространения звука и встречается при: – увеличении подкожно-жирового слоя; – синдромах гидро- и пневмоторакса; – наличии плевральных спаек и шварт; – синдроме обтурационного ателектаза; – пневмосклерозе и пневмофиброзе; – синдроме бронхиальной обструкции. Усиление голосового дрожания обусловлено улучшением проведения голоса и встречается при: – тонкой грудной клетке; – синдроме инфильтрата при пневмококковой пневмонии, так как уплотненная воспалительным экссудатом легочная ткань при сохраненной проходимости воздуха через бронхи, лучше передает звуки (следует заметить, что при сегментарных пневмониях, из-за вовлечения в процесс воспаления бронхов и образования в них слизистых пробок, голосовое дрожание ослабевает); – синдроме полости (из-за физического явления – резонанса); – синдроме компрессионного ателектаза в зоне уплотнения легочной ткани. Перкуссия (percussio) – это метод исследования, заключающийся в простукивании различных участков тела и оценки возникающих при этом звуков. Перкуссия как метод выстукивания была известна давно. Приоритет в разработке этого метода принадлежит австрийскому врачу Ауэнбругеру, который в 1761 году изложил его основы в своем трактате. Причем, в то время это был единственный физикальный способ исследования, позволявший при жизни выявить патологию внутренних органов у больных. В дальнейшем, метод в течение 50 лет был незаслуженно забыт и только в 19 веке, личный врач Наполеона Жан-Николь Корвизар ввел его как стандарт для диагностики заболеваний. Затем, в 1828 году французский врач Пиорри предложил плессиметр, сделанный из слоновой кости, а Уильям Стокс, Джеймс Хоун и Шкода разработали пальце пальцевую перкуссию и описали основные перкуторные тоны. В России данный метод исследования был внедрен известными клиницистами С.П. Боткиным, Г.А. Захарьиным, Г.И. Сокольским и Н.И. Коровщиковым, применявшего топографическую перкуссию разных органов. М.Г. Курлов разработал методику перкуссии сердца и печени. Образующийся при перкуссии звук зависит от строения ткани, расположенной в области выстукивания и характеризуется амплитудой, частотой и продолжительностью. Звуки по амплитуде бывают громкие и тихие, по частоте высокие или низкие, по продолжительности – длительные или короткие. Характеристики звука зависят от соотношения в исследуемом органе воздуха и плотной ткани. Чем больше воздушность органа, тем звук громче, ниже по частоте и более длительный за счет явления резонанса и, наоборот, при перкуссии плотных органов звук тихий, притупленный или тупой, высокий и короткий, за счет более быстрого затухания звуковых колебаний. В настоящее время принято выделять 3 основных перкуторных звука: 1. Ясный легочный звук, определяемый в норме над здоровыми легкими, он громкий, низкий, длительный и не тимпанический. 2. Бедренный звук, выявляемый в норме над плотными органами (мышцы, печень, сердце), он тихий, высокий, короткий и не тимпанический. 3. Тимпанический желудочно-кишечный) звук, определяемый над органами, содержащими большое количество воздуха и тонкие стенки (газовый пузырь желудка, кишечник), в норме он громкий, как правило, высокий и длительный. Перкуссия по способу применения бывает прямой (непосредственной) и непрямой (опосредованной). Данный метод разработал и начал применять Ауэнбругер во время работы в госпитале в Вене. Метод заключался в выстукивании грудной клетки плотно сомкнутыми кончиками пальцев. В дальнейшем этот способ был модифицирован Ф.Г. Яновским и В.П. Образцовым, которые использовали указательный и средний палец для перкуссии. При непрямой перкуссии, родоначальником которой был Пиорри, используется плессиметр и молоточек. В настоящее время общепринятой является пальце-пальцевая перкуссия, где плессиметром является 3 палец левой кисти, а молоточком – 3 палец правой кисти. Преимущество этого метода заключается в простоте, он удобен, не надо возить с собой инструментарий, который можно потерять. Кроме того, звук, образующийся при перкуссии более однородный. По силе перкуссия бывает громкой при исследовании глубоко расположенной патологии (в пределах 7-8 см), средней (5-6 см), тихой (3-4 см) и тишайшей (2-3 см). Выделяют сравнительную и топографическую перкуссию. Сравнительная перкуссия. Целью сравнительной перкуссии является выявление патологического очага в легких или плевральной полости путем сравнения перкуторного звука в симметричных участках грудной клетки. Для этого используются следующие правила: – сравнения перкуторного звука проводят только в симметричных участках правой и левой половин грудной клетки; сила перкуторного – тона громкая или средняя в зависимости от расположения патологического очага; – перкуссия проводится в строго определенном порядке; – удар пальцем-молоточком наносится в ямках по концевой фаланге пальца плессиметра, в межреберьях – по средней; – перкуссия проводится при спокойном и глубоком дыхании больного; – сначала проводят перкуссию по передней поверхности грудной клетки, затем по боковой и задней, двигаясь сверху вниз; – перкуссию выполняют спереди и сбоку справа налево, сзади – слева направо.
В норме над легкими при сравнительной перкуссии выслушивается ясный легочный тон. Однако, в некоторых случаях, возможны физиологические изменения перкуторного звука: над верхушкой – правого легкого из-за значительного развития мышц плечевого пояса; – справа в нижней части подмышечной области перкуторный звук несколько короче из-за расположенной рядом печени, а слева в нижней доле по передней подмышечной линии имеет тимпанический оттенок из-за газового пузыря в желудке. При развитии патологического процесса в легких и плевре перкуторный звук может измениться. Притупление перкуторного звука определяется при уменьшении воздушности легочной ткани и появлении плотных участков при сегментарной пневмонии, пневмосклерозе, опухоли легкого, наличии плевральных спаек и шварт. Тупой звук наблюдается при пневмококковой пневмонии, синдроме гидроторакса (скоплении жидкости в плевральной полости), синдроме обтурационного ателектаза, при наличии опухоли значительных размеров, при выраженном утолщении плевральных листков и развитии мощного спаечного процесса, при абсцессе легких или туберкулезной каверне до опорожнения. Притупленно-тимпанический тон определяется в случаях, когда на фоне небольшого уплотнения легочной ткани остается небольшое количество воздуха при одновременном снижении эластичности альвеол. Это встречается при пневмосклерозе, долевой пневмонии в 1 и 3 стадиях, при компрессионном ателектазе (тон Шкоды), отеке легких в начальной стадии. Тимпанический звук определяется при: синдроме пневмоторакса (скоплении воздуха в плевральной полости), наличии полости, сообщающейся с бронхом, туберкулезной каверне и абсцессе легких в стадии опорожнения, крупном бронхоэктазе. При наличии крупной гладкостенной полости (6-8 см), расположенной поверхностно, тимпанический звук имеет «металлический» оттенок. Он более низкий и напоминает удар по металлу. Если поверхностно расположенная крупная полость сообщается с бронхом узким отверстием, то при перкуссии над ней тимпанический звук напоминает звук «треснувшего горшка». Коробочный звук возникает при синдромах бронхиальной обструкции и эмфиземы легких: при диффузном увеличении воздушности легочной ткани при одновременном снижении эластичности альвеол. Он имитирует звук, возникающий при ударе по спичечному коробку или подушке. Топографическая перкуссия. Целью топографической перкуссии является определение верхних и нижних границ легких, а также экскурсии нижних краев легких по основным топографическим линиям. Правила перкуссии: – проводят тихую перкуссию; – перкуссию проводят по ребрам и межреберьям; – палец-плессиметр должен передвигаться параллельно определяемой границе от легочного звука в сторону тупого справа и слева; – границу легкого определяют по стороне пальца, обращенной в сторону ясного легочного звука; – применяется отскакивающая перкуссия. Практическое значение имеет определение нижней границы легких по основным топографическим линиям справа и слева. Палец-плессиметр располагают во 2 межреберье и направляют вниз параллельно ребрам. Перкутируют по средней фаланге по межреберьям тихой перкуссией до притупления легочного звука. Отметка границы производится по стороне пальца плессиметра, обращенного в сторону ясного легочного звука. При косом расположении ребер и межреберьев концевая фаланга плессиметра справа обращена книзу, а слева – кверху. Следует знать, что по лопаточной линии перкуссию начинают от угла лопатки. Необходимо помнить при этом, что нижний угол лопаток прикрывает 7 ребро.
Аускультация (auscultatio) – метод исследования звуковых явлений, возникающих при их выслушивании. Этот метод известен очень давно и описан около 1800 лет до н.э. Он также был известен Гиппократу, который пользовался прямой, непосредственной аускультацией ухом. В дальнейшем этом метод упоминался Леонардо Да Винчи, Уильямом Гарвеем. Впервые более подробно описал метод аускультации в 1819 году в 2-х томном труде Рене Лаэннек, который первый предложил стетоскоп (перевод с греческого – инспектор грудной клетки). В дальнейшем в 1854 году в Нью-Йорке он был усовершенствован Калманом и в России Н.Ф. Филатовым в бинауральный. Лаэннек также впервые ввел в терминологию такие слова как аускультация, хрипы, голосовое дрожание, бронхофония, ослабленное дыхание и другие. Фонендоскоп, отличающийся от стетоскопа наличием мембраны, которая с одной стороны усиливает звук, а с другой может его искажать за счет собственных колебаний, был изобретен и изучен Шкодой, А.А. Остроумовым, В.П. Образцовым и другими. Развитию аускультации в России также способствовали известные врачи М.Я Мудров, С.П. Боткин, Н.Д. Стражеско. Аускультация с применением стетоскопа и фонендоскопа относится к непрямым, опосредованным методам и в отличие от прямого метода имеет ряд преимуществ: метода имеет ряд преимуществ: 1. Более громкий звук при аускультации. 2. Метод более гигиеничен. 3. Позволяет выслушивать в различных точках грудной клетки. При аускультации легких сначала при спокойном вдохе и выдохе выслушивают основные дыхательные шумы, а затем дополнительные или побочные; для уточнения побочных шумов можно использовать следующие приемы: попросить больного сделать глубокий вдох или выдох, задержать дыхание, покашлять, изменить положение тела. К основным дыхательным шумам относят везикулярное и ларинго-трахеальное. Ларинго-трахеальное (бронхиальное) дыхание. Это громкий, высокочастотный и грубый шум, возникающий при прохождении воздуха через гортань, голосовую щель и верхнюю часть трахеи, образуя при этом турбулентный поток. Он напоминает звук «Х», если произносить эту букву открытым ртом. Ларинготрахеальное дыхание лучше всего выслушивается над гортанью и трахеей: спереди в яремной ямке, сзади на уровне VII шейного позвонка и смещается вниз до III-IV грудных позвонков. Соотношение фаз вдоха и выдоха составляет 4:5. Возникший в трахее и бронхах шум распространяется вверх и вниз. Распространяясь вверх, он содержит весь спектр частот и поэтому слышится громким (аускультация в области шеи). Распространяясь вниз, через легкие на грудную клетку, его интенсивность снижается, так как воздух, содержащийся в альвеолах, работает как высокочастотный фильтр и удаляет шумы с частотой более 200 ГЦ, которые в основном и воспринимает человеческое ухо. В связи с этим, при уплотнении легких создаются условия для лучшего проведения шума, при повышении воздушности (снижении эластических свойств альвеол) громкость шума уменьшается. Везикулярное дыхание (альвеолярное, нормальный дыхательный шум). Это ясный дующий шум, напоминающий звук при произношении буквы «Ф» и связанный с колебаниями стенок альвеол, обеспечивающих определенную воздушность легочной ткани. Шум выслушивается на протяжении всего вдоха и в первую треть выдоха. В последние две трети выдоха шум исчезает, так как колебанием альвеол он значительно уменьшается и практически не слышен. Между вдохом и выдохом нет паузы. Отношение вдоха к выдоху составляет 5:3. Шум лучше всего выслушивается в областях, где наибольшее количество альвеол – подмышечной, подключичной и подлопаточной. Основные изменения везикулярного дыхания. Ослабление везикулярного дыхания, которое связано с уменьшением продолжительности и интенсивности фаз вдоха и выдоха. Причинами ослабления везикулярного дыхания являются: 1. Физиологические: – чрезмерное развитие мышечной массы и подкожно-жирового слоя в области грудной клетки; – над верхушкой легких, так как в этом участке масса альвеол меньше. 2. Патологические: – Внелегочные: а) образование препятствия в верхних дыхательных путях при сужении гортани, трахеи, попадании инородного тела, злокачественные новообразования; б) уменьшение подвижности грудной клетки, высоком стоянии диафрагмы при ожирении, возникновении боли при межреберной невралгии, травмах и переломах ребер, снижении функциональной активности дыхательных мышц. – Плевральные причины: а) синдром гидроторакса (скопление в плевральной полости жидкости воспалительного и невоспалительного характера, либо крови – гемоторакс); б) синдром пневмоторакса (скопление воздуха в плевральной полости); в) утолщение листков плевры и развитие спаек между их листками; г) сухой плеврит, при котором ограничивается дыхание из-за возникновения болевых ощущений. – Бронхиальные причины: а) синдром обтурационного ателектаза – спадение сегмента или доли легкого в результате закрытия просвета соответствующего бронха инородным телом, опухолью; б) синдром бронхиальной обструкции, при котором увеличивается воздушность легочной ткани и снижаются высокочастотные колебания стенок альвеол, что приводит к уменьшению интенсивности дыхательного шума. – Легочные причины: а) синдром эмфиземы легких, при котором происходит увеличение воздушности легочной ткани вследствие уменьшения эластических свойств альвеол; б) при утолщении стенок альвеол в результате воспаления (начальная стадия пневмококковой пневмонии) или при нарушении гемодинамики (начинающийся отек легких); в) уменьшение массы альвеол вследствие развития опухоли, пневмосклеротического процесса. Соотношение фаз вдоха и выдоха при ослабленном везикулярном дыхании соответствует 2:1. Усиление везикулярного дыхания характеризуется усилением вдоха и выдоха без изменения их соотношения.
Физиологическими причинами усиления везикулярного дыхания являются: а) тонкая грудная клетка; б) значительные физические нагрузки, способствующие гипервентиляции и увеличению амплитуды колебания стенок альвеол. – Патологическими причинами являются: а) гипертиреоз; б) гипервентиляция, развивающаяся на противоположной от патологического процесса части легких при пневмококковой пневмонии, пневмотораксе, экссудативном плеврите. К разновидностям усиленного везикулярного дыхания относят: пуэрильное, саккадированное, жесткое. Пуэрильное дыхание впервые описал Рене Лаэннек, который отметил, что у детей интенсивность шума выше. Это более громкое, но нежное дыхание. Соотношение фазы вдоха и выдоха 5:5. Причинами увеличения интенсивности дыхания считаются: а) резонансные свойства «маленькой» грудной клетки; б) меньший радиус воздухоносных путей, увеличение скорости воздушного потока, что приводит к большей громкости. Жесткое дыхание возникает в связи с появлением вихревого воздушного потока, вследствие сужения просвета бронха в результате скопления секрета, утолщении стенок, бронхоспазма. Увеличивается интенсивность и звучность обеих фаз дыхания с небольшим удлинением выдоха. Соотношение фаз вдоха и выдоха составляет 5:4. Саккадированное (прерывистое) дыхание. Для него характерно прерывистый через одинаковые паузы вдох при неизмененном выдохе. Причинами являются заболевания дыхательных мышц, переохлаждение, нарушение проходимости мелких бронхов и неодновременное расправление альвеол при воспалительном и туберкулезном процессах.
Патологическое бронхиальное дыхание. При создании условий для улучшения проведения дыхательного шума из трахеи и бронхов и при сохранной проходимости бронхов, в области, где обычно выслушивается везикулярное дыхание, можно выслушать бронхиальное. Это дыхание называется патологическим бронхиальным. Причинами появления патологического бронхиального дыхания являются: 1. Уплотнение легочной ткани при: – пневмококковой пневмонии (за счет экссудата). 2. Синдром компрессионного ателектаза, в результате чего происходит спадение и уплотнение альвеол большим количеством жидкости в плевральной полости. 3. При наличии полостей в легких: туберкулезная каверна, абсцесс легких или эхинококковая киста после опорожнения. Это происходит за счет сохранения проведения воздуха через бронхи, уплотнения вокруг полости и явления резонанса (усиление звука). При определенных условиях бронхиальное дыхание может приобретать металлический оттенок, например, при развитии пневмоторакса, когда возникает сообщение бронхов с плевральной полостью (напоминает удар по металлу). Иногда возникает амфорическое дыхание. Оно громкое за счет хорошего резонанса и выслушивается при движении воздуха по полостям (синдром полости), сообщающихся с бронхами. Это дыхание напоминает звук как при вдувании воздуха в пустой сосуд с узким горлышком. Побочные (дополнительные) дыхательные шумы. К ним относятся хрипы, крепитация и шум трения плевры. Появляются они только в патологии, наслаиваясь при этом на основные дыхательные шумы. Хрипы (ronchi). Этот термин принадлежит Рене Лаэннеку, который считал их шумами, не похожими на везикулярное и бронхиальное дыхание. Согласно общепринятой классификации в России, принято делить хрипы на влажные и сухие, а согласно международной классификации (1977) они делятся на кратковременные (<250мс) и продолжительные (>250мс). Влажные хрипы. Механизм их возникновения связан с прохождением потока воздуха через жидкий секрет, содержащийся в трахее, бронхах или полостях легких и возникновением в результате этого пузырьков, которые лопаясь, издают звук напоминающий «треск» или «потрескивание» (crackles). Влажные хрипы выслушиваются в обе фазы дыхания, но больше выражены на вдохе. В зависимости от калибра бронха или полости они подразделяются на: – крупнопузырчатые; – среднепузырчатые; – мелкопузырчатые; – субкрепитирующие. Крупнопузырчатые влажные хрипы это громкие, «взрывоподобные» низкочастотные хрипы, возникающие в трахее, бронхах крупного калибра или полостях диаметром не менее 5-6см и сообщающихся с бронхом. Они выслушиваются при абсцессе в стадию опорожнения, туберкулезной каверне, отеке легких, при наличии крупных бронхоэктазов. Среднепузырчатые влажные хрипы образуются в бронхах среднего калибра (сегментарных) при бронхоэктатической болезни, острой левожелудочковой недостаточности, хроническом бронхите. Мелкопузырчатые влажные хрипы возникают в мелких бронхах при хронической сердечной недостаточности, пневмонии, невмофиброзе, хроническом бронхите. Они более тихие, высокочастотные и обильные. Субкрепитирующие влажные хрипы возникают в мельчайших бронхах при бронхиолитах, сегментарной пневмонии. Их трудно отличить от крепитации, поэтому в ряде литературы они не выделяются отдельно. При наличии уплотнения легочной ткани вокруг бронхов, обладающей лучшей проводимостью, или полостей, создающих эффект резонанса, хрипы становятся более громкими, звучными, консонирующими. Это наблюдается при пневмонии, инфильтративном и кавернозном туберкулезе. Если легочная ткань не потеряла воздушность, то интенсивность хрипов, возникающих u1074 {в бронхах уменьшается и они становятся более тихие, незвучные, неконсонирующие. Это встречается при отеке легких, бронхитах. Сухие хрипы. Сухие хрипы образуются в результате поражения трахеи и бронхов различного калибра и подразделяются на свистящие (ronchi sibilantes) и жужжащие (ronchi sonori). Свистящие хрипы это продолжительные (>250 мс), высокие, дискантовые и возникают в результате сужения просвета мелких и мельчайших бронхов при отеке слизистой оболочки, спазме гладкой мускулатуры или скоплении в просвете бронхов секрета. Это приводит к ускорению движения воздушных потоков через суженные воздухоносные пути, вызывая при этом вибрацию стенок бронхов (эффект Бернулли) и появление свистящих хрипов. При значительном ускорении движения воздуха через мелкие бронхи, например при форсированном выдохе, свистящие хрипы выслушиваются гораздо лучше. Причинами появления сухих свистящих хрипов является бронхообструктивный синдром, встречающийся при бронхиальной астме, остром и хроническом бронхитах, бронхиолите. Во время приступа бронхиальной астмы их можно услышать на расстоянии. Сухие свистящие хрипы выслушиваются в обе фазы дыхания, но преимущественно на выдохе и ослабевают или исчезают при покашливании. Сухие жужжащие хрипы – продолжительные, низкие, басовые, возникают в результате скопления вязкого секрета в просвете крупных воздухоносных путей в виде нитей, колебание которых и сопровождается появлением «гудящих» звуков. Они также выслушиваются как на вдохе, так и на выдохе, и изменяются после кашля. Жужжащие хрипы могут выслушиваться при бронхитах, бронхоэктатической болезни, пневмосклерозе. Крепитация (crepitatio). Это звуковое явление, которое возникает на высоте вдоха при наличии небольшого секрета в спавшихся альвеолах. В результате поступления воздуха в альвеолы, происходит их разлипание и возникает звук, напоминающий, как писал Лаэннек, «хруст соли на нагретой сковородке» или трение волос над ухом. Крепитация может встречаться у здоровых пожилых лиц и ослабленных больных в нижних отделах по задней поверхности грудной клетки и исчезать после первых глубоких вдохов. В патологии крепитацию можно выслушать в начальной и конечной стадии пневмококковой пневмонии, при синдроме компрессионного ателектаза, хронической сердечной недостаточности. Большое диагностическое значение имеет отличие крепитации от влажных хрипов: 1. Влажные хрипы изменчивы, так как могут усиливаться или ослабевать при кашле, а крепитация нет. 2. Влажные хрипы выслушиваются в обе фазы дыхания, а крепитация только на высоте вдоха. Шум трения плевры. Это грубый громкий с преобладанием низкочастотного компонента шум, возникающий в результате трения неровных (шероховатых) листков плевры друг о друга. В норме, из-за наличия определенного количества жидкости в плевральной полости, этого трения не возникает и шума нет. В патологии он обычно возникает при сухости листков плевры (обезвоживание), при отложении нитей фибрина (сухой плеврит, плевропневмония), при образовании туберкулезных бугорков на поверхности плевры, азотистых шлаков (хроническая почечная недостаточность), при спаечном процессе и коллагенозах. Аускультативными свойствами шума трения плевры являются: 1. Выслушивается в обе фазы дыхания, но преимущественно на вдохе, так как в эту фазу движения листков плевры сильнее. 2. Не изменяется при кашле. 3. Выслушивается, как правило, локально, в области пораженного участка, чаще в нижне-задних отделах. 4. Громкий, обычно длительный и низкочастотный, напоминающий «хруст снега» или «шорох бумаги». 5. Иногда может пальпироваться. 6. Может усиливаться при надавливании стетофонендоскопом из-за сближения и усиления трения листков плевры. 7. Может сопровождаться болевыми ощущениями. 8. Изменяется в динамике: при появлении жидкости в плевральной полости исчезает, так как трение листков плевры прекращается.
В практике очень важно отличать шум трения плевры от влажных хрипов и крепитации. Признаками отличия от влажных хрипов являются: – шум трения плевры после кашля не изменяется, а хрипы могут изменяться или ослабевать; – шум трения плевры более продолжительный по времени; – более громкий и низкочастотный; – может ощущаться при пальпации, а влажные хрипы нет; – усиливаются при надавливании фонендоскопом, а влажные хрипы нет; – сохраняются в пробе с имитацией дыхания: при закрытых ротовой и носовой полостях больного просят совершать движения передней брюшной стенкой. Шум трения плевры слышен, а хрипы исчезают. Гораздо проще отличить шум трения плевры от сухих свистящих хрипов по следующим признакам: – шум трения плевры лучше выслушивается на вдохе, а свистящие хрипы во время выдоха, особенно форсированном; – не изменяется при кашле, а хрипы непостоянны; усиливаются – при надавливании фонендоскопом, а хрипы нет; – шум трения плевры грубый и низкочастотный, а свистящие хрипы высокочастотные; – выслушивается в пробе с имитацией дыхания, а хрипы – нет. Отличия шума трения плевры от крепитации: – выслушивается в обе фазы дыхания, а крепитация на высоте вдоха; – может сопровождаться болевыми ощущениями, а крепитация нет; – может пальпироваться, а крепитация нет; – усиливается при надавливании фонендоскопом, а крепитация нет; – не исчезает в пробе с имитацией дыхания, а крепитация отсутствует; – выслушивается только в патологии, а крепитация может и в норме. В редких случаях приходится отличать шум трения плевры от шума трения перикарда. Различием является исчезновение шума трения плевры при задержке дыхания. Бронхофония (шум бронхов в переводе с греческого). Данное исследование является заключительным этапом аускультации. Она представляет собой звуковые колебания, возникающие в гортани и распространяющиеся через бронхи и легочную ткань на переднюю, боковые и заднюю поверхности грудной клетки при тихой и шепотной речи. Диагностируется бронхофония с помощью фонэндоскопа, который прикладывается на симметричные участки грудной клетки (как и голосовое дрожание), в точках сравнительной перкуссии. В норме воздух, содержащийся в альвеолах, снижает количество высокочастотных звуков, содержащихся в основном в гласных буквах, что делает их, а вместе с ними и целое слово непонятным и нераспознающимся, одинаково выслушиваемое в симметричных участках грудной клетки. В патологии бронхофония может усиливаться, что приводит к тому, что слова становятся ясными и хорошо различимыми и ослабевать или даже не выслушиваться. Причиной усиления бронхофонии является улучшение проводимости звука через легочную ткань при: 1. Синдроме уплотнения легочной ткани (пневмококковая пневмония II стадия, туберкулезный инфильтрат). Иногда при этом возникает феномен «Е на А», описанный Шестли в 1922 году и выражающийся в том, что при произношении буквы Е слышится буква А из-за улучшения проводимости звука, но не высокочастотного, характерного для Е. 2. Синдроме компрессионного ателектаза (над областью поджатого легкого). 3.Синдроме полости, вследствие эффекта резонанса (абсцесс в стадии опорожнения, туберкулезная каверна, «сухие» и крупные бронхоэктазы). Важно также заметить, что усиление бронхофонии сочетается с усилением голосового дрожания и появлением бронхиального дыхания. Причинами ослабления бронхофонии являются: 1. Внелегочные: – утолщение грудной клетки; – избыточное развитие подкожно-жирового слоя. 2. Плевральные: – синдром гидро- и пневмоторакса; – образование массивных спаек и шварт. 3. Легочные: – синдром эмфиземы легких, из-за повышения воздушности легочной ткани и преобладания неразборчивых низкочастотных звуков; – синдром обтурационного ателектаза; – синдром бронхиальной обструкции. Пневмония (от греческого pneumon - легкие) - заболевание, объединяющее группу различных по этиологии, патогенезу и морфологической характеристике воспалительных процессов, основным патологическим субстратом, которого является экссудативное, чаще инфекционной природы воспаление легочной ткани с преимущественным поражением ее респираторных отделов. Пневмония как нозологическая форма включает лишь те случаи, когда возбудителем является патогенная или условно патогенная флора, а главным механизмом заболевания - прорыв естественных механизмов защиты. Другие воспалительные заболевания легочной паренхимы, обусловленные разнообразными факторами внешней среды (неинфекционной природы) или возникающие вследствие повышенной чувствительности (аллергические реакции), называют обычно пневмонитами или альвеолитами и исключают из группы пневмоний.
ЭТИОЛОГИЯ. Международная классификация болезней предусматривает дефиницию пневмоний исключительно по этиологическому принципу. Выяснение этиологии пневмоний, несомненно улучшает лечение больных, а значительное количество неудач обусловлено именно незнанием возбудителя. Пневмонию могут вызвать практически все известные на сегодняшний день инфекционные агенты. Этиология пневмоний непосредственным образом связана с нормальной микрофлорой “нестерильных” отделов верхних дыхательных путей (полостей рта, носа, рото- и носоглотки). Однако на практике в подавляющем большинстве случаев возбудителями пневмонии является сравнительно ограниченное количество видов микроорганизмов. Типичными возбудителями пневмоний являются: · Streptococcus pneumoniae - грамположительные кокки, которые являются ведущим этиологическим фактором ОП. Удельный вес пневмококковых ОП составляет 80-90%. Этиологическая диагностика возбудителя ОП по данным секционного материала показывает, что в 60% случаев возбудителем является пневмококк. · Haemophilus influenzae - грамотрицательные палочки, ответственные за развитие пневмонии у 5-18% взрослых, чаще у курильщиков и больных хроническим обструктивным бронхитом. · Moraxella (Branhamella) catarralis - грамотрицательныее коккобациллы, имеет этиологическое значение, как правило, у больных с сопутствующим хроническим обструктивным бронхитом. · Mycoplasma pneumoniae - микроорганизм, лишенный внешней мембраны, что обусловливает его природную устойчивость к бета-лактамным антибиотикам. Вызывает пневмонию у 20-30% лиц моложе 35 лет. · Chlamidia pneumoniae - микроорганизм, являющийся исключительно внутриклеточным паразитом. Вызывает пневмонию в 2-8% случаев. · Legionella pneumophila - легионеллезная пневмония занимает второе место (после пневмококковой) по частоте смертельных исходов. Ряд микроорганизмов в норме редко встречается в составе микрофлоры верхних дыхательных путей. Частота их обнаружения, а соответственно, и роль в этиологии пневмоний несколько увеличивается у лиц старших возрастных групп с сопутствующими хроническими заболеваниями и другими факторами риска развития пневмоний. К таким микроорганизмам относятся: · Echerichia coli, Klebsiella pneumonia - являются причиной развития пневмонии, как правило, у больных с сопутствующими заболеваниями (сахарный диабет, застойная сердечная недостаточность, почечная, печеночная недостаточность). · Staphylococcus aures - возбудитель пневмонии у больных с известными факторами риска - пожилой возраст, наркомания, хронический гемодиализ, грипп. Этиологический спектр пневмоний за последние 15-20 лет существенно расширился. Наряду с известными пневмотропными возбудителями появились и новые, которые значительно видоизменили традиционные клинико-эпидемиологические представления о пневмонии. Эпидемиологическая ситуация 80-90-х годов характеризуется возросшей этиологической значимостью таких возбудителей как микоплазма, легионеллы, хламидии, пневмоцисты и значительным ростом резистентности стафилококков, пневмококков, стрептококков, гемофильных палочек, моракселлы к наиболее широко применяемым антибиотикам. Частота микоплазменных и хламидийных пневмоний изменяется в зависимости от эпидемиологической ситуации. Микоплазменной, легионеллезной и хламидийной инфекциям более подвержены молодые люди. По данным А.Г. Чучалина (1991), из 349 этиологически расшифрованных случаев острой пневмонии бактериальные агенты и их маркеры были обнаружены у 84,5% больных, микоплазма - у 10%, вирусы - у 8%. Из бактериальных агентов чаще обнаруживались пневмококк (60%), стрептококк (15%), гемофильная палочка (15%); реже выявлялись легионелла (2%), клебсиелла (1,5%), стафилококки (0,5%), энтеробактерии (0,3%), протей (0,15%). Существует определенная связь между возрастом больных и этиологией пневмонии. У лиц молодого возраста пневмонии чаще вызываются монокультурой возбудителя (обычно пневмококк), а у пожилых - ассоциацией бактерий, из которых достоверно преобладает ассоциации пневмококков с гемофильной палочкой (до 18%) и стрептококкоками (до 11%). Ассоциации, состоящие исключительно из грамположительных микроорганизмов встречаются в три раза реже, чем ассоциации грамположительной и грамотрицательной микрофлоры Этиологическая структура современных ОП представляется следующим образом: 44% - это вирусно-бактериальные пневмонии, 29% - бактериальные, вирусные - 7% и доля вирусно-микоплазменных - бактериальных ОП составляет 8%. В настоящее время большинство ОП (в 69% случаев) возникает на фоне ОРВИ. Большинство авторов рассматривает вирусную инфекцию как предрасполагающий фактор для последующей бактериальной инфекции. Несмотря на рост числа вирусно-бактериальных пневмоний, по данным современных эпидемиологических исследований ведущими возбудителями в этиологической структуре пневмоний являются пневмококки, микоплазма, легионелла и хламидии, на долю которых приходится около 90% всех случаев пневмонии.
КЛАССИФИКАЦИЯ. Важное значение в диагностическом процессе принадлежит классификационным схемам. Классификации ОП можно разделить на этиологические, патогенетические, клинико-морфологические и синтетические. Этиологический принцип построения классификации был предложен Bullowa. В международной классификации болезней Х пересмотра представлено разделение пневмоний в зависимости от этиологического фактора, и именно это позволяет говорить о нозологической самостоятельности пневмонии. Установление диагноза ОП без этиологического подтверждения приравнивается к синдромному диагнозу. Нозологическим диагноз становится после установления возбудителя. Трудности этиологической расшифровки обусловлены в первую очередь большим разнообразием микроорганизмов, способных вызвать пневмонию. Бактерии, грибы, хламидии, микоплазмы, риккетсии, вирусы, простейшие - все они требуют различных приемов для идентификации. Большое значение имеет выбор материала для поиска возбудителя. Для установления возбудителя традиционно проводят бактериологическое исследование мокроты. Количественная оценка микрофлоры считается необходимой, так как диагностически значимыми являются концентрации более 1 млн. микробных тел в 1 мл мокроты, а для грибов - более 10 000 Достоверность микробиологического исследования увеличивается, если от получения мокроты до ее посева на среду прошло не более 2 часов и предварительно произведено полоскание полости рта 2% раствором соды. В то же время нельзя забывать, что микроорганизмы, обнаруженные в мокроте не всегда являются истинными возбудителями болезни. Так показано, что у 35-70% здоровых лиц в ротоглотке содержатся пневмококки, у 5 - 50% - золотистый стафилококк, у 25-85% - палочка инфлюэнцы. Поэтому прибегают к специальным способам получения “чистой” мокроты (например, только после повторного “глубокого” откашливания или путем транстрахеальной пункции с введением в бронх катетера). Результаты бактериологического исследования могут быть искажены предшествующей антибактериальной терапией. К сожалению, чаще всего исследование проводится на фоне лечения или после безуспешной антибактериальной терапии и из мокроты выделяются микроорганизмы, не имеющие отношения к этиологии пневмонии. Достаточно широко применяется в клинической практике исследование бронхиальной лаважной жидкости, получаемой в ходе бронхоскопического исследования и специально защищаемой от бактериального загрязнения. Микрофлора бронхиального секрета, полученного при бронхоскопии, наиболее точно отражает этиологию заболевания. Для установления этиологического фактора пневмонии возможно исследование гемокультуры, которая является наиболее существенным доказательством, однако она может быть получена только при пневмониях, протекающих с бактериемией. Частота получения гемокультур при посевах крови на стерильность выше, если забор крови осуществляют во время озноба и посевы проводят неоднократно. Проводимая до забора крови антибактериальная терапия снижает вероятность получения положительного ответа. Основным недостатком этого метода является длительность исследования - результат бывает готов лишь к 10 дню. Не следует пренебрегать и ориентировочным методом, доступным любому лечебному учреждению - микроскопией мазка мокроты, окрашенного по Граму. Естественно, что этот метод следует применять до начала антибактериальной терапии. При бактерископии в мазке мокроты можно дифференцировать пневмококки, стрептококки, стафилококки, гемофильные палочки и, как минимум, определить преобладание в мокроте грамположительной или грамотрицательной флоры, что собственно и имеет значение для выбора антибиотика первого ряда. Таким образом, оптимальная схема бактериологической диагностики пневмонии должна включать посев бронхиального секрета и крови больного, использование исследование мокроты с предварительной бактериоскопией мазков, окрашенных по Граму (рис.1).
Посев Рис.1. Схема бактериологического обследования при пневмонии. Проводимое лечение почти не влияет на результаты так называемых некультуральных методов выявления этиологического фактора пневмонии. Под некультуральными методами понимают определение в сыворотке крови антигенов возбудителей и специфических антител к ним с помощью реакции непрямой иммунофлюоресценции (РНИФ) или реакции связывания комплемента (РСК). Выявление антигенемии считается одним из самых точных методов этиологического диагноза. При оценке титров специфических антител доказательна 4-х кратная сероконверсия, то есть увеличение титров антител в 4 раза в парных сыворотках, взятых с интервалом в 10-14 дней. Следовательно серотипирование также имеет существенный недостаток, так как позволяет установить этиологический диагноз только ретроспективно. К экспресс-методам относится определение антигенов в мокроте, мазке со слизистых методом прямой иммунофлюорисценции. Перспективным представляется в будущем использование для этиологический расшифровки пневмонии полимеразной цепной реакции. Таким образом, этиологическую оценку ОП следует проводит комплексно с использованием разнообразных методов исследования, среди которых должны быть не только доказательства присутствия микробного агента, но и данные, характеризующие реакцию организма на микробный агент. Использование этиологической классификации в клинике затруднено еще и тем, что этиологический диагноз, основанный на данных микробиологического и серологического методов исследования - это в большинстве случаев ретроспективный диагноз уже купированного инфекционного процесса. В основе патогенетических классификаций лежит деление пневмоний на первичные и вторичные с дальнейшим подразделением: а) по синдромам, послужившим фоном для развития пневмонии; б) по путям проникновения микробов в легкие. Основные принципы клинико-морфологических или анатомических классификаций ОП: 1) по протяженности - лобарные, очаговые, сегментарные, лобулярные 2) по преимущественному поражению того или иного отдела бронхолегочного аппарата - плевропневмонии, бронхопневмонии, паренхиматозные и интерстициальные пневмонии. 3) по характеристике воспалительного процесса - крупозные, катаральные. Таким образом, наиболее перспективны синтетические классификации ОП, которые должны отражать следующие характеристики воспалительного процесса; · характер возбудителя; · патогенетический вариант; · клинико-морфологическую форму, которая устанавливается по особенностям физикальных и рентгенологических проявлений. И такая классификация в нашей стране была создана Н.С. Молчановым (1962), а в дальнейшем дополнена и уточнена О.В. Коровиной (1978) (таб.1). Изменение клинической картины пневмоний в наши дни закономерно обусловило и пересмотр общепринятых классификаций 70-80-х годов. Однако следует иметь в виду, что этиологический принцип деления пневмоний, положенный в основу международной классификации, является принципиально самым правильным, но следует признать, что и в начале ХХ1 века этиологическая расшифровка пневмоний при первом контакте с пациентом невозможна из-за недостаточной информативности и длительности традиционных микробиологических исследований. В соответствии с этим альтернативной является классификация, в которой учтены те условия, в которых развилось заболевание, некоторые особенности инфицирования легочной ткани. Таблица 1. Классификация острых пневмоний по О.В. Коровиной (1978)
При правильном учете перечисленных факторов можно со значительной долей вероятности установить этиологию заболевания. В соответствии с этой классификацией в настоящее время для практических целей повсеместное распространение получило разделение пневмоний на следующие виды пневмоний: · внебольничные - community-acquired pneumonia (приобретенная вне лечебного учреждения пневмония). Синонимы: домашняя, амбулаторная. · внутрибольничные - nosocomial pneumonia (приобретенная в лечебном учреждении пневмония). Синонимы: нозокомиальная, госпитальная. В этих двух больших группах выделяют еще аспирационные и так называемые атипичные пневмонии, а также пневмонии у больных с нейтропениями и/или на фоне различных иммунодефицитов. Столь условное деление пневмоний тем не менее является оправданным потому, что различаются их этиологические агенты. Существенно, что врач может оценить клиническую ситуацию (эпидемиологические и клинические особенности, предшествовавшие заболеванию, факторы риска) значительно раньше, чем будут получены лабораторные данные об этиологическом факторе. Суждение о месте развития пневмонии врач может вынести незамедлительно после сбора анамнеза, а следовательно, и более обоснованно подойти к выбору антибактериального препарата.
ПАТОГЕНЕЗ. Отечественные клиницисты издавна считали, что возникновение, течение и исход пневмонии зависит как от вирулентности возбудителя, так и от выраженности реакции макроорганизма на инфекцию. Противоинфекционную защиту нижних дыхательных путей осуществляют механические факторы, а также механизмы неспецифического и специфического иммунитета, которые подразделяют на клеточные и гуморальные. Причинами развития воспалительной реакции в респираторных отделах легких могут быть как снижение эффективности защитных механизмов макроорганизма, так и массивность дозы микроорганизмов или их повышенная вирулентность. Принципиально можно выделить четыре патогенетических механизма развития пневмонии: · аспирация секрета ротоглотки · вдыхание аэрозоля, содержащего микроорганизмы · гематогенное распространение из внелегочного очага · непосредственное распространение инфекции из соседних пораженных тканей. Аспирация содержимого ротоглотки является основным путем инфицирования респираторных отделов легких, а значит, и основным патогенетическим механизмом развития пневмонии, как внебольничной, так и госпитальной. Микроаспирация секрета ротоглотки - физиологический феномен, наблюдающийся у 70% здоровых индивидов во время сна. Однако в нормальных условиях кашлевой рефлекс, отлаженный механизм мукоцилиарного клиренса, антибактериальная активность альвеолярных макрофагов и секреторных иммуноглобулинов обеспечивают элиминацию инфицированного секрета из нижних дыхательных путей. В случае же повреждения механизмов “самоочищения” трахеобронхиального дерева, при нарушении функции ресничек эпителия бронхов, снижении фагоцитарной активности альвеолярных макрофагов создаются благоприятные условия для развития пневмонии. Микроорганизмы могут проникать в легкие и вызывать пневмонию при ингаляции возбудителей, содержащихся в воздухе. Более 80 кв.м. дыхательного эпителия ежедневно контактирует с 107000 л вдыхаемого воздуха и вероятность проникновения микроорганизмов в легкие очень велика. Однако у здоровых людей дыхательные пути дистальнее гортани стерильны. Еще меньшее значение (по частоте встречаемости) имеют гематогенное и непосредственное распространение возбудителя из очага инфекции. Клиническая практика показывает, что возникновение пневмоний нередко связано с рядом условий или факторов риска, предрасполагающих к заболеванию. Вирусная инфекция верхних дыхательных путей. Десквамация эпителия и даже некрозы, характерные для вирусной инфекции, ведут к нарушению мукоцилиарного транспорта и дренажной функции бронхов, что благотворно сказывается на размножении других микроорганизмов. Этому способствует также угнетение клеточного и гуморального иммунитета, снижение активности альвеолярных макрофагов. Обструкция бронхиального дерева. Нарушение дренажной функции бронхов и мукоцилиарного транспорта ведет к задержке слизи и размножению микроорганизмов, среди которых чаще обнаруживаются пневмококки. В происхождение значительной части пневмоний решающую роль приобретают нарушения местной бронхиальной проходимости. В остром периоде у 95% больных имеется скрытый бронхоспазм, а у 44% - явный, в период реконвалесценции у 75% скрытый, а у 21% - явный бронхоспазм. Бронхоспазм ведет к снижению активности мукоцилиарного барьера, активируется микрофлора. Развитию пневмоний способствуют нарушения фагоцитарной функции лейкоцитов и макрофагов, что особенно отчетливо проявляется при лейкозах, сахарном диабете. Иммунодефициты. В настоящее время все более очевидным становится значение в развитии пневмоний иммунодефицитных состояний. Дефицит гуморального иммунитета протекает с недостаточной продукцией антител. В этих случаях характерна инфекция пневмококком, стафилококком. При дефиците клеточного иммунитета наблюдается неполноценность лимфоцитов Т, что способствует более частому инфицированию стафилококком, грамотрицательными палочками и вирусом простого герпеса. Причины развития иммунодефицитных состояний удается установить далеко не всегда. Они могут быть связаны с ранее перенесенными заболеваниями и травмами, быть следствием лечения кортикостероидами, цитостатиками. Клиническое течение таких пневмоний отличается большим своеобразием, что и позволило выделить пневмонии при иммунодефицитах. Алкоголь. Больные алкоголизмом предрасположены к пневмони Дата добавления: 2015-02-05 | Просмотры: 1180 | Нарушение авторских прав |
 Мокрота в первые 3 дня Кровь
Мокрота в первые 3 дня Кровь

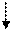 Бактериоскопия Посев
Бактериоскопия Посев
 Клетки воспаления
Клетки воспаления