|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Неингаляционный наркозПринцип многокомпонентности анестезиологического пособия позволил с успехом проводить оперативное вмешательство без той мультифокальной депрессии центральной нервной системы, которая типична для традиционных ингаляционных анестезирующих средств с сохранением стабильной гемодинамики и без подавления механизмов, регулирующих гомеостаз. Это делает внутривенную анестезию более управляемой, технически более простой и нетоксичной. Не случайно, что в последние годы развитие анестезиологии в стоматологии отмечено интенсивным поиском тех вариантов анестезии, при которых отпадает необходимость вводить в организм средства общенаркотического действия. Стоматологические больные, поступающие для лечения, не могут иметь одинаковый функциональный фон, при котором нужна бы была одна и та же степень аналгезии и нейролепсии. Это обстоятельство привело к созданию основных и вспомогательных средств для общей анестезии. Внутривенные компоненты анестезиологического пособия применяются не только на разных этапах оперативного вмешательства, но и являются методами интенсивной терапии (аналгезия, вегетативная блокада, атараксия, миоплегия), которая принципиально не отличается от анестезиологического пособия. Многокомпонентность является отличительной чертой современной анестезиологии и позволяет строго индивидуализировать тактику в зависимости от характера хирургического вмешательства, физического статуса больного, выраженных особенностей и сопутствующей патологии. В этом разделе мы коснемся основных современных неингаляционных анестезиологических средств, применяемых в стоматологии. Совокупность местных и общих проявлений заболевания, относительная кратковременность вмешательства создают особые условия для проведения анестезии в амбулатории. С учетом этих особенностей мы выделяем те качества, которыми должна обладать анестезия: кратковременность эффекта, минимальная токсичность, отсутствие
выраженного влияния на основные системы организма; достаточная релаксация, в том числе жевательной мускулатуры; снижение активности гортанноглоточньгх рефлексов; минимальное воздействие на слюноотделение. Гексенал. Тиопентал натрия. Преимущество внутривенного наркоза заключается в быстроте и удобстве индукции и отсутствии стадии возбуждения. Реализация протекторных свойств барбитуратов при гипоксии составила значительный этап анестезиологии в использовании этих средств. Остается актуальным дальнейшее развитие проблемы внутривенного наркоза и поиски средств, свободных от недостатков, которыми обладают, в частности, препараты барбитуровой кислоты. В последние годы представления о механизмах развития наркоза у этой, наиболее старой группы внутривенных средств, в значительной степени изменились. Самостоятельный, длительный, внутривенный наркоз барбитура-тами в настоящее время практически не используется. Клиника вводного наркоза мало отличается от того, каким средством проводится наркоз. Для вводного наркоза характерно быстрое и незаметное для больного наступление сна и практически полное отсутствие стадии возбуждения. Барбитураты являются традиционными средствами внутривенной анестезии и в полной мере отвечают сказанному. Считается, что тиопентал натрия и гексанал инактивируются главным образом печенью. Это старое правило необходимо учитывать при использовании указанных препаратов у больных с заболеванием печени. Известно, что при введении в наркоз барбитураты снижают сердечный выброс на 20—30% и связано это с отрицательным инотропным действием препаратов на миокард (Гало-горский В.А. и др., 1979; Дарбинян Т.М. и др., 1980). Гиповолемия при кровотечении, постуральные реакции, гипервентиляция могут вызвать дальнейшее снижение сердечного выброса. При проведении барбитурового наркоза у стоматологических больных необходимо помнить о рано проявляющейся центральной дыхательной депрессии. Такая депрессия носит умеренный характер, но в связи с шинирова-нием челюстей, дислокацией тканей может привести к значимым нарушениям газообмена. Угнетение дыхания КОМБИНИРОВАННЫЕ МЕТОДЫ АНЕСТЕЗИИ И НАРКОЗА 93 наблюдается по окончании наркоза и ИВЛ. У ослабленных больных подобная депрессия может быстро прогрессировать. Вводный наркоз не должен совпадать с началом манипуляций в полости рта и глотке (интубация трахеи, введение воздуховода), что может привести к кашлевому рефлексу, ларинго- или бронхоспазму, реакции со стороны трахеокардиального рефлекса (брадикардия, нарушение ритма, остановка сердца). Такой механизм синкопэ является одной из причин осложнений, в связи с барбитуровым наркозом. К числу редких осложнений наркоза барбитами относятся различной степени выраженности аллергические реакции, проявляющиеся уртикарной сыпью, падением АД, бронхоспазмом. При использовании барбитуратов для анестезии на начальном этапе возможно появление гипер-рефлексии. При этом следует доводить наркоз до стабильного уровня (миоз, сниженный роговичный рефлекс, аналгезия), несмотря на депрессию биоэлектрической активности мозга. Интубацию трахеи, сопровождающуюся кратковременным подъемом АД и учащением сердечного ритма, можно считать допустимой только у больных без сопутствующих сердечно-сосудистых заболеваний. У пациентов с гипертонической болезнью, коронарной недостаточностью во избежание осложнений целесообразно усилить анестезию и гипорефлексию добавлением других средств (Осипова Н.А., 1968). Учитывая изложенное, вряд ли целесообразно стремиться к проведению вводного наркоза барбитуратами в «чистом» виде. Это сопряжено с необходимостью достижения глубокого наркоза, а следовательно, с использованием больших доз анестетиков. Сомбревин (пропанидид, эпонтол). Это небар-битуровое наркотическое средство, производное эугенола. В организме сомбревин подвергается быстрому ферментативному расщеплению, главным образом в печени и крови. Спустя 25 мин. после введения препарат перестает определяться в сыворотке крови, тогда как барбитураты обнаруживаются в крови в течение суток (Caillard В., 1980). Сомбревин не требует предварительного разведения и вводится непосредственно в вену в количестве 8—10 мг/кг массы при средней скорости 10 мг/с. Наркотический эф-
фект сомбревина развивается стремительно. При этом отмечается гипервентиляция с увеличением частоты и глубины дыхания. Действие сомбревина на дыхание отличается своеобразием и постоянством проявлений. Наблюдаются две фазы изменений дыхания. Первая характеризуется увеличением минутного объема до 250—350 % и сменяется второй фазой угнетения дыхания вплоть до апноэ. Изменения гемодинамики при наркозе сомбревином преходящи и сводятся к снижению минутного объема сердца за счет тахикардии при одновременном уменьшении сердечного выброса, снижения АД и периферического сопротивления. Продолжительность этих сдвигов не превышает 2—4 мин., после чего наступает нормализация показателей. Сомбревин выпускается в виде 5 % раствора с добавлением стабилизатора. В одной ампуле содержится 10 мл (500 мг) сомбревина. Несмотря на сходство сомбревина с барбитуратами, он отличается по характеру наркотического действия, длительности и влиянию на основные функции организма. Потеря сознания происходит внезапно, а не постепенно, как это характерно для барбитуратов. По быстроте восстановления психических и моторных функций после наркоза сомбревину нет равных. Для него характерно быстрое пробуждение с полной ориентировкой в окружающей обстановке. Спустя несколько минут психическая деятельность полностью восстанавливается. Это делает со-мбревин особо ценным анестетиком для амбулаторной практики. Больные после наркоза не требуют особого наблюдения и могут быть спустя 30 мин. отпущены домой. Для сомбревина характерна мышечная гиперактив-ность (судороги, икота), особенно в период выхода из наркоза. При мощных рефлекторных воздействиях, под влиянием трахеи, целесообразна комбинация сомбревина с другими общими анестетиками. Т.М. Дарбинян и Т.А. Хашман (1982 г.) считают наиболее целесообразной комбинацию сомбревина с фентанилом, предотвращающую возникновение постинтубационной гипертензии и тахикардии. Седуксен, являясь транквилизатором с противосудо-рожным действием, оказывает тормозящее действие на активацию сомбревином подкорковых структур. Отсюда сочетание сомбревина и седуксена вполне оправдано. КОМБИНИРОВАННЫЕ МЕТОДЫ АНЕСТЕЗИИ И НАРКОЗА 95 Таким образом, сомбревин, отличаясь от ранее рассмотренных препаратов, обладает ультракоротким наркотическим действием, быстрым восстановлением исходного функционального состояния ЦНС, тем самым определяется его ценность для амбулаторной анестезиологии. Наряду с этим сомбревин, точнее его стабилизатор — кремофор, обладает способностью освобождать эндогенный гистамин (Осипова Н.А., 1988), что может явиться причиной тяжелых и смертельных аллергических реакций и требует обязательной преднаркозной подготовки антигистаминньгми средствами. Сомбревин нецелесообразно применять у людей с отягощенным аллергологическим анамнезом. Гипномидат (этомидат). Водорастворимый наркотический препарат короткого действия с большой терапевтической широтой, не похожий по химической структуре ни на один из известных наркотических агентов. Наркоз этомидатом развивается быстро в течение 20—30 сек. после введения. Наступление сна не сопровождается нарушениями дыхания и кровообращения. Продолжительность сна не превышает 10 мин. при дозе 0,3 мг/кг. Гипномидат применяется при амбулаторных вмешательствах как гип-нотик кратковременного действия. Для усиления наркотической силы препарата требуется дополнительное применение анальгетиков. Отсутствие влияния на дыхание и кровообращение свидетельствует, что при амбулаторном наркозе гипномидат является методом выбора. При анестезии этим препаратом не происходит нарушений газообмена и легочной вентиляции. Это считается одним из главных преимуществ гипномидата перед другими внутривенными анестетиками короткого действия. Гипномидат, не изменяя частоты сердечных сокращений, незначительно снижает систологическое АД, не влияет на сократимость миокарда, снижая потребление кислорода. Это свойство позволяет применять гипномидат в стационаре и амбулатории у больных с нарушениями системы кровообращения. В отличие от сомбревина гипномидат, применяемый внутривенно, не приводит к повышению концентрации гистамина в крови, в результате дополнительного его высвобождения. Хорошие результаты дает сочетание гипномидата с закисью азота. Благодаря
минимальному угнетению дыхания и кровообращения он может быть использован у больных с сердечной патологией. Оксибутират натрия (ГОМК). Оксибутират натрия — натриевая соль гаммаоксимасляной кислоты. Обладает гипнотическим (снотворным) и более слабым анальгезирующим действием. Общепринятой методикой является внутривенный путь введения 20 % раствора в ампулах по 10 мл. Дозы применения препарата составляют от 40—50 мг/кг для достижения гипнотического действия и 60—80 мг/кг массы для достижения хирургической стадии наркоза. Для получения адекватной аналгезии оксибутират натрия применяют с анальгетиками, закисью азота, барбитуратами, фторотаном. Особенностью ГОМК является самостоятельная фаза глубокого сна, но отсутствует при этом адекватная хирургическая стадия наркоза, которая достигается более высокими концентрациями. Значительное распространение ГОМК получил в 70— 80-е гг. как малотоксичное средство, не влияющее на систему дыхания и кровообращения, не угнетающее клеточный метаболизм. Последнее свойство в сочетании со способностью обеспечивать процессы окисления и фосфори-лирования повышает устойчивость тканей организма к гипоксии и позволяет его считать протектором антигипок-сической активности, обеспечивающей наилучшую защиту печени, мозга, почек при критических состояниях. К недостаткам ГОМК следует отнести малую управляемость анестезии, длительное пробуждение, что нежелательно при его использовании в амбулаторных условиях. Отчетливое седативное, антипсихотическое и проти-восудорожное действие ГОМК в малых дозах (100—200 мг) делает его препаратом выбора для преднаркозной подготовки, являющейся одновременно средством премеди-кации и базисного наркоза. Целесообразно в подобных ситуациях его пероральное введение, особенно в детской практике. Наркотический сон наступает через 35—40 мин., достигая максимума к 1,5 часам при сохранении самостоятельного дыхания. При этом утрачивается необхо- КОМБИНИРОВАННЫЕ МЕТОДЫ АНЕСТЕЗИИ И НАРКОЗА 9 7 дямость в ИВЛ, но возникает необходимость дополнения анестезии другими средствами: местно-инфильтрацион-ной и проводниковой анестезией, масочной ингаляцией закиси азота, внутривенным введением малых доз нарко-тическ их ан ал ьгети к о в. ГОМК применяется как моноанестетик с целью увеличения устойчивости к гипоксии. Наиболее оправданным является применение его для целей базис-наркоза, при поддержании длительной анестезии, что обусловлено большой терапевтической широтой, длительным наркотическим действием, слабыми анестетическими свойствами и мощиой потенцирующей активностью. Благодаря минимальной токсичности и возможности перорального введения препарат особенно ценен в практике детской и гериатрической хирургии (Осипова Н.А., 1988; Островский В. Ю., 1972). Кетамин (кеталар, к а липсол). Актуальным остается поиск эффективных препаратов для наркоза в амбулаторной стоматологии. Поэтому понятен тот интерес, который был вызван у ааестезиологов к появлению кета- мина и его аналога калипсола. Наркотическое средство кетамин обладает выраженным «диссоциативнмм» и селективным действием, угнетающим подкорковые структуры, стимулирующим лимбичес-кую систему и ретикулярную формацию (Дарбинян Т.М., 1983; Domino E.F. et al., 1982; Klausen N.0„ 1983). Используют кетамин в качестве анестетика для вводного, базисного и мононаркоза в дозах 1—2 мг/кг внутри -венно и в дозах 4—7 мг/кг внутримышечно. Для поддержания общей анестезии применяют кетамин 0,5 мг/кг внутривенно и 3 мг/кг внутримышечдо. В отличие от известных наркотических средств клиника кетаминового наркоза имеет некоторые особенности. Через 5—10 сек. после начала внутривенного введения у больных утрачивается сознание. Больной лежит с открытыми глазами, все рефлексы живые, может наблюдаться нистагм. Кожные покровы сухие, теплые, обычной окраски. Артериальное давление повышается на 20—30 мм рт. ст., пульс учащается на 10—20 ударов в 1 мин., дыхание сохраняется в полном объеме. Из-за способности кетамина 4 3ai. i2
оказывать избирательное стимулирующее действие на лимбические структуры головного мозга, его относят к группе галлюциногенов. Поэтому начальные этапы развития наркотического состояния сопровождаются возбуждением или вегетативными расстройствами в виде гипертен-зии или тахикардии. Одновременное использование нескольких препаратов (анальгетик, атарактик, гипнотик) позволяет проводить адекватную анестезию для любой категории стоматологических больных, включая использование всех основных факторов современной анестезии: сон, аналгезию, релаксацию. Клиническая картина кетаминовой анестезии у стоматологических больных, когда применяются минимальные дозы (субнаркотические), характеризуется стимулирующим влиянием препарата на сердечно-сосудистую систему с умеренным повышением АД и увеличением частоты сердечных сокращений (ЧСС) без признаков нарушения ритма. Увеличение среднего АД и возрастание минутного объема кровообращения, сопровождалось снижением систолического объема и общего периферического сопротивления. Избыточная стимуляция гемодинамики при «чистой» кетаминовой анестезии не может быть рекомендована у больных с высоким хирургическим и анестезиологическим риском, при декомпенсированных заболеваниях сердечно-сосудистой системы. Седуксен и дроперидол уменьшают чрезмерную ги-пертензию при комбинированной анестезии. Снижение артериального давления и урежение пульса под влиянием этих препаратов, вероятно, связано с гемодинамическими свойствами дроперидола, которое проявляется возрастанием периферического кровенаполнения (Кузин И.И., 1977), снижением периферического сопротивления и центрального венозного давления (Бунятян А.А., 1968) и оказывает умеренное вазоплегическое действие (Мещеряков А.В., 1971). Применение комбинации кетамин-дропе-ридол и кетамин-седуксен позволяет предотвратить или смягчить побочное действие мононаркоза кетамином со стороны системы кровообращения. Сочетание кетамина и закиси азота при плановых оперативных вмешательствах следует признать оптимальным средством для выключе- КОМБИНИРОВАННЫЕ МЕТОДЫ АНЕСТЕЗИИ И НАРКОЗА 99 ния сознания в связи с управляемостью и минимальной токсичностью этой смеси. При продолжительных плановых оперативных вмешательствах оправдана следующая методика кетаминовой анестезии: в качестве премедикации пациентам на ночь назначали снотворные и седативные средства, а за 30 мин. до операции вводили седуксен в дозе 5—10 мг внутримышечно, 20 мг промедола, 0,5 мг атропина. Индукция проводилась с помощью внутривенного введения седуксена 0,3 мг/кг массы и кетамина 5 мг/кг. Для выключения дыхания и миоплегмии применялась тест-доза туба-рина (7,5 мг) и деполяризующего релаксанта (150—200 мг), после чего проводилась интубация трахеи. Для поддержания общей анестезии кетамин вводился фракционно 3—5 мг/кг массы в сочетании с дроперидолом (0,5 мг/кг) в потоке закиси азота с кислородом в соотношении 3:1. Искусственная вентиляция легких осуществлялась аппаратом РО-5 или РО-6 в режиме умеренной нормо- или гипервентиляции (Грицук С.Ф., 1981). В амбулаторной стоматологической практике применение кетамина в сочетании с атарактиками не влияло на спонтанную вентиляцию легких, не вызывало депрессии дыхания, сохраняло гортаноглоточные рефлексы. Эти особенности кетаминовой анестезии важны у пациентов при лечении зубов. Внутримышечное и внутривенное введение кетамина при амбулаторном приеме характерно сохранением в течение непродолжительного времени после-наркозной депрессии и мышечной вялости. Кетамин широко применяется в неотложной стоматологии. Его свойства не вызывать депрессию дыхания и сохранять функцию гортаноглоточных рефлексов применяется при общей анестезии у больных флегмонами челюстно-лицевой области и дна полости рта. В неотложной стоматологии применяют следующую методику кетаминовой анестезии: премедикацию атропином в общепринятых дозировках. Вводный наркоз и поддержание общей анестезии проводится в двух вариантах: седуксен 10 мг, калипсол 2 мг/кг, а для поддержания анестезии — 1 мг/кг; седуксен 10 мг, калипсол 1 мг/кг, со-мбревин 500 мг. Наркоз проводят на фоне самостоятельного дыхания.
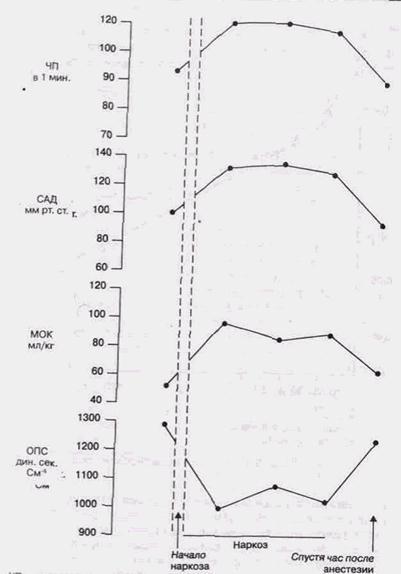
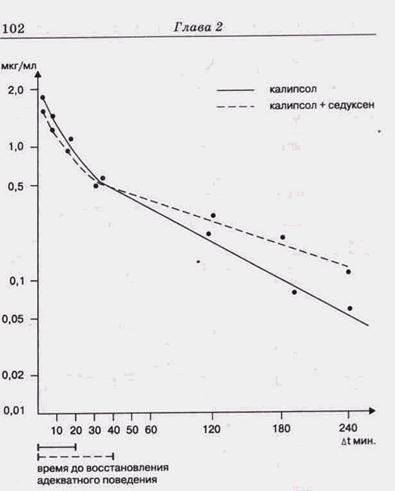
У больных с острыми воспалительными процессами в челюстно-лицевой области введение кетамина сопровождалось повышением среднего АД на 25 %, увеличением частоты сердечных сокращений на 20 % и одновременного возрастания минутного объема кровообращения (рис. 17). Обычно к концу операции наблюдалось снижение минутного объема кровообращения до исходного уровня. Исследование фармакокинетики калипсола позволяет считать, что она укладывается в рамки двухкамерной модельной системы. В течение 1 ч. концентрация препарата в крови изменялась с 1,5 до 0,3 мкгс/мл при Т 1/2 = 6,8 мин., Т 1/2 =° 61,8 мин. При применении калипсола на фоне седуксена концентрация препарата снижалась с 1,2 до 0,4 мкг/мл при Т 1/2 = 6,7 мин, Т 1/2 = 145,6 мин. (рис. 18). Как видно из полученных результатов, введение калипсола на фоне седуксена приводит к удлинению В — фазы, уменьшению скорости выведения калипсола. Оказалось, что введение калипсола без седуксена приводит к анальге-тическому эффекту продолжительностью 10 ± 2,5 мин., через 14 ± 2 мин. больной начинал вступать в контакт и через 20 — 2,5 мин. полностью возвращался к исходному состоянию. Таким образом, введение седуксена увеличивает время биологической жизни калипсола и коррелирует с клиническими данными, т.е. увеличение времени анальгетического действия, времени возвращения к адекватному состоянию (Лепахин В.К. и др., 1981). Специфическим отличием кетамина от всех других видов общей анестезии является картина гиперсинхрон-ного — ритма в ЭЭГ, сочетающаяся с нарушением или потерей сознания, анестезией, амнезией и особым сочетанием симптомов вегетативной (гипертензия, тахикардия), психоэмоциональной (галлюцинации, делирий) и моторной (судороги) активацией (Осипова Н.А., 1988). Таким образом центральное действие кетамина характеризуется первичной активацией лимбической системы мозга с последующим распространением возбуждения на кору и подкорковые структуры. На фоне распространенного возбуждения ЦНС наступает дезорганизация болевого проведения и появление побочных реакций. Это делает нецелесообразным использование кетамина в чистом виде. Наши данные подтверждают необходимость сочета- КОМБИНИРОВАННЫЕ МЕТОДЫ АНЕСТЕЗИИ И НАРКОЗА 101
ныйпк4'"''1'01'6' щпьса СА^ - среднее артериальное давление, МОК - минутный объем кровообращения. ОПС - общее периферическое сопротивление с rhn^0 17 динамика гемодинамических показателей у больных ч"1егмонамм в челюстно-лицевой области при калипсоловой анестезии
Рис. 18. Клиническая фармакокинетика калипсола ния кетамина с транквилизаторами бензодиазепинового ряда (седуксен, феназепам), обладающих прямым тормозящим действием на лимбические структуры мозга, устраняющие симптомы вегетативной и психомоторной активации и стабилизирующие течение анестезии. Особенности современного комплексного анестезиологического обеспечения амбулаторных стоматологических вмешательств и жесткие требования к созданию условий комфорта для стоматолога практически исключают КОМБИНИРОВАННЫЕ МЕТОДЫ АНЕСТЕЗИИ И НАРКОЗА 103 применения традиционной объемной искусственной вентиляции легких (ИВЛ). В последнее десятилетие методики использования ингаляционных средств для анестезии при амбулаторных стоматологических операциях подверглись пересмотру. Доминирующее значение приобрела тотальная внутривенная анестезия (ТВА), явившаяся средством выбора при терапевтических и хирургических вмешательствах. Такой подход обусловлен анатомо-топографическими особенностями черепно-лицевой области и полости рта. При этом операционное поле полости рта находится в зоне, где проходит газовоздушная струя для вентиляции легких и располагаются наконечники с жидкоструйными и воздушными потоками. Это затрудняет применение ларинге-альных масок, которые могут создавать непреодолимые препятствия для проведения санации полости рта. В этой связи поиски новых препаратов для ТВА и внедрение их в современную клиническую практику стоматологии и оперативной черепно-лицевой хирургии являются чрезвычайно актуальной задачей. Гипотетически идеальный препарат для наркоза в стоматологии должен отвечать требованиям конкретной клинической ситуации, которая нередко наблюдается в амбулаторной стоматологической практике: отек тканей полости рта, наличие операционной раны, снижение вентиляции за счет сужения воздухопроводящих путей и др. Он должен оказывать надежный эффект без побочного влияния на кровообращение и дыхание, не влиять на метаболизм других медикаментов, иметь короткий период полураспада независимо от состояния внутренних органов. Задачей исследования явилась разработка в отделении анестезиологии ЦНИИС различных методик ТВА на основе нового внутривенного анестетака дипривана (пропофол) «Zenaca» Англия. Диприван, анестетик, обладающий кратковременным действием, вызывает быстрое наступление сна без возбуждения в дозировках 2,5—3,0 мг/кг. Препарат может быть использован как для вводного наркоза, так и для поддержания анестезии. Как компонент ТВА, он может применяться во всех случаях, когда необходим предсказуемый анестетик, не влияющ.ий на основные системы
организма. Диприван обладает коротким периодом полувыведения, высоким клиренсом, который осуществляется в печени. Конъюгаты дипривана удаляются с мочой. Эти свойства дипривана легли в основу исследований методик ТВА в клинической амбулаторной стоматологии и черепно-лицевой хирургии. Дата добавления: 2015-02-06 | Просмотры: 1461 | Нарушение авторских прав |