|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Операции прямой реваскуляризации миокарда на работающем сердце без искусственного кровообращения — малоинвазивная коронарная хирургияНакопленный опыт выполнения операций реваскуляризации миокарда в условиях ИК, отработанная десятилетиями хирургическая техника АКШ создали все необходимые предпосылки для появления новых технологий и методик в хирургическом лечении ИБС. F.Benetti (1993) — пионер современной коронарной хирургии без ИК — в докладе на международной конференции 1994 г. подвел первые итоги применения этого метода, называя его «менее инвазивным», что наиболее точно отражает его суть. Результаты хирургического лечения 2000 пациентов ИБС, прооперированных без ИК, превзошли все ожидания. Операции на работающем сердце оказались более безопасными, что в свою очередь расширило показания к ним, процесс реабилитации больных стал значительно короче, а экономические аспекты более выгодными, чем при операциях с ИК. На сегодняшний день определены основные пути применения метода малоинвазивной коронарной хирургии и выработаны показания к нему. Отсутствие негативного влияния ИК как непосредственно на миокард (по данным K.Arom, опубликованным в 1999 г., частота периоперационных инфарктов миокарда составила 0,6 % без ИК и 2,2 % с ИК, а нарушения ритма — 14 и 23 % соответственно), так и на весь организм в целом позволило расширить показания к применению малоинвазивной коронарной хирургии. Стало возможным оперировать больных с исходно сниженными ресурсами сердечно-сосудистой системы и тяжелой сопутствующей патологией (почечно-пече-ночная недостаточность, ХНЗЛ, диабет, выраженный атеросклероз брахиоцефальных сосудов, инсульт в анамнезе, злокачественные новообразования и т.д.). Техника операций на работающем аортокоронарного шунтирования используют универсальный доступ, каким является срединная стерно-томия. Первоначально на пристеночно отжатой аорте выполняют все проксимальные анастомозы. При выполнении дистальных анастомозов используют специальные стабилизаторы (Octopus) либо турникеты — держалки. В обоих случаях это позволяет обеспечить малоподвижность КА в месте наложения анастомоза и добиться сухого операционного поля, однако в ряде случаев в месте артериотомии находятся боковые ветви КА, чей ретроградный кровоток создает определенные технические трудности. В таких ситуациях визуализация места анастомоза улучшается смыванием крови из его просвета струей газа (СО2) или изотонического раствора натрия хлорида. Перед выполнением артериотомии необходимо провести тесты с пережатием КА, что позволяет не только выявить реакцию миокарда на ишемию, но и адаптировать миокард к ней. В ряде случаев данный тест проводят неоднократно с целью стабилизации гемодинамики и профилактики развития сложных нарушений ритма. Особенно важна адекватность проведения «ишеми-ческого теста» в случае шунтирования неокклюзированной КА. Следует отметить, что наиболее чувствительной к пережатию оказалась ПКА. В ряде случаев из-за тяжелых ишемических изменений миокарда на ЭКГ возникает необходимость использования внутреннего шунта, что позволяет наложить дисталь-ный анастомоз на функционирующую КА и предотвратить возможность появления тяжелых осложнений. При наложении анастомоза, как широко используют различные фармакологические препараты — b-блокаторы ультракороткого действия, антагонисты кальция, а также кратковременную остановку сердца аденозином, однако ряд авторов считают эффект аденозина трудно предсказуемым [Gill S., 2000] и воздерживаются от его применения. При реваскуляризации КА задней поверхности сердца, требующей его выворачивания, в некоторых случаях возникает нестабильность гемодинамики, требующая использования инотропной поддержки и увеличения объема инфузии, что непременно увеличивает время наложения анастомоза до 10— 12 мин. При этом ударный объем снижался на 21 % в случае экспозиции ОВ, на 6 % при экспозиции ПМЖВ или 15 % при экспозиции ПКА, среднее артериальное давление составляло 61—65 и 68 мм рт.ст. соответственно, а необходимость в инотропной поддержке возникала в 28 и 5 % случаев соответственно. Для объективной оценки метода прямой реваскуляризации миокарда без ИК на работающем сердце необходима тщательная оценка отдаленных результатов. На 77-м Ежегодном конгрессе Ассоциации торакальных хирургов (май 1997 г.) были представлены данные семилетнего наблюдения 120 пациентов, оперированных с ИК, и 117 пациентов, оперированных без ИК. При этом с одинаковой частотой шунтированы ПМЖВ и ПКА. Существенные различия отмечены при шунтировании ОВ (89 и 18 % соответственно). Семилетняя выживаемость составила 80 % в обеих группах; статистически достоверные, но незначительные отличия выявлены лишь в количестве функционирующих шунтов — 67 и 74 % соответст-вено. Мини-инвазивная коронарная хирургия. В 1995 г. в клиническую практику кардиохирургии вошел новый метод — мини-инвазивная коронарная хирургия. Наиболее емкое определение термину «мини-инвазивная реваскуляризация миокарда» (МИРМ) дал A.Calafiore (1996): МИРМ — реваскуляризация миокарда через торакотомию не более 10 см, без ИК, с использованием только артериальных кондуитов in situ. Итогом 2-го Всемирного Конгресса по малоинвазивной реваскуляризации миокарда (Испания, Барселона, 1998 г.) явилось определение показаний для МИРМ: 1. Повторные операции. 2. Одно-, двухсосудистое поражение КА в группе пациентов повышенного риска для операций с использованием ИК. 3. Рестеноз КА после ТЛБАП. Технические аспекты мини-инва-зивной коронарной хирургии. К настоящему времени применяют несколько мини-инвазивных досту-
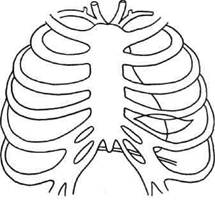
Рис. 5.6. Мини-торакотомия.
пов, позволяющих шунтировать практически все коронарные артерии: право- и левостороннюю ми-ни-торакотомию с иссечением или без иссечения реберных хрящей [Benetti F. et al., 1995; Subramanian V. et al., 1996] (рис. 5.6); субксифо-идальный доступ [Grandjean et al., 1996]; парастернальную левостороннюю мини-торакотомию с иссечением реберных хрящей [Власов Г.П. и др., 1998; Nataff P. et al., 1996] (рис. 5.7). Было разработано также несколько доступов, позволяющих произвести реваскуляриза-цию нескольких КА: Г-образ-ный нижний мини-стернотомиче-
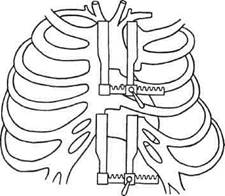
Рис. 5.8. Верхняя и нижняя срединная мини-стернотомия для выполнения аутовенозного аортоконарного шунтирования.
ский доступ для множественного маммарокоронарного шунтирования (ПМЖВ, ДВ и ПКА), верхний и нижний министернотомические доступы для выполнения аутовенозного аортокоронарного шунтирования ПМЖВ, ДВ, ВТК и ПКА [Власов Г.П. и др., 1998] (рис. 5.8). Одними из самых больших проблем мини-инвазивной коронарной хирургии являются нехватка артериальных кондуитов для полностью артериальной реваскуляризации миокарда, а также метод их мобилизации. Во многом эту проблему решает методика эндоскопического выделения артериальных трансплантатов. К преимуществам эндоскопической мобилизации следует отнести прецизионность и малотравматич-ность техники, возможность выделения артерии на всем ее протяжении с пересечением всех боковых ветвей без технических сложностей. Использование эндоскопической техники позволяет уменьшить доступ до 4—5 см. Мобилизация ВГА в скелетизированном виде осуществляется гораздо проще, обеспечивает выигрыш в длине трансплантата до 25 %, что в свою очередь позволяет разрешить проблему нехватки длины и избежать его натяжения. На сегодняшний день уже разработаны и внедрены методы эндоскопической мобилизации обеих внутренних грудных и правой желу-дочно-сальниковой артерии ПЖСА (Г.П.Власов, P.Nataff). При эндоскопическом выделении ВГА используют раздельную интубацию бронхов посредством двухпросвет-ной трубки «Carlens» и проводят од-нолегочную (правую) вентиляцию. Больного укладывают на правый бок с наклоном 30° и с отведенной вверх левой рукой. Артериальные кондуиты выделяют эндоскопически через три торакопорта, проведенных в левую плевральную полость. При этом камера находится справа от эндоскопических инструментов в третьем межреберье по передней подмышечной линии. Второй порт вводят в четвертое-пятое межреберье по средней подмышечной линии и третий порт — в шес-тое-седьмое межреберье по передней подмышечной линии. Подобное расположение торакопортов (рис. 5.9), по нашему мнению, значительно улучшает возможность визуализации и оставляет больше возможности для выполнения хирургических манипуляций (Г.П.Власов и др.). Расположение портов по отношению к межреберным промежуткам в каждом конкретном случае индивидуальное в зависимости от конституциональных особенностей пациентов. ЛВГА выделяют на всем протяжении с клипированием и пересечением боковых ветвей. Мобилизацию ВГА всегда начинают в средней части с продольного рассечения париетальной плевры в проекции артерии в проксимальном и дистальном направлениях. Далее производят рассечение внутренней поперечной грудной мышцы в проекции артерии в дистальном направлении. Учитывая выраженную склонность ВГА к спазму, после отсечения ее дистальной части в просвет артерии вводят раствор папаверина, что позволяет добиться адекватного антеградного кровотока. Ни в одном случае эндоскопического выделения ВГА не было зафиксировано значимого повреждения артерии или развития про-фузного кровотечения, в случае же отрыва мелких боковых ветвей после остановки активного кровотечения путем временной компрессии марлевым тупфером поврежденную ветвь клипируют. Среднее время мобилизации ЛВГА составляет 40+10 мин [Власов Г.П., 1998]. Применение эндоскопической методики в мобилизации ВГА позволяет в случае необходимости выполнения двухсосудистой реваску-ляризации миокарда вместе с ЛВГА произвести выделение и ПВГА. При этом оба кондуита выделяют через левосторонний доступ без изменения расположения портов. Необходимо отметить, что мобилизация ПВГА должна проводиться в первую очередь, в противном случае мобилизованная первой ЛВГА значительно затрудняет дальнейшие манипуляции. Техника выделения ПВГА не отличается от таковой при мобилизации ЛВГА. После тщательного эндоскопического контроля гемостаза осуществ- ляют доступ к КА — левосторонний парастернальный доступ длиной 4 см с резекцией участков хрящей IV или V ребер или левостороннюю переднюю миниторакотомию длиной 4—5 см. Перикард рассекают продольно и фиксируют на держалках. На участок КА в месте предполагаемого анастомоза накладывают турникеты и после проведения пробы с пережатием КА осуществляют анастомоз непрерывным обвивным швом нитью пролен 7/0. Накопленный опыт эндоскопического выделения ВГА позволяет заключить, что данная методика вполне безопасна и применима в подавляющем большинстве случаев. Однако ряд факторов значительно затрудняет мобилизацию кондуита, делая ее не только неэффективной, но и подчас рискованной. К такого рода затрудняющим факторам относятся узкие межреберные промежутки, значительные жировые отложения в переднем средостении и выраженный спаечный процесс в плевральной полости. Мобилизация ПЖСА может также проводиться с использованием эндоскопической поддержки, что имеет преимущества перед выделением артерии через мини-лапаро-томию. Эндоскопическую мобилизацию ПЖСА выполняют через 3 лапаро-порта. При этом через иглу Вереша, проведенную через пупочное кольцо, в брюшную полость нагнетают воздух, после чего всегда через пупочное кольцо проводят первый порт для видеокамеры. Второй и третий порты для эндоскопических инструментов устанавливают в левом мезогастрии (рис. 5.10, а). При необходимости обеспечения адекватной тракции желудка в эпигаст-рии может быть установлен дополнительный порт для зажима Бэбко-ка (рис. 5.10, б). Мобилизацию ПЖСА проводят от луковицы двенадцатиперстной кишки до селезеночного угла же-
Рис. 5.10. Расположение лапаропортов при выделении ПЖСА. Объясне: ние в тексте. лудка. Парные короткие ветви кли-пируют и пересекают. Передние и задние ветви клипируют раздельно, что позволяет избежать деформирования кондуита. Для исключения «излишней» мобильности ПЖСА во время мобилизации желательно оставлять 1—2 перемычки из коротких ветвей. После отсечения и клипирования дистальной части ПЖСА через отверстие 1 — 1,5 см, проделанное в сухожильном центре диафрагмы, артерию проводят в полость перикарда с контролем ее возможного перекрута. Среднее время мобилизации ПЖСА составляет примерно 65 мин. Для предотвращения спаз-
Рис. 5.11. Секвенциальное шунтирование двух коронарных артерий с помощью ЛВГА. Рис. 5.12. У-образный композитный шунт из лучевой и левой внутренней грудных артерий.
Рис. 5.13. Шунтирование ПМЖВ и ПКА с помощью внутренней грудной и передней желудочно-сальниковой артерий. Рис. 5.14. Шунтирование ПМЖВ и ДВ с помощью ЛВГА и ПКА с использованием дистальной части ЛВГА с вставкой из лучевой артерии.
мирования артерии в ее просвет вводят раствор папаверина. Благодаря широкому внедрению в клиническую практику метода эндоскопического выделения артериальных кондуитов появилась возможность расширить показания к МИРМ. У пациентов с поражением ПМЖВ и ДВ могут быть использованы следующие схемы МИРМ: секвенциальное шунтирование двух коронарных сосудов с помощью левой внутренней грудной артерии (рис. 5.11; 5.12) и использование Y-образного композитного шунта из ЛВГА и лучевой артерии в качестве свободного трансплантата, а также раздельное шунтирование ПМЖВ и ПКА с помощью ВГА и ПЖСА (рис. 5.13). Возможно также шунтирование трех КА (ПМЖВ, ДВ и ПКА) одной ЛВГА с исполь- зованием как антеградного, так и ретроградного кровотока по ней. При этом выполняют секвенциальное шунтирование ПМЖВ и ДВ, а с помощью дистальной части ЛВГА, надставленной лучевой артерией, проводят реваскуляризацию ПКА (рис. 5.14). Основные преимущества мини- миокарда заключаются в том, что мини-торакотомия не нарушает стабильность грудины, что позволяет пациенту вернуться к привычным физическим нагрузкам уже в раннем послеоперационном периоде. Кроме того, МИРМ расширяет показания к операции у больных с низкой фракцией выброса, острым инфарктом миокарда, тяжелыми сопутствующими заболеваниями и у больных преклонного возраста. Особую ценность миниинвазивная реваскуляризация миокарда приобретает в случае повторных операций. Возможность отказаться от продольной рестернотомии, каню-ляции аорты и полых вен, а также выполнения кардиолиза позволяет значительно снизить риск повторного хирургического вмешательства. Дата добавления: 2015-02-06 | Просмотры: 1104 | Нарушение авторских прав |