|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
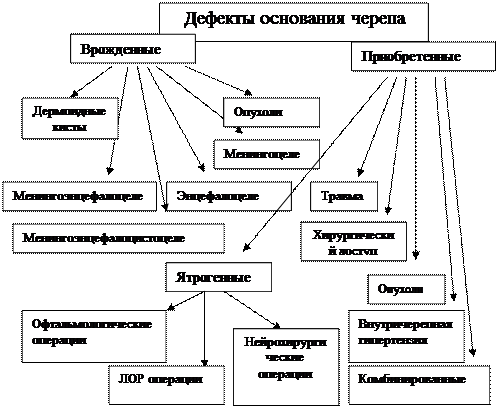
ДЕФЕКТЫ ОСНОВАНИЯ ЧЕРЕПА ПОСЛЕ УДАЛЕНИЯ КРАНИОФАЦИАЛЬНЫХ ОПУХОЛЕЙ (КЛАССИФИКАЦИЯ, ПЛАСТИЧЕСКОЕ ЗАКРЫТИЕ)Белов А.И., Винокуров А.Г., Цикаришвили Л.М., Зайцев А.М., Бекяшев А.Х. Дефекты основания черепа могут быть следствием врожденной патологии, травм, опухолей, внутричерепной гипертензии; ятрогенными (таб. № 1). Таблица № 1. Классификация дефектов основания черепа.
При возникновении дефектов основания черепа, включается сложный патогенетический механизм, проявляющийся ликвореей, изменениями ликвородинамики, смещением в той или иной степени ткани мозга в область дефекта, местными нарушениями кровообращения, воспалительной реакцией в связи с наличием прямого сообщения субарахноидального пространства с внешней средой. Если вовремя не разорвать этот порочный круг, возникают грозные, порой необратимые осложнения: менинго- и энцефалоцеле, менингоэнцефалит, грубые косметические деформации. В большинстве случаев дефекты основания черепа могут быть эффективно закрыты перемещенными местными тканями (надкостница, височная мышца, ткани глазницы) и свободными фрагментами жировой клетчатки. Эти методики не представляют сложности и могут быть выполнены при соблюдении определенных правил нейрохирургом. Разработка эффективных методов реконструктивной и пластической хирургии явилось основой для разработки блок-резекции у больных со злокачественными опухолями краниофациального распространения, когда удаляется опухоль единым блоком с прилежащими нормальными тканями (твердой мозговой оболочкой, мышцами, костями основания черепа и лицевого скелета, слизистой, тканями глазницы, кожей). Для пластики дефектов основания черепа применяются различные методики. Чаще всего применяется пластика местными тканями с сохранением их кровоснабжения. Пластика лоскутом надкостницы получила широкое использование в клинической практике. Лоскут надкостницы можно укладывать как выше, так и ниже верхнего края глазницы, в зависимости от характера дефекта основания черепа. Этот метод позволяет надежно отграничить твердую мозговую оболочку от области костного дефекта основания черепа, однако не создает достаточной жесткости, поэтому при больших дефектах необходимы в дополнение к нему другие методы пластики. Так Roux F.X. для создания прочности в дополнение к надкостничному лоскуту применял кораллы, а Goel A. фрагмент лобной кости. Эффективной при определенных дефектах является пластика височной мышцей. Появление метода микрохирургической аутотрансплантации позволил многие осевые лоскуты, которые раньше перемещали в пределах радиуса сосудистой ножки, свободно переносить на отдаленные дефекты с восстановлением кровообращения в трансплантанте путем подключения микрохирургическим сосудистым швом сосудистой ножки лоскута к источнику кровоснабжения в зоне дефекта. В настоящее время известно около 60 различных лоскутов. В 1989 году было предложено делить лоскуты на 3 основные группы: моно-, поли- и мегакомплексы тканей. Монокомплексы – это участки тканей, выделенные в пределах одного сосудистого бассейна единым блоком. Они наиболее пригодны для замещения дефектов тканей простой конфигурации (плоскостной, цилиндрической, сферической) и др. Именно монокомплексы тканей наиболее часто используются в клинической практике. Поликомплексы тканей представляют сочетание монолоскутов, выделенных в пределах одного сосудистого бассейна. Мегалоскут – это совокупность двух или нескольких монокомплексов или поликомплекса, границы которых выходят за пределы бассейна одного сосудистого пучка и для жизнеспособности которого необходимо сохранение дополнительных сосудов и другой сосудистой ножки. Впервые возможность закрытия обширных ран конечностей, сформированных на двух сосудистых ножках и включающих зоны кожно-фасциального пахового и кожно-мышечного торакодорзального лоскутов, была продемонстрирована японскими хирургами в 1981 году. Использование предплечья в качестве донорской области для формирования кожно-фасциальных лоскутов на сосудистой ножке было предложено китайскими авторами. На основании анатомических исследований ими была обоснована возможность выделения комплексов тканей на лучевом сосудистом пучке. Song R. осуществил свободную пересадку лучевого лоскута для устранения обширной послеожоговой контрактуры шеи. Показана эффективность применения лучевого лоскута для пластики дефектов основания черепа, а также закрытия дефектов после удаления опухолей. Впервые использование широчайшей мышцы спины было описано в 1886 году Тansini. Этот итальянский хирург покрывал дефекты грудной стенки после радикальной мастэктомии при помощи кожно-мышечного лоскута, состоящего из участка широчайшей мышцы спины, большой круглой мышцы с прилежащей кожей. Длинная сосудистая ножка позволяет идеально использовать широчайшую мышцу для свободной трансплантации. В последнее время появились сообщения об успешном применении широчайшей мышцы спины с фрагментом ребра для реконструкции сложных дефектов, в частности для моделирования верхней и нижней челюстей. На основе волокон прямой мышцы живота возможно формировать лоскуты, длина которых может достигать 50 см. В зависимости от ситуации применяются лоскуты, включающие прямую мышцу живота с включением кожной площадки или фрагмента ребра. В свободном варианте лоскут обычно пересаживают на нижнем сосудистом пучке. Размеры прямой мышцы, постоянство сосудистого пучка, является методом выбора при краниофациальных резекциях и для восстановления неба. Лоскуты из большой грудной мышцы применяются давно. С 1968 года данный лоскут используется в качестве составного лоскута из кожи и мышцы. Грудная мышца может быть использована в свободном или островковом вариантах, а также с включением фрагмента ребра. При их несвободной пересадке, точкой ротации лоскутов является место выхода грудоакромиальных сосудов в дельтовидно-грудной ямке (Моренгейма), что с успехом используется для реконструкции в области головы и шеи. Имеется много сообщений об успешном применении грудной мышцы после удалении опухолей пирамиды височной кости и удаления опухолей основания черепа и шеи. Давно известно, что большой сальник является хорошим биологическим материалом, используемым в пластической хирургии. Сальник имеет хорошее кровоснабжение и обладает свойством прилипать к другим тканям, которые впоследствии также быстро васкуляризируются, помимо этого, обладая особыми иммунологическими свойствами, сальник устойчив к воздействию инфекционных агентов. Длинная сосудистая ножка, большие размеры, склонность к адгезии позволяют использовать сальник в качестве оптимального пластического материала. Kiricutа и Galatar разработали методику мобилизации сальника с наложением сосудистого анастомоза в эксперименте на собаках, а McLean и Buncke пересадили его с целью закрытия обширной раневой поверхности на черепе в 1972 году с восстановлением кровообращения в сальнике путем формирования анастомозов между желудочно-сальниковыми и поверхностными височными сосудами. Sangler J. описал закрытие обширного кожно-костного дефекта свода черепа размером 15 х 16 см в результате постлучевого остеомиелитического повреждения. В последующем пластические хирурги использовали эти лоскуты для различных целей, включая реконструкции по поводу гемифациальной атрофии (болезнь Ромберга); реконструкции после резекции опухолей нижней челюсти и шеи; закрытия дефектов основания; реваскуляризации очагов ишемии головного и спинного мозга (оментопексия). Предложено ряд методов пластики дефектов основания черепа костными аутотрансплантантами. Широкие возможности открылись с внедрением методов расщепления кости и современных методов фиксации микропластинами. Широкое распространение получили различные пластические материалы- аутоткани
Расширились возможности радикального удаления опухолей с появлением клеевых композиций (Tissukol-Kit). Простота применения двухкомпонентного фибрин-тромбинового клея, способствует закрытию послеоперационных дефектов без применения сложных видов пластики, тем самым укорачивается время и объем операции. Попытка систематизировать дефекты краниофациальной области представляет большие трудности. Интересную классификацию предлагает Urken M. (1993), где основополагающим является степень поражения мягких тканей, костных структур, нервно-сосудистых пучков, вне зависимости от локализации поражения (таб.№ 2). В настоящее время единой концепции, позволяющей определить оптимальный метод пластики дефектов основания черепа в зависимости от характера, распространенности патологического процесса и особенностей возникающего дефекта. Дата добавления: 2015-02-05 | Просмотры: 1287 | Нарушение авторских прав |