|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
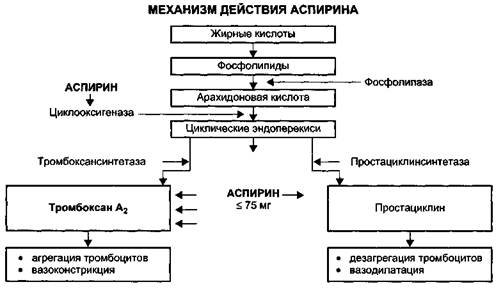
Схема 12.2
в 24 %, а НС в 76 % случаев, а у больных, не принимавших предварительно аспирин, соответственно в 54 и 46 % случаев (р < 0,0001). На сегодняшний день в Российских рекомендациях по лечению ОКС без стойких подъемов сегмента ST на ЭКГ, так же как и в рекомендациях Европейского общества кардиологов и Американской ассоциации сердца, указано, что прием аспирина в суточной дозе 75—325 мг в сутки на 50 % уменьшает вероятность смерти и ИМ при ОКС без подъема ST, а длительный прием аспирина у больных, перенесших ОКС, на 25 % снижает риск развития суммарной частоты ИМ, инсульта и сердечно-сосудистой смерти. Аспирин — единственный препарат, рекомендованный для длительного приема у больных, перенесших ОКС. Однако аспирин не решает все проблемы антитромботической терапии у больных с ОКС. Хорошо известно [Braunwald E. et al., 1994] что, несмотря на терапию аспирином, 10—15 % больных с ОКС умирают или переносят крупноочаговый ин- фаркт миокарда. Примерно 1/5 больных (20 %), перенесших ОКС, в течение года поступают в стационар повторно в связи с явлениями нестабильной стенокардии. Кроме того, применение коронароангиоскопии [Van Belle et al., 1998] у больных, переживших ОКС, позволило обнаружить признаки внутрикоронарного тромбоза спустя месяц после периода нестабильности, т.е. в период, когда у большинства больных отмечается стабилизация клинического состояния. У подавляющего большинства больных ОКС отмечается не только активация тромбоцитов, но и активация каскада коагуляции. Маркеры активации системы свертывания крови, отражающие усиленную генерацию тромбина, повышены более чем у 90 % больных ОКС, причем длительность их повышения существенно превышает длительность периода клинической нестабильности больного с ОКС и выявляется спустя 3—4 нед после периода нестабильности. Пусковым моментом в активации системы свертывания крови при ОКС является нарушение целос- тности покрышки атеросклероти-ческой бляшки и освобождение в кровоток тканевого фактора, инициирующего каскад коагуляции. Перечисленные факты указывают на целесообразность усиления анти-тромботической терапии у больных ОКС. Учитывая инициирующую роль тромбоцитов в патогенезе артериального тромбоза, в последние годы изучалась эффективность новых ан-титромбоцитарных препаратов при лечении ОКС. Ингибиторы IIb/IIIа-рецепторов тромбоцитов являются новым классом антитромбоцитарных препаратов, появившимся в последние 15 лет, по механизму действия их можно отнести к универсальным антитромбоци-тарным агентам, ингибирующим конечный этап агрегации тромбоцитов, индуцированной любыми агентами. Конечный этап агрегации тромбоцитов связан с образованием мостиков между активированными рецепторами Ilb/IIIa и адгезивными белками (фибриноген, фибронектин, фактор Виллебранда). При ОКС изучалась эффективность четырех ингибиторов IIb/IIIа-рецепторов: абсиксимаб (РеоПро), эптифибатид (интегрилин), тирофи-бан и ламифибан. Установлено, что добавление ингибиторов IIb/IIIа-ре-цепторов к терапии аспирином и ге-паринами при ОКС улучшает исходы эндоваскулярных вмешательств на коронарных артериях, в частности коронарной баллонной ангиопластики (КБА). Практически все исследования с абсиксимабом: epilog, epistemt, epic, capture, эптифибатидом: impact II, pursuit, тирофибаном: restore, prism+, установили снижение частоты смерти и ИМ за 30 дней наблюдения в сравнении с плацебо при коронарной баллонной ангиопластике у больных ОКС без подъема ST при одновременном использовании гепарина и аспирина. Эти результаты послужили основанием для организации исследования gusto IV, целью которого было оценить эффектив- ность абсиксимаба на фоне приема аспирина и гепарина у больных ОКС без подъема ST вне связи с вмешательством на коронарных артериях. Результаты gusto IV оказались разочаровывающими, добавление абсиксимаба к аспирину и гепарину не оказало дополнительного положительного воздействия ни на частоту смерти, ни на суммарную частоту смерти и ИМ, ни на смертность и потребность в срочной реваскуляри-зации миокарда. Среди причин полученных результатов gusto IV обсуждается возможный протромботи-ческий эффект абсиксимаба, так как Peter и соавт. (1998) обнаружили, что AT могут активировать IIb/IIIа-ре-цепторы с последующей диссоциацией, кроме того, больные, включенные в GUSTO-IV, не были крайне тяжелыми ("+" уровень тропонина Т имели всего 30 % больных), а показатели смертности в группе плацебо в GUSTO-IV составляли 8 % против 13,3 % в группе плацебо в метаана-лизе исследований pursuit и paragon. Надежды, связанные с появлением пероральных представителей ингибиторов рецепторов IIb/IIIа тромбоцитов, не оправдались, так как практически все исследования, посвященные их изучению, были досрочно завершены из-за большого числа серьезных геморрагических осложнений и увеличения смертности. Европейским и Российским обществами кардиологов рекомендуется использовать ингибиторы рецепторов IIb/IIIа тромбоцитов у больных с ОКС без подъемов ST лишь при проведении эндоваскулярного вмешательства на коронарных артериях. В США эксперты сочли, что результаты gusto IV не следует экстраполировать на другие ингибиторы IIb/IIIа-рецепторов и сочли возможным рекомендовать тирофибан и эптифибатид больным ОКС без вмешательства на коронарных артериях, однако абсиксимаб рекомендован только в случае проведения КБА. В отличие от аспирина антитром-боцитарный эффект производных ти-енопиридина: тиклопидина (тиклида) и клопидогреля (плавикса) связан с блокадой АДФ-индуцированной активации IIb/IIIa-рецепторов тромбоцитов. В марте 2001 г. в Орландо на ежегодной сессии АСС были впервые обнародованы результаты исследования CURE, целью которого было сравнение эффективности клопидогреля в комбинации с аспирином и монотерапии аспирином в лечении больных ОКС без подъемов ST. Идея комбинации аспирина с клопидогрелем для усиления анти-тромботического эффекта имеет теоретические и экспериментальные основания. Во-первых, препараты действуют на различные пути активации тромбоцитов, во-вторых, на модели артериального тромбоза у кролика был выявлен синергизм ан-титромботических эффектов аспирина и клопидогреля. Особенностью исследования CURE было использование однократной нагрузочной дозы в 300 мг для ускорения достижения максимального антитромбоци-тарного действия. Известно, что в обычной дозе — 75 мг/сут оптимальный антитромбоцитарный эффект клопидогреля достигается через несколько дней. В исследование было включено 12 562 больных ОКС без подъемов ST. Более 90 % больных с ОКС имели изменения конечной части желудочкового комплекса на ЭКГ, почти 100 % больных получали гепарин, 80 % бета-блокаторы, около половины больных получали ингибиторы АПФ и препараты, снижающие ли-пиды. Длительность лечения клопидогрелем была от 3 до 12 мес. Наблюдали за больными в течение 12 мес. Комбинация аспирина с клопидогрелем оказалась более эффективной по сравнению с монотерапией аспирином — снижение относительного риска сердечно-сосудистых событий (смерть, ИМ, инсульт) за 9 мес наблюдения составило 20 %; р = 0,001. Снижение относительного риска сердечно-сосудистых событий отмечалось независимо от наличия или отсутствия изменений на ЭКГ, повышения ферментов, наличия сахарного диабета и проведения реваску-ляризации после рандомизации. Количество серьезных геморрагических осложнений в группе комбинированной антитромбоцитарной терапии было больше, соответственно 3,6 и 2,7 %; р < 0,05, однако статистически достоверной разницы по числу угрожающих жизни геморрагии не отмечено — 2,1 и 1,8 %. 8 группе комбинированной анти-тромботической терапии чаще проводили переливания крови — у 2,8 % больных против 2,2 % в группе аспирина; р < 0,05. Было подсчитано, что на 1000 пролеченных больных за 9 мес наблюдения назначение клопидогреля предотвращает 28 сердечно-сосудистых событий у 23 больных, при этом возможно развитие 3 угрожающих жизни кровотечений и потребность в 3 переливаниях крови. Результаты исследования CURE, показавшие, что прием клопидогреля с аспирином в течение 3—6 мес позволяет снизить риск развития сердечно-сосудистой смерти, ИМ и инсульта на 1/5по сравнению с монотерапией аспирином, дают основания для использования данной комбинации у больных ОКС без подъемов ST с целью улучшения исходов и повышают шансы клопидогреля войти в необходимый минимум ан-титромбоцитарных препаратов, необходимых для лечения больных ОКС без подъемов ST. Отдельный анализ 2658 больных, подвергнутых КБА (исследование PCI-CURE), также подтвердил безусловные преимущества клопидогреля. В этой части исследования все больные в течение 4 нед получали клопидогрель, а затем возвращались к терапии в соответствии с рандомизацией. Коронарная баллонная ангиопластика проводилась в среднем через 10 дней от рандомизации больных. В группе больных, продолжавших принимать клопидогрель, относительный риск развития сердечно-сосудистой смерти, ИМ и потребности в срочной КБА за 30 дней наблюдения был на 30 % ниже (р = 0,03), чем в группе больных, принимающих аспирин. Снижение относительного риска смерти и ИМ за 12 мес наблюдения в группе клопидогреля составило 25 % (р=0,047). Результаты исследования PCI-CURE дают основания рекомендовать комбинацию аспирин + клопидогрель всем больным ОКС без подъема SТ до и в течение нескольких месяцев после процедуры КБА. Одновременно с активацией тромбоцитов при ОКС происходит активация свертывания крови, поэтому внутрикоронарный тромб при ОКС состоит не только из тромбоцитов, но и фибрина. В активации свертывания крови важнейшим моментом является высвобождение тканевого фактора из макрофагов атеромы. В результате активации коагуляцион-ного каскада усиливается образование тромбина, осуществляющего множество функций, среди которых основной является прокоагулянтная — осуществление перехода фибриногена в фибрин. В связи с этим использование препаратов, инактивирующих тромбин, а также уменьшающих его образование, представляется чрезвычайно важным при ОКС. Среди препаратов, инактивирующих тромбин, наиболее известен гепарин, который является непрямым ингибитором тромбина, так как для осуществления антикоагулянтного действия ему необходим кофактор — антитромбин III. Использование различных способов деполимеризации гепарина позволило создать гепа-рины с низким молекулярным весом (ГНМВ), которые являются фрагментами молекулы нефракциониро-ванного гепарина (НФГ). ГНМВ, так же как и НФГ, являются непрямыми ингибиторами тромбина, так как для осуществления антикоагулянтной функции им необходим кофактор антитромбин III. Комплекс гепарин—AT III инактивирует несколько активированных факторов свертывания: тромбин(П), Ха, ХIIа, XIa, IXa. Однако основными являются тром-бин(П) и факторы Ха. Механизмы ингибирования тромбина и фактора X антитромбином III (AT III) имеют некоторые различия. Для ингибирования тромбина гепарин должен связаться и с AT III, и тромбином, причем для связи с тромбином молекула гепарина должна быть длиной не менее 18 сахарных остатков. Для ингибирования фактора Ха также необходима связь гепарина с AT III, но связи гепарина с фактором Ха не нужно. Из этого следует, что длины короткой молекулы гепарина, какую имеют ГНМВ, недостаточно для связи с тромбином. Именно это свойство объясняет преимущественную активность анти-Ха фактора у ГНМВ, таким образом ГНМВ ингибируют каскад коагуляции на этапе, предшествующем образованию тромбина. Уменьшение размеров молекулы привело к улучшению биодоступности ГНМВ, составляющей при подкожном введении около 90 % (у НФГ — 30 %), что обеспечивает стабильный и предсказуемый антикоагулянтный эффект и не требует лабораторного мониторинга. Применение гепарина в лечении ОКС без подъемов ST стало общепризнанным с начала 90-х годов. Результаты двух больших исследований, выполненных группой П.Теру в Канаде в 1988 и 1993 гг. убедительно продемонстрировали, что назначение гепарина больным НС достоверно уменьшает суммарную частоту развития ИМ, рефрактерной к лечению стенокардии и смерти от карди-альных причин. Следует особо подчеркнуть, что эффективность гепарина при ОКС без подъемов ST показана лишь для внутривенного способа введения препарата в дозах, увеличивающих показатель АЧТВ в 1,5—2,5 раза от исходного [Neri Serneri et al., 1995]. Эффективность подкожного введения гепарина нельзя считать доказанной, так как лишь в одном исследовании SESAIR были продемонстрированы похожие эффекты при внутривенном и подкожном способах введения гепарина. Учитывая положительное влияние дезагрегантов на исход ОКС без подъемов ST, логичным представляется сочетание антитромбоцитарных препаратов и гепарина. В 1996 г. Oler и соавт. опубликовали результаты метаанализа 6 исследований, посвященных сравнению аспирина и комбинации аспирина с гепарином в отношении профилактики ИМ и смерти у больных с НС, показавшие, что комбинация аспирина с гепарином уменьшает риск смерти и развития инфаркта на 33 %, при сравнении с терапией одним аспирином. П.Те-ру и соавт. в 1992 г. описали феномен отмены гепарина при его монотерапии, выражающийся в увеличении вероятности сердечно-сосудистых эпизодов в первые 5 дней после отмены гепарина. При комбинации аспирина с гепарином подобного явления описано не было. Все это дает основание рекомендовать сочетание аспирина и гепарина в терапии больных ОКС без подъемов ST. ГНМВ отличаются друг от друга по физико-химическим, биологическим и фармакокинетическим свойствам и прежде всего по соотношению анти-Ха/антитромбиновая активность, которая является наибольшей у эноксапарина и надропарина. Это обусловлено различной технологией их производства, в связи с этим нельзя экстраполировать клинические результаты, полученные с одним из ГНМВ, на других представителей этого семейства. При лечении ОКС без подъема ST изучалась эффективность трех ГНМВ: эноксапарина (клексана), надропарина (фраксипа-рина) и дальтепарина (фрагмина). Сравнение эффективности обычного или нефракционированного гепари- на (НФГ) и ГНМВ у больных ОКС без подъема ST проведено в ряде исследований. Дальтепарин сравнивался в исследованиях fric и frisc II, над-ропарин в исследовании fraxis и эноксапарин в исследованиях essence и TIMI 11В. Несмотря на то что все исследования были запланированы с одинаковой целью, проведение сравнения эффективности различных ГНМВ по их результатам невозможно, так как имеются существенные различия в дизайнах исследований. Так, в исследовании FRIC открытая оценка эффективности терапии в острую фазу лечения (5—7 дней) не была первичной целью исследования, кроме того, НФГ в последние дни терапии назначался подкожно. Более того, больные, включаемые во FRIC, имели невысокий риск развития сердечно-сосудистых эпизодов (доля больных с ИМ без Q составляла всего 16 %), в то время как в исследованиях essence и timi 11В соответственно 21 и 35 %. Это имеет значение, так как эффективность антитромботи-ческой терапии в большей степени выражена у больных с высоким риском развития осложнений. Особенности исследований с эноксапари-ном заключаются в более коротком периоде лечения: НФГ в среднем около 3 дней, эноксапарином — от 3 до 4,5 дня, а кроме того, в essence и timi 1 IB было включено существенно больше больных с ИМ без Q и чаше применялись хирургические способы лечения. В большинстве исследований, посвященных исследованию эффективности ГНМВ при ОКС без подъемов ST, в качестве конечной точки использовалась суммарная частота таких событий, как сердечно-сосудистая смерть, инфаркт миокарда, рецидив стенокардии. В исследовании timi 11В дополнительно учитывали потребность в срочной реваскуляризации миокарда, а в исследовании fraxis частоту рефрактерной стенокардии. В настоящее время считается установленным, что надропарин и даль- тепарин сравнимы по эффективности с НФГ, это было показано в исследованиях fric, frisc II и fraxis. Исследования essence и timi 11В, проведенные с эноксапарином, показали его преимущества перед НФГ в отношении снижения суммарной частоты таких событий, как смерть, ИМ и рецидивирующая стенокардия. Объединенный анализ исследований essence и timi 11В, проведенный Antman и соавт. в 1999 г., обнаружил, что назначение эноксапарина по сравнению с НФГ на 20 % снижает суммарную частоту смерти и нефатального ИМ. Активация свертывания крови обнаруживается дольше, чем клинические признаки обострения ИБС, это создает предпосылки к удлинению сроков лечения ингибиторами тромбина. Однако вопрос об оптимальной длительности гепариноте-рапии у больных ОКС без подъема SТ до сих пор открыт. Исследование fraxis не обнаружило преимуществ удлинения срока лечения фраксипа-рином до 2 нед, не исключено, что это могло быть связано с относительно "легкими" больными ОКС, включенными в исследование (смертность в группе плацебо за вторую неделю терапии составляла всего 1,4 %), так как вероятность обнаружения дополнительного эффекта на небольшой группе больных с низким риском невысока. В исследовании timi 11В у половины больных лечение эноксапарином было продлено до 5 нед в дозе 40 мг дважды в день, при этом положительных эффектов на конечные точки обнаружено не было, но следует учитывать, что доза эноксапарина была уменьшена и не адаптирована к весу больного, а кроме того, 40 % больных с высоким риском осложнений были исключены из длительной программы терапии, так как были подвергнуты процедурам реваскуляризации миокарда. В этом исследовании эффективность длительной терапии ГНМВ изучалась у популяции с низким риском осложнений. В единственном исследовании frisc II продление лечения фрагмином до 90 дней снижало риск развития ИМ, смерти и потребности в АКШ в 1-й месяц лечения. По мнению экспертов-кардиологов, опрошенных в Европе и Канаде в 1999 г., длительность лечения гепарином больных ОКС без подъемов ST определяется симптомами стенокардии. При консервативном ведении больных период терапии больше, удлинение срока лечения оправдано при рецидивах стенокардии, невозможности выполнения или ожидании хирургического вмешательства. По частоте "больших" геморрагии НФГ и ГНМВ близки, как показало исследование fraxis, число серьезных геморрагии увеличивалось в группе надропарина только при удлинении срока лечения. Как было установлено в исследованиях essence и timi 11В по числу "малых" геморрагии, подавляющее число из которых составляли подкожные экхимозы в местах инъекций, эноксапарин уступает не-фракционированному гепарину. На сегодняшний день установлено, что больные с ОКС без подъемов ST, при отсутствии противопоказаний должны получать гепарин: либо нефракционированный внутривенно под контролем АЧТВ, добиваясь его удлинения в 1,5—2,5 раза, либо низкомолекулярные гепарины. ГНМВ можно вводить подкожно, дозу подбирать по весу больного, без специального лабораторного контроля, что, безусловно, удобнее для больного и медицинского персонала. При этом эффективность дальтепарина и надропарина не меньше, чем у НФГ, а эффективность эноксапарина превышает эффективность НФГ. Эффективность прямого ингибитора тромбина — гирудина изучалась в трех исследованиях: oasis-1, oasis-2 и gusto IIB. Их объединенный анализ не обнаружил преимуществ гирудина перед НФГ у больных ОКС без подъемов ST. В настоящее время гируди- ны не рекомендованы к применению при ОКС без подъемов ST. В соответствии с рекомендациями Европейского общества кардиологов их применение возможно лишь при тромбо-цитопении, вызванной гепарином. Применение тромболитических препаратов при ОКС без подъемов ST не оправдано. Как сообщают Braunwald и соавт. (1993), в исследовании TIMI-IIIa было показано, что хотя на фоне введения т-АП ангио-графическая картина в стенозирован-ном участке артерии, "ответственном" за обострение болезни, улучшается, но это не сопровождается повышением основного показателя оценки эффективности терапии НС — частоты развития ИМ. Близкие результаты были получены и при использовании у больных НС комплексов стрепто-киназы с ацилированным плазмино-геном [Bar et al., 1992]. Более того, после завершения timi IIIb, где в группе больных НС, получавших т-АП, оказалось больше ИМ, чем в группе плацебо, стал обсуждаться возможный вред тромболитиков при НС. В связи с установленной ролью активации свертывания крови в патогенезе ОКС, а также упомянутыми выше фактами, указывающими на необходимость длительной терапии антикоагулянтами у больных, перенесших ОКС, а также появлением возможности повысить безопасность терапии непрямыми антикоагулянтами (НАКГ) в последние годы возобновился интерес к этой группе антитромботических средств. Механизм действия непрямых (оральных) антикоагулянтов связан с уменьшением образования печенью четырех витамин К-зависимых факторов свертывания крови: II, VII, IX и X, что в конечном итоге приводит к уменьшению образования тромбина. Оральные АКГ, помимо указанных функций, ограничивают кар-боксилирование таких регуляторных белков, как протеины С и S, и тем самым оказывают влияние на функцию противосвертывающей системы. К оральным АКГ относят производные индандиона (фенилин) и кумарина (варфарин, неодикумарин, синкумар, аценокумарол). Наиболее широко применяются производные кумарина — варфарин, синкумар, что связано с началом и длительностью их действия, а также с предсказуемостью эффектов препаратов. Варфарин связывается с белками плазмы и быстро накапливается в печени. Из-за того что отношение доза/ответ различается у отдельных больных, доза препарата должна подбираться индивидуально. В связи с индивидуальными особенностями всасывания, метаболизма печени и почек доза варфарина, так же как и других НАКГ, регулируется по величине протромбинового времени — показателя, увеличивающегося в ответ на угнетение трех из четырех витамин К-зависимых факторов свертывания: протромбина II, VII и X. Для стандартизации показателя протромбинового времени, принимая во внимание разные препараты тром-бопластина, используемые в лабораториях, экспертами ВОЗ был рекомендован показатель INR (International Normalisation Ratio), в русской транскрипции MHO (Международное Нормализованное Отношение). MHO позволяет учесть особенности разных тромбопластинов, выражающиеся в так называемом Международном Индексе Чувствительности (МИЧ), указываемом на препарате тромбопластина. MHO = (протромби-новое время больного/протромбино-вое время нормальной плазмы)мич. Величина MHO прямо пропорциональна степени антикоагуляции. Многочисленные исследования, проведенные с НАКГ, позволили установить оптимальный терапевтический уровень MHO, находящийся в диапазоне от 2,0 до 3,0. При этом уровне MHO достигается оптимальное соотношение профилактики тромбоэмболии и риска кровотечений. В последние несколько лет опубликованы результаты четырех исследований, в которых изучалась эффективность оптимальных терапевтических доз варфарина (MHO = = 2,0—3,0) у больных, перенесших ОКС. В исследование ASPECT (Anticoagulants in the Secondary Prevention of Events in Coronary Thrombosis-2) было включено 993 больных с ОКС: у 43 % из них был крупноочаговый ИМ, у 41 % - ИМ без Q, у 14 % -НС. В среднем на 7-й день от начала ОКС больные были рандомизирова-ны в три группы: аспирин 80 мг, вар-фарин (MHO = 3,0—4,0) и комбинация аспирин + варфарин (MHO = = 2,0—2,5). Через 1 год наблюдения суммарная частота смерти, ИМ и инсульта соответственно составила 9,2/5,1/5,2 %, т.е. снижение ОР в обеих группах больных, лечившихся варфарином, составило 45 %. Частота серьезных геморрагических осложнений соответственно составила 0,9/2,1/0,9 %; р > 0,05. Таким образом, добавление варфарина к аспирину (MHO = 2,0—2,5) и монотерапия варфарином (MHO = 3—4) имели преимущества перед монотерапией аспирином у больных, перенесших ОКС без статистически достоверного увеличения частоты серьезных геморрагии. Исследование apricot-2 (Antithrombotics in the Prevention of Reocclusion in Coronary Thrombolysis-2) было проведено с целью изучения эффективности варфарина в отношении поддержания проходимости инфарктсвя-занной артерии (ИСА) у больных ИМ после успешного тромболизиса. В исследование было включено 306 больных в возрасте до 76 лет с восстановлением кровотока в ИСА (III степень по timi) после тромболизиса, проведенного в первые 6 ч ИМ. Больные были рандомизированы в две группы: аспирин 80 мг в сутки и аспирин + варфарин (MHO = 2—3). Через 3 мес всем больным была повторена КАГ и оценена частота реок-клюзий ИСА (0—1 степень по timi). В группе аспирина частота реокклю-зий составила 30 %, в группе аспирин + варфарин 18 %, снижение относительного риска составило 40 %; р = 0,02. Частота серьезных геморрагии была соответственно 1 и 2 %. Таким образом, данное исследование показало, что комбинация аспирина с варфарином (MHO = 2—3) имеет преимущества перед монотерапией аспирином в отношении возникновения реокклюзий ИСА у больных ИМ после тромболизиса, при отсутствии разницы в числе серьезных геморрагических осложнений. Интересными представляются результаты исследования OASIS-2, одной из целей которого было оценить эффективность варфарина у больных после ОКС без подъемов ST в течение 5 мес наблюдения. В исследование было включено 3703 больных, которые после терапии ингибиторами тромбина были рандомизированы в группу аспирина и комбинации аспирина и варфарина (MHO = 2,0— 3,0). Результаты данного исследования отражают проблему терапии НА-КГ в целом, при анализе всех больных оказалось, что снижение ОР смерти и ИМ составило всего 11 %, а смерти, ИМ и рефрактерной ишемии — 6 %, что было статистически недостоверным, при этом приверженность терапии варфарином на протяжении наблюдения в ряде стран была низкой. При отдельном анализе стран, в которых более 70 % больных в течение 5 мес продолжали получать варфарин, результаты оказались более впечатляющими: снижение ОР смерти и ИМ в группе варфарина составило 31 %; р = 0,03, а смерти, ИМ и рефрактерной ишемии — 26 %; р = 0,01. Частота серьезных геморрагии в группе варфарина была невысокой и составила 2,6 против 1 % в группе аспирина. 2 сентября 2001 г. в Стокгольме на XXIII конгрессе ЕОК были доложены результаты исследования WARIS, организованного в Норвегии, целью которого было сравнительное изуче- ние аспирина (160 мг), варфарина (MHO 2,8—4,2) и комбинации аспирин 75 мг + варфарин (MHO 2,0—2,5) у больных, перенесших ОКС. Исследование было открытым, рандомизация больных проводилась при выписке из стационара, срок наблюдения составил 4 года. Оценивалась суммарная частота смерти от всех причин, не фатального ИМ и ише-мического инсульта. Всего в исследование было включено 3630 больных, средний возраст 60 лет, большинство (77 %) были мужского пола. У 59 % больных ОКС проявлялся крупноочаговым ИМ, по поводу которого у 54 % была проведена тром-болитическая терапия. Статины при выписке были назначены 77 % больным, b-блокаторы — 74 %. Ингибиторы АПФ получали 29 %, нитраты — 22 %, антагонисты кальция — 13 %, диуретики — 14 % больных. Средний уровень MHO за период наблюдения в группе монотерапии варфарином составил 2,8, в группе аспирин + варфарин — 2,2. Суммарная частота смерти, ИМ и инсульта за 4 года наблюдения составила в группе аспирина 20 %, в группе варфарина 16,7 %, а в группе аспирин + варфарин 15 %. Снижение относительного риска событий в группе варфарина по сравнению с группой аспирина составило 19 %, р = 0,028, а в группе комбинированной терапии по сравнению с группой монотерапии аспирином — 29 %, р = 0,0005. Таким образом, наилучшие результаты в отношении влияния на частоту конечных точек были достигнуты в группе больных, получавших аспирин в дозе 75 мг в сутки в комбинации с варфарином при среднем MHO = 2,2. Частота серьезных геморрагии в группах аспирин, варфарин, аспирин + варфарин составила соответственно 0,15/0,58/0,52 % в год, что было меньше, чем в исследовании CURE при использовании клопидогреля. Резюмируя исследования, посвященные использованию варфарина у больных, перенесших ОКС, следует подчеркнуть, что добавление варфарина (умеренная антикоагуляция, MHO 2,0—2,5) к аспирину в суточной дозе 80 мг уменьшает частоту сердечно-сосудистых эпизодов (aspect, oasis-2, waris-II), уменьшает риск реокклюзий ИСА (apricot-2), и при этом не увеличивает частоты серьезных геморрагии (aspect-2, oasis-2). Монотерапия варфарином (MHO 2,8—3,2) также в большей степени, чем аспирин в дозе 80 мг, снижает риск развития сердечно-сосудистых эпизодов (aspect-2, waris-II). Частота серьезных геморрагии при умеренной антикоагуляции не столь высока, как это отмечалось в более ранних исследованиях с высокой степенью антикоагуляции. В исследовании waris-II в группе аспирина она составила 0,15 % за год, в группе аспирин + варфарин (MHO = 2,2) - 0,52 % за год, в группе аспирин + варфарин (MHO = 2,8) - 0,58 % за год, для сравнения интересны данные о частоте геморрагических осложнений в исследовании сиге, которые составили 3,6 % за 9 мес наблюдения. Таким образом, результаты последних исследований указывают, что достижение умеренной антикоагуляции варфарином (MHO 2,2) усиливает эффективность аспирина у больных, переживших ОКС. Вероятно, эта комбинация особенно целесообразна у больных высокого риска сердечно-сосудистых осложнений в случаях невозможности проведения процедур реваскуляризации миокарда, неэффективности аспирина как средства вторичной профилактики. Стоимость варфарина существенно меньше стоимости клопидогреля, что также немаловажно для нашей страны. Единственной проблемой, ограничивающей широкое и безопасное применение НАКГ в нашей стране, является то, что в большинстве случаев лабораторный контроль за терапией НАКГ осуществляется с помощью протромбинового индекса, что снижает безопасность терапии НАКГ и не должно применяться. Кроме того, терапия подобранной дозой НАКГ требует регулярного (не реже 1 раза в 3 нед) контроля MHO и при необходимости корректировки дозы. В настоящее время созданы портативные приборы индивидуального пользования, позволяющие из капли капиллярной крови определить протромбин и рассчитать MHO, что создает удобства для больного и позволяет повысить безопасность терапии НАКГ. В последние годы созданы новые препараты, ингибирующие каскад коагуляции на разных этапах: ингибиторы комплекса VIIa/тканевый фактор, пентасахариды — синтетические аналоги пентозной последовательности НФГ и ГНМВ, а также прямой пер-оральный ингибитор тромбина — ксимелагатран. Эффективность пен-тасахаридов и ксимелагатрана в настоящее время изучается у больных с острым коронарным синдромом. Литература Лечение острого коронарного синдрома без стойких подъемов сегмента ST на ЭКГ/Российские рекомендации. Разработаны Комитетом экспертов Всероссийского научного общества кардиологов. — М., 2001. Приложение к журналу "Кардиология" № 10, 2001. Acute myocardial infarction: pre-hospital and in-hospital management. The task force on the management of acute myocardial infarction of the European Society of Cardiology //Europ. Heart. J. - 1996. - Vol.17. - P.43-63. Ambrose J.A., Tannenbaum M.A., Alexopouluos D. et al. Angiographic progression of coronary artery disease and the development of myocardial infarction//J. Amer. Coll. Cardiol. — 1998. -Vol. 12. - P. 56-62. Antman E.M., Cohen M., Radley A. et al. Assessment of the treatment effect of enoxaparin for unstable angina/non-Q-wave myocardial infarction: TIMI UB-ESSENCE meta-analy-sis//Circulation. - 1999. - Vol. 100. -P. 1602-1608. Arnesen H. WARIS-II (Warfarin-Aspirin Re-Infarction Study) Presented at the 23d Congress of the European Society of Cardiology. — Stockholm, Sweden, September 2001. Assessment of the Safety an Efficacy of a new Thrombolytic (ASSENT-2) Investigators. Sin- gle-bolus tenecteplase compared with front-loaded alteplase in acute myocardial infarction: The ASSENT-2 double blind randomised trial // Lancet. - 1999. - Vol. 354. - P. 716-722. Badimon J.J., Lettino M., Toschi V. et al. Local inhibition of tissue factor reduces the thrombo-genicity of disrupted human atherosclerotic plaques: Effects of TFPI on plaque thrombo-genicity under flow condition//Circulation. — 1999. - Vol. 14. - P. 1780-1787. Braunwald E., Jones R.H., Mark D.B. et al. Diagnosing and managing unstable angina. Agency for health care policy and research//Circu-lation. - 1994. - Vol. 90. - P. 613-622. Brouwer M. APRICOT-2 (Antithrombotics in the Prevention of Reocclusion in Coronary Thrombolysis)//Presented at the 22nd Congress of the European Society of Cardiology. — Amsterdam, The Netherlands. — September, 2000. Brown B.G., Gallery C.A., Badger R.S. etal. Incomplete lysis of thrombus in the moderate underlying atherosclerotic lesion during intracor-onary infusion of streptokinase for acute myocardial infarction. Quatitave angiographic ob-servations//Circulation. — 1986. — Vol. 73. — P. 653-661. Calvete J.J. Clues for understanding the structure and function of a prototypic human inte-grin: the platelet glycoprotein Ilb/IIIa com-plex//Thromb Hemost. - 1994. - Vol. 72. -P. 1-15. Dangas G., Badimon J.J., Smith D.A. etal. Pravastatin therapy inhyperlipidemia: effects on thrombus formation and the systemic hemostatic profile//J.AC.G. - 1999. - Vol. 33, N 5. - P. 1294-1304. Davies V.J., Bland J.M., Hangartner J.R.W. et al. Factors influencing the presence of absence of acute coronary thrombi in sudden ischaemic death//Europ. heart J. - 1989. - Vol. 10 -P. 203-208. Effects of clopidogrel in addition to aspirin in patients with acute coronary syndromes without ST elevation. The CURE trial investiga-tors//N. Engl. J. Med. - 2001. - Vol. 345. -P. 494-502. Efficacy and safety of tenecteplase in combination with enoxaparin, abciximab, or unfra-tionated heparin: the ASSENT-3 randomised trial in acute myocardial infarction//Lancet. — 2001. - Vol. 338. - P. 605-613. Epilog investigators. Platelet glycoprotein Ilb/IIIa receptor blockade and low dose heparin during percutaneous coronary revascularization. The EPILOG Investigators//N. Engl. J. Med. - 1997. - Vol. 336. - P. 1689-1696. Epistent Investigators. Randomised placebo-controlled and balloon-angioplasty-controlled trial to assess safety of coronary stenting with use of platelet glycoprotein Ilb/IIIa blockade. The Epistent Investigators. Evaluation of platelet Ilb/IIIa inhibitor for stenting//Lancet. — 1998. - Vol. 352. - P. 87-92. Falk E. Why do plaques rupture?//Circulation. — 1992. - Vol. 86. - Suppl. Ill: 111-30—111-42. Farb A., Burke A.P., Tang A.L. et al. Coronary plaque erosion without rupture into a lipid core. A frequent cause of coronary thrombosis in sudden coronary death // Circulation. — 1996. - Vol. 93. - P. 1354-1363. Flugelman M.V., Virmani R., Correct R. et al. Smooth muscle cell abundance and fibroblast growth factors in coronary lesions of patients with nonfatal unstable angina. A clue to the mechanism if transformation from the stable to the unstable clinical state//Circulation. — 1993. - Vol. 88. - P. 2493-2500. Fragmin and fast revascularization during instability in coronary artery disease (FRISC-II) investigators. Long-term low-molecular-mass heparin in unstable coronary artery disease: FRISC-II prospective randomized multicenter study//Lancet. - 1999. - Vol. 354. - P. 701— 707. Fragmin during Instability in Coronary Artery Disease (FRISC) study group. Low-molecular-weight heparin during instability in coronary artery disease//Lancet. — 1996. — Vol. 347. — P. 561-568. Fraxis study group. Comparison of two treatment durations (6 days and 14 days) of a low molecular weight heparin with a 6-day treatment of unfractionated heparin in the initial management of unstable angina or non-Q wave myocardial infarction.—Fraxis//Europ. Heart J. - 1999. - Vol. 20. - P. 1553-1562. Fuster V. Mechanisms leading to myocardial infarction: Insights from studies of vascular bi-ology//Circulation. - 1994. - Vol. 90. -P. 2126-2146. Ginsburg D., Sadler J.E. Von Willebrand disease: a data base of point mutation, insertions and deletions//Thromb Haemost. — 1993. — Vol. 69. - P. 177-184. Gruppo Italiano per lo Studio Delia Soprav-vivenza NeU'Infarto Miocardico. GISSI-2: A factorial randomised trial of alteplase versus streptokinase and heparin versus no heparin among 12,490 patients with acute myocardial infarction//Lancet. - 1990. - Vol. 336. -P. 65-71. Lefkovits J., Plow E.F., Topol E.J. Platelet glycoprotein Ilb/IIIa receptors in cardiovascular medicine//N. Engl. J. Med. - 1995. -Vol. 332. - P. 1553-1559. Management of acute coronary syndromes: acute coronary syndromes without persistent ST segment elevation//Eur. Heart J. — 2000. — Vol. 21. - P. 1406-1432. Meta-analysis by the FTT collaborative group//Lancet. — 1994. - Vol. 343. — P. 311-322. Meyr D., Girma J. P. Von Willebrand factor: structure and function//Thromb. Haemost. — 1993. - Vol. 70, N 1. - P. 99-104. Neri Serneri G.G., Modesti P.A., Gensini G.F. et al. Randomised comparison of subcutaneous heparin, intravenous heparin, and aspirin in unstable angina//Lancet. — 1995. — Vol. 345. — P. 1201-1204. OlerA., Whooley M., OlerJ., Grady D. Adding heparin to aspirin reduces the incidence of myocardial infarction and death in patients with unstable angina. A meta-analysis//J.A.M.A. — 1996. - Vol. 276. - P. 811-815. Paragon investigators. International, randomized controlled trial of lamifiban, heparin, or both in unstable angina. The PARAGON in-vestigators//Circulation. — 1998. — Vol. 97. — P. 2386-2395. Plow E.F., D'Souza S.E., Ginsberg M.H. Ligand Binding to GPIIb-IIIa: a status report//Semin. Thromb. Hemost. - 1992. - Vol. 18. - P. 324-332. Prism-plus study investigators. Inhibition of platelet glycoprotein Ilb/IIIa receptor with tor-ofiban in unstable angina and non-Q-wave myocardial infarction. Platelet receptor inhibition in ischemic syndrome management in patients limited by unstable signs and symptoms (PRISM-PLUS) study investigators//N. Engl. J. Med. - 1998. - Vol. 338. - P. 1488-1497. Pursuit Investigators. Inhibition of platelet glycoprotein Ilb/IIIa with eptifibatide in patients with acute coronary syndromes. The PURSUIT trial investigators. Platelet Glycoprotein Ilb/IIIa in Unstable angina: receptor suppression using Integrilin therapy//N. Engl. J. Med. — 1998. - Vol. 339. - P. 436-443. Randomised placebo-controlled trial of abcix-imab before and during coronary intervention in refractory unstable angina: the CAPTURE study//Lancet. - 1997. - Vol. 349. -P. 1429-1435. Randomised placebo-controlled trial of effect of eptifibatide on complications of percutaneous coronary intervention: IMPACT-II//Lancet. — 1997. - Vol. 349. - P. 1422-1428. Ruggeri Z.M., Ware J. The structure and function of von Willebrand factor//Thromb. Haemost. - 1992. - Vol. 67. - P. 594-599. The EPIC Investigators. Use of A Monoclonal Antibody Directed Against The Platelet Glycoprotein Ilb/IIIa Receptor In High-Risk Coronary Angioplasty//N. Engl. J. Med. — 1994. — Vol. 330. - P. 956-961. The Global Use Strategies to Open Occluded Coronary Arteries (gusto III) Investigators. A comparison of reteplase with alteplase for acute myocardial infarction//N. Engl. J. Med. — 1997. - Vol. 337. - P. 1118-1123. The Organization to Assess Strategies for Ischemic Syndromes (OASIS) investigators. Effects of long-term, moderate-intensity oral anticoagulation in addition to aspirin in unstable angina// J. Amer. Coll. Cardiol. — 2001. — Vol. 37. - P. 475-484. The Restore Investigators. Effects of platelet glycoprotein Ilb/IIIa blokade with tirofiban on adverse cardiac events in patients with unstable angina or acute myocardial infarction undergoing coronary angioplasty//Circulation. — 1997. - Vol. 96. - P. 1445-1453. Van Belle et a /.//Circulation. — 1998. -Vol. 97. - P. 26-33. Van Es RF ASPECT (Anticoagulants in the Secondary Prevention of Events in Coronary Thrombosis-2) Presented at the 22nd Congress of the European Society of Cardiology. — Amsterdam, The Netherlands. — September 2000. Дата добавления: 2015-02-06 | Просмотры: 911 | Нарушение авторских прав |