|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
ПУТЬ КЛАССА IIАнтиген, Любой чужеродный материал, захваченный в результате фагоцитоза и эндоцитоза, попадает в вакуоли эндоцитарного пути, или эндосомы, к которым относятся также кислые лизосомы. Различные протеолитические ферменты могут действовать при соответствующих значениях рН. При микробной инфекции цельный микроб подвергается разрушению в этих условиях. sIg — поверхностный иммуноглобулин, с помощью которого В-лимфоциты связывают антиген, который затем подвергается эндоцитозу. ГКГС II — молекула ГКГС класса II. Состоит из двух цепей, образующих между концевыми доменами a1- и b1-цепей пептидсвязывающий желобок. Наибольшая специфичность связана с р-цепью. В процессе синтеза молекулы связывание предупреждается специальным белком,названным инвариабельной цепью (на рисунке — Инв.), которая впоследствии отделяется и заменяется продуцируемыми пептидами в эндосомах. Пептиды. Молекулы ГКГС класса II способны присоединять пептиды длиной до 20 аминокислот, в том числе происходящие из микробов в эндосомах и «свои» пептиды (многие их которых происходят из самих молекул ГКГС). CD4 — корецептор, взаимодействующий с молекулой ГКГС класса II. Экспрессирован на Т-хелперах, взаимодействует с В-лимфоцитами или макрофагами. Таким образом, тип Т-клеточного ответа определяется следующими факторами: 1) тип Т-клетки — CD8 цитотоксический или CD4 хелпер; 2) класс молекулы ГКГС — I или II; 3) цитоплазматическое или эндосомальное происхождение пептида, связываемого молекулой ГКГС; 4) инфекция — вирусная или микробная. Существуют, конечно, и исключения (рис. 26-29). 18. ГУМОРАЛЬНЫЙ ИММУННЫЙ ОТВЕТ
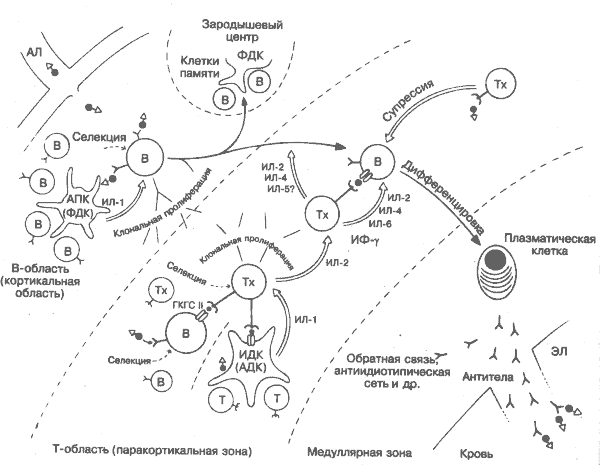
Животные, которые родились и выращивались в безмикробных условиях, практически не содержат иммуноглобулинов в сыворотке, но уровень их быстро достигает обычных показателей (10-20 мг/мл, или 6*106 молекул) сразу после создания нормального микробного окружения, Это показывает, что антитела синтезируются только в ответ на стимуляцию чужеродными антигенами. Процесс известен как антительный ответ. На рисунке схематично изображён срез лимфатического узла. Антиген поступает из тканей (слева вверху), и антитела освобождаются в кровь (справа внизу). Антиген составляет комбинацию из 2 детерминант (компонентов): гаптенной (черные кружки) и несущей (белые треугольники). В-лимфоцит распознаёт гаптенную детерминанту и синтезирует специфичные к ней антитела. Несущая детерминанта взаимодействует с Т-лимфоцитом и необходима для полной активации В-клетки. Обычно антигены имеют множество различных гаптенных и несущих детерминант (например, вирусы, бактерии и др.), тогда как небольшие молекулы могут действовать только как гаптены (например, токсины). Но даже небольшая, но хорошо выраженная антигенная детерминанта стимулирует гетерогенную популяцию В-лимфоцитов, каждая из которых продуцирует антитела со слабыми различиями в специфичности и аффинитете. Основными стадиями иммунного ответа являются распознавание и переработка антигена (рис. 17), селекция соответствующих индивидуальных Т- и В-клеток, их пролиферация в клоны и дифференцировка в функционально зрелые клетки. Каждый из перечисленных этапов характеризуется множественными межклеточными взаимодействиями, опосредуемыми в основном цитокинами (белые стрелки). Существуют и другие регулирующие факторы, но их значение пока неясно. Большая часть межклеточных взаимодействий проходит в лимфатических узлах или селезёнке, но образование антител — только в лимфоидной ткани. Повторный ответ на тот же антиген, или ответ по вторичному типу, происходит гораздо быстрее и эффективнее благодаря большему количеству предшественников В- и Т-клеток. увеличившемуся разнообразию классов иммуноглобулинов и более высокому аффинитету антител, Ответ по вторичному типу означает, что в организме развилась иммунная память об антигене, что является целью большинства вакцин (рис. 41). АЛ — афферентный лимфатический сосуд, по которому антигены и нагруженные антигенами клетки поступают в лимфатический узел (рис. 11). АПК — антигенпредставляющая клетка. Для запуска лимфоцитов в активацию антиген должен быть представлен на поверхности специализированных клеток. Различные дендритные клетки лимфоидных тканей, клетки Лангерганса в коже и др. (рис. 7) выполняют эту функцию: часть из них выделяет ИЛ-1. Клетки, представляющие антиген Т-лимфоцитам, должны иметь поверхностные молекулы ГКГС класса II. За исключением небольших пептидов, которые могут непосредственно связываться с молекулами ГКГС класса II, другие антигены должны быть переработаны (расщеплены до пептидов) (рис. 17), ФДК — фолликулярная дендритная клетка, специализированная для представления антигена В-лимфоцитам в В-клеточных фолликулах. ИДК — интердигитальная дендритная клетка, специализированная для представления антигена Т-лимфоцитам в Т-клеточ-ной зоне или в паракортикальном слое. Селекция. Лишь небольшая часть лимфоцитов распознаёт и связывает специфический антиген. Следовательно, эти молекулы селекционируются антигеном. Связывающими рецепторами являются поверхностные иммуноглобулины В-клеток и Т-клеточный рецептор в случаях с Т-клетками, которые распознают антиген вместе с молекулой ГКГС (рис. 14, 17). Клональная пролиферация. Отобранные В-лимфоциты начинают активно делиться с образованием клонов идентичных клеток. Основным стимулятором пролиферации является растворимый продукт АПК — ИЛ-1. Для В-клеточной пролиферации также требуются Т-клеточные цитокины и взаимодействие через адгезивные молекулы (рис. 14). Пролиферация Т-лимфоцитов усиливается другими растворимыми факторами (ИЛ-2), которые они продуцируют сами (рис. 23). Сочетание селекции антигенами с последующей клональной пролиферацией приводит в целом к ответу лимфоцитов, получившему название «клональная селекция». Дифференцировка. Пролиферирующие В-лимфоциты становятся чувствительными к факторам, выделяемым Т-хелперами. Идентифицированным факторам присвоены номера интерлейкинов, но многие известные цитокины в той или иной мере усиливают рост или функции В-лимфоцитов. Некоторые антигены, особенно антигены с многочисленными повторяющимися детерминантами, способны стимулировать дифференцировку В-лимфоцитов без помощи Т-клеток. Такие антигены называют тимуснезависимыми (Т-независимыми). Обычно это бактериальные полисахариды. Как правило, они стимулируют лишь IgM-ответ, представляющий более примитивную форму ответа. Плазматические клетки. Для синтеза и секреции антител в В-лимфоците развиваются рибосомы и эндоплазматический ретикулум, отчего цитоплазма становится базофильной, а ядро располагается эксцентрично. Плазматические клетки, живущие только несколько дней, способны секретировать до 2000 молекул антител в секунду. ЭЛ — эфферентный лимфатический сосуд, через который антитела, секретируемые в медуллярном слое, поступают в лимфу, а затем в кровь и распространяются по всему организму. Клетки памяти. Некоторые В-лимфоциты не дифференцируются в плазматические клетки-антителопродуценты, а сохраняются как клетки памяти, увеличение которых и быстрое реагирование формируют высокоэффективный вторичный ответ. В-клетки памяти мало отличаются от их предшественников (больше поверхностных Ig, более вероятная циркуляция в крови), но сохраняют туже специфичность к антигену. Генерация В-клеток памяти происходит в зародышевых центрах и требует присутствия комплемента. Также необходимы Т-клетки, так как Т-независимый иммунный ответ не оставляет иммунной памяти. Т-хелперы также развиваются в клетки памяти, но где это происходит, ещё не выяснено. Неизвестно также, как долго живут клетки памяти и нуждаются ли они в повторной стимуляции. Супрессия. Некоторые Т-клеточные цитокины, особенно те, которые стимулируют макрофаги, подавляют функцию В-клеток. Этим можно объяснить некоторые случаи супрессорного действия Т-клеток. Существование отдельной линии Т-супрессоров в настоящее время не подтверждается. Отрицательная обратная связь. Антитела, особенно IgG, могут подавлять антителообразование путём элиминации антигена или предупреждения стимуляции В-клеток. Антиидиотипическая сеть. Известный иммунолог Н. Ерне предположил (впоследствии это подтвердилось), что идиотипы антител (уникальные по конфигурации участки активных центров) способны выполнять роль антигена и вызывать В- и Т-клеточный ответ, в результате чего иммунная реакция постепенно затухает. Это привело к появлению интересной концепции сети антиидиотипических рецепторов, согласно которой антиидиотипические антитела несут в себе «внутренний образ» чужеродных антигенов (рис. 22). Однако истинная роль идиотипантиидиотипических сетей в регуляции обычного антительного ответа ещё неясна. Возможно, наиболее значимым в регуляции продукции антител является удаление антигена. 19. ВЗАИМОДЕЙСТВИЕ АНТИГЕНА И АНТИТЕЛА И ИММУННЫЕ КОМПЛЕКСЫ
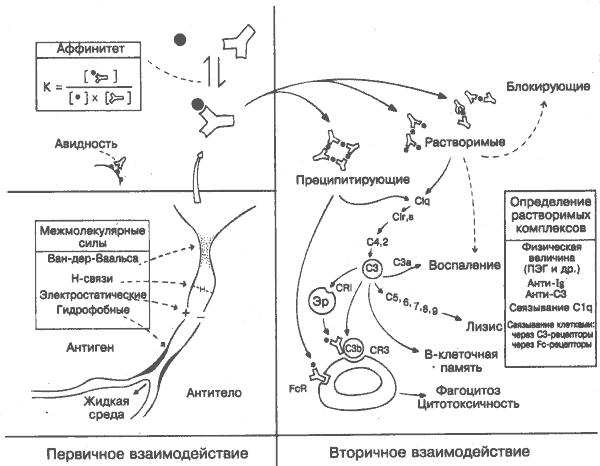
Антиген стимулирует синтез антител, которые соединяются с этим антигеном. Оба процесса основаны на взаимной комплементарности конфигурации антигенной детерминанты и антигенсвязываюшего участка антитела, образованного гипервариабельными участками тяжёлой и лёгкой цепей (рис. 16). Чем ближе это соответствие, тем интенсивнее нековалентные силы между ними (гидрофобные, электростатические и т.д.; на рисунке слева внизу) и тем выше аффинитет (слева вверху). Связывание антигена двумя активными центрами антитела увеличивает прочность соединения и характеризуется авидностью. Способность связываться только с определённой антигенной детерминантой характеризует специфичность антител. Специфичность основана на огромном числе различающихся по конфигурации активных участков, которое заложено в V-генах и ещё более увеличивается в результате соматических мутаций (рис. 15). В результате в организме образуются миллионы антител различной специфичности, что составляет антительный репертуар. Последствия соединения антитела с антигеном могут быть различными. Иногда, как в случае тех микроорганизмов и токсинов, которым для проявления патогенного свойства необходимо прикрепиться к поверхностным рецепторам клетки,нейтрализующего действия антител, связывающих антигенные детерминанты, оказывается достаточно. Чаще всё-таки требуется взаимодействие антител с другими эффекторными агентами, такими, как комплемент или фагоциты. О значении этого вторичного взаимодействия говорит уже то, что проявления дефицита комплемента и миелоидных клеток приводят почти к таким же последствиям, как дефицит антител (рис. 39). Соединение из антигена и антитела называют иммунным комплексом. В зависимости от природы и соотношения антигена и антител иммунные комплексы могут быть мелкими (растворимыми) или крупными (преципитирующими) (справа вверху). Обычно они удаляются фагоцитарными клетками в результате взаимодействия Fc-участка антитела с комплементом и поверхностными рецепторами фагоцитов (в центре внизу; см. также рис. 8). В некоторых случаях комплексы циркулируют в крови и вызывают воспалительное поражение органов (рис. 34) или подавляют иммунитет, например, к опухолям или паразитам. Обнаружение иммунных комплексов и идентификация входящих в их состав антигенов представляют большой практический интерес и проводятся с помощью многочисленных методик. Дата добавления: 2014-12-12 | Просмотры: 1069 | Нарушение авторских прав |