|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
СПЕЦИФИЧЕСКАЯ ИММУНОСУПРЕССИЯБезотносительно к лежащим в её основе механизмам специфическая супрессия традиционно называется усилением, если она опосредована антителами, и толерантностью, если вызвана антигеном. Между тем инъекция антигена может оказаться эффективной только потому, что стимулировала синтез антител. В такой ситуации лучше оставить терминологию и лишний раз подробно рассмотреть, что же происходит в действительности. Антитела к антигенам клеток-мишеней, по-видимому, способны блокировать детерминанты молекул класса II, препятствуя таким образом отторжению опухоли. Переливание крови, предшествующее пересадке почки, способствует её приживлению (рис. 37). Антирезусные антитела предотвращают сенсибилизацию резус-отрицательной матери, устраняя резус-положительные клетки. Антитела к идиотипическим рецепторам теоретически способны блокировать распознавание антигена как В-, так и Т-клетками. Однако пока нет уверенности, окажется ли эта способность достаточно эффективной при трансплантации и аутоиммунной патологии. Клональная элиминация, или классическая толерантность, создаётся in vitro при использовании антигена, конъюгированного с радиоизотопами или токсическими препаратами. Клетки, специфически связавшие отравленные антигены, погибают. Из-за некоторого сходства с действиями римских гладиаторов способ получил название ретиарной терапии. На сегодняшний день достигнуты некоторые успехи в её применении in vivo. Возможно, что супрессия, вызванная антипролиферативными препаратами (циклофосфан, циклоспорин А) в присутствии антигена, содержит элемент специфической клональной элиминации. 39. ИММУНОДЕФИЦИТЫ
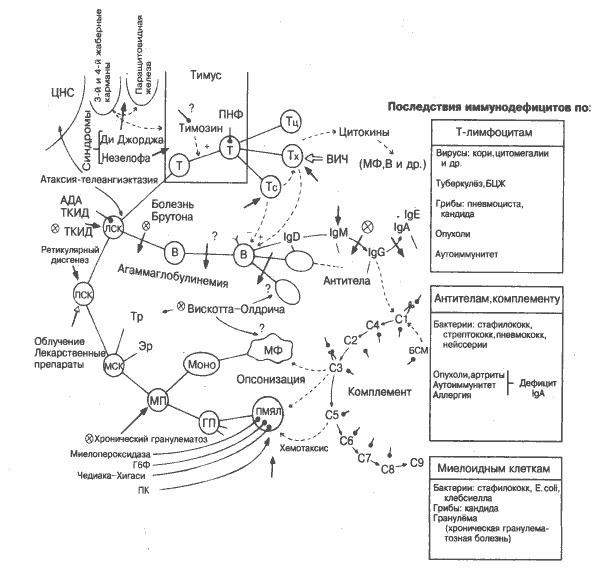
Полноценность иммунного ответа основана на взаимодействии множества клеток и молекул, и многочисленные их дефекты снижают эффективность иммунитета, во многих случаях повышая чувствительность к инфекции (на рисунке справа). Дефекты Т-лимфоцитов (вверху), антител и/или комплемента (в центре) и миелоидных клеток (внизу) различными путями приводят к разным заболеваниям. Иммунодефициты (ИД) подразделяют на первичные (врождённые), генетически обусловленные, и вторичные по отношению к другим состояниям (химиотерапия, инфекция, нарушение питания). Среди первичных ИД многие связаны с Х-хромосомой, т.е. наследуются мальчиками от матерей, указывая на то, что непарная часть Х-кромосомы содержит некоторые иммунологически важные гены (на рисунке дефекты, вызванные Х-сцеплением, помечены крестиком в круге). В большинстве случаев ИД характеризуются множеством частичных разрозненных дефектов на клеточном уровне. В некоторых случаях на определённых стадиях нарушается дифференцировка клеток (чёрные стрелки), но чаще имеется комбинация дефектов. При некоторых заболеваниях может быть идентифицирован недостающий генный продукт, например, отдельные компоненты комплемента, ферменты нейтрофилов и лимфоцитов (чёрные точки). Исследования в этой области крайне важны не столько для классификации ИД на биохимической основе, сколько для заместительной терапии. Частоту ИД связывают с понятием нормального состояния. Некоторые формы явного иммунодефицита наблюдаются у более чем 1 из 1000 человек. Эти показатели оказываются явно заниженными, если учитывать, насколько часто так называемые здоровые люди подвергаются простудным заболеваниям, фурункулёзу, ангинам и др. На самом деле иммунную природу этих вторичных заболеваний ещё предстоит выяснить (подробнее см. рис. 4 и 9). Дата добавления: 2014-12-12 | Просмотры: 935 | Нарушение авторских прав |