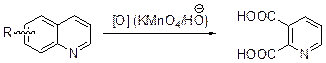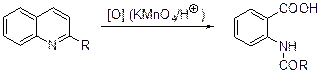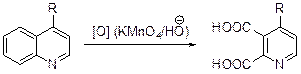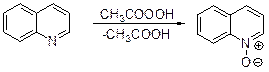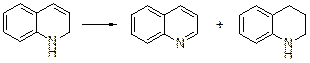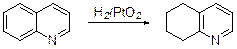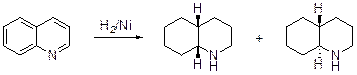|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Реакции окисления и восстановления в ряду хинолина.Хинолин устойчив к действию большинства мягких окислителей. Даже с водной хромовой кислотой он реагирует медленно. Водный раствор перманганата калия окисляет хинолин и алкилхинолины с заместителями в карбоциклическом фрагменте до хинолиновой (пиридин-2,3-дикарбоновой) кислоты.
2-Алкил- и 2-арилхинолины окисляются перманганатом калия в кислой среде до N-ацил- или N-ароилантраниловых кислот.
Окисления 3-алкилхинолинов сопровождается разрушением обоих колец и образованием щавелевой кислоты, оксида углерода (IV) и аммиака. 4-Алкилхинолины дают хинолиновые кислоты с алкильным заместителем у С(4).
Гипохлорит натрия окисляет хинолин до 2-хинолона. Эта реакция подробно рассмотрена в разделе 2.7.3.2. Перуксусная кислота окисляет хинолин до хинолин-N-оксида.
Сам хинолин, а также 5-, 6-, 7- или 8-алкилхинолины, восстанавлива-ются преимущественно по гетероциклическому ядру. Использование в качестве восстановителей Na/NH3(ж), LiAlH4, Et2AlH позволяет с хорошим выходом получить 1,2-дигидрохинолин.
В кислом растворе и в отсутствии воздуха 1,2-дигидрохинолин диспропорционирует с образованием хинолина и 1,2,3,4-тетрагидрохинолина.
Последний может быть получен с помощью Na/EtOH (восстановление по Вышнеградскому), Sn/HCl или каталитическим гидрированием.
Гидрирование хинолина над PtO2 в CF3CO2H приводит к 5,6,7,8-тетра-гидрохинолину.
Гидрирование хинолина над никелевым катализатором в условиях повышенных давления и температуры (70 атм, 210°С) заканчивается образованием стереоизомерных пергидрохинолинов.
Дата добавления: 2015-12-15 | Просмотры: 1792 | Нарушение авторских прав |