Углеводные дистрофии, связанные с нарушением обмена гликопротеидов
При нарушении обмена гликопротеидов в клетках, как и в межкле-
точном веществе, происходит накопление муцинов и мукоидов, называемых
также слизистыми или слизеподобными веществами. В связи
с этим при нарушении обмена гликопротеидов говорят о слизистой
дистрофии.

| Микроскопическая картина: происходит не только усиленное слизеобразо-
вание, но и изменение физико-химических свойств слизи. Многие секретирую-
щие клетки погибают и десквамируются, выводные протоки желез обтури-
руются слизью, что ведет к развитию кист. Нередко в этих случаях
присоединяется воспаление. Слизь может закрывать просветы бронхов, след-
ствием чего является возникновение
ателектазов и очагов пневмонии.
Слизистая дистрофия может наблю-
даться в эпителиальных опухолях
(например, слизистый рак желудка).
Иногда в железистых структурах
накапливается не истинная слизь,
а слизеподобные вещества (псевдо-
муцины). Эти вещества могут уплот-
няться и принимать характер кол-
лоида. Тогда говорят о коллоид-
ной дистрофии (рис. 9), которая
наблюдается, например, при кол-
лоидном зобе, коллоидном раке.
Рис. 9. Коллоидная дистрофия щитовидной
железы при зобе. В альвеолах железы
скопления коллоида.
Причины слизистой дистрофии разнообразны, но чаще всего это воспале-
ние слизистых оболочек в результате действия различных патогенных раздра-
жителей (см. «Катаральное воспаление»).
Исход в значительной мере определяется степенью и длительностью повы-
шенного слизеобразования. В одних случаях регенерация эпителия приводит
к полному восстановлению слизистой оболочки, в других она атрофируется,
подвергается склерозу.
Функциональное значение слизистой дистрофии достаточно велико, если
учесть, что она может привести к атрофии и склерозу слизистых оболочек.
Слизистая дистрофия лежит в основе наследственного системного заболевания, называемого
му к о в и сци д о з о м, для которого характерно изменение качества слизи, выделяемой эпите-
лием слизистых желез: слизь становится густой и вязкой, она плохо выводится, что обусловли-
вает развитие ретенционных кист и склероза (кистозный фиброз). Поражаются экзо-
кринный аппарат поджелудочной железы, железы бронхиального дерева, пищеварительного
и мочевого тракта, желчных путей, потовые и слезные железы (подробнее см. «Пренатальная па-
тология», с. 513).
МЕЗЕНХИМАЛЬНЫЕ ДИСТРОФИИ
Мезенхимальные дистрофии развиваются в результате наруше-
ний обмена в соединительной ткани и выявляются в строме органов и стенках
сосудов.
Структурно-функциональной единицей соединительной ткани, в которой наблюдаются мно-
гие патологические процессы, в том числе и дистрофические, считается г ист и он. Он образо-
ван отрезком микроциркуляторного русла с окружающими его элементами соединительной тка-
ни (основное вещество, волокнистые структуры, клетки) и нервными волокнами.
Гистион представляет собой транспортную систему трофики, в которой встречаются пути об-
мена между кровью и клеткой,- а также между клеткой и лимфой. От правильных ритмов ра-
боты этой системы зависит не только отправление специализированной функции паренхима-
тозными элементами органов и тканей, но и сохранность среды обмена, т. е. гистиона. При
нарушениях обмена в соединительной ткани, преимущественно в ее межклеточном веществе, на-
капливаются продукты метаболизма, которые могут приноситься с кровью и лимфой (и н-
фильтрация), быть результатом извращенного синтеза или появляться в результате
декомпозиции (дезорганизации) основного вещества и волокон соединительной ткани.
В зависимости от вида нарушенного обмена мезенхимальные дистрофии
делят на белковые (диспротеинозы), жировые (липидозы) и угле-
водные.
Мезенхимальные белковые дистрофии (диспротеинозы)
Среди белков соединительной ткани основное значение имеет фибрил-
лярный белок —коллаген, из макромолекул которого (тропоколлаген)
строятся коллагеновые и ретикулярные волокна. Коллаген является неотъе-
млемой частью базальных мембран (эндотелия, эпителия) и эластических во-
локон, в состав которых, помимо коллагена и эластина, входят гликозамино-
гликаны. Коллаген синтезируется клетками соединительной ткани, среди
которых главную роль играют фибробласты. Кроме коллагена, эти клет-
ки синтезируют также гликозаминогликаны основного вещества соединитель-
ной ткани.
Волокна соединительной ткани имеют характерную ультраструктуру. Они хорошо выя-
вляются с помощью ряда гистологических методов: коллагеновые — окраской пикрофуксиновой
смесью (по Ван-Гизону), эластические — окраской фукселином или орсеином, ретикулярные —
импрегнацией солями серебра (ретикулярные волокна являются аргирофильными).
Волокна и составляющие их фибриллы соединительной ткани цементи-
руются ее основным веществом, которое, помимо гликозаминогликанов, со-
держит белки и полисахариды плазмы крови.
Белки плазмы хорошо выявляются не только гистологическими (например, окраска азокар-
мином), но и иммуногистохимическими методами при использовании антисывороток к альбу-
мину, фракциям глобулинов (иммуноглобулинов), фибриногену и др.
В соединительной ткани, помимо клеток, синтезирующих ее белки и глико-
заминогликаны (фибробласт, ретикулярная клетка, лаброцит, или тучная
клетка), находятся клетки (преимущественно гематогенного происхождения),
осуществляющие фагоцитоз (лейкоциты, гистиоциты, макрофаги) и иммунные
(плазмобласты и плазмоциты, лимфоциты, макрофаги) реакции.
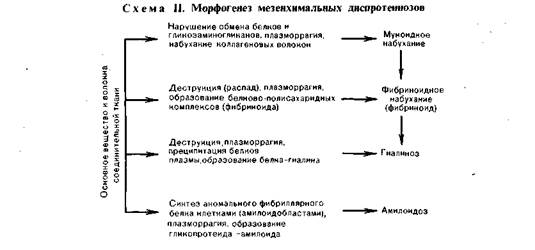
К мезенхимальным диспротеинозам относят мукоидное набухание,
фибриноидное набухание (фибриноид), гиалиноз, амилои-
доз.
Нередко мукоидное набухание, фибриноидное набухание и гиалиноз
являются последовательными стадиями дезорганизации соедини-
тельной ткани; в основе этого процесса лежат накопление продуктов
плазмы крови в основном веществе в результате повышения тканевососуди-
стой проницаемости (плазморрагии), деструкция элементов соединительной
ткани и образование белковых (белково-полисахаридных) комплексов. Ами-
лоидоз отличается от этих процессов тем, что в состав образующихся белко-
во-полисахаридных комплексов входит не встречающийся обычно фибрил-
лярный белок, синтезируемый клетками — амилоидобластами (схема II).
Мукоидное набухание \
Мукоидное набухание — поверхностная и обратимая дезорганиза-
ция соединительной ткани. При этом в основном веществе происходят на-
копление и перераспределение гликозаминогликанов за счет увеличения содер-
жания прежде всего гиалуроновой кислоты. Гликозаминогликаны обладают
гидрофильными свойствами и накопление их обусловливает повышение
тканевойисосудистойпроницаемости. В результате этого к гли-
козаминогликанам примешиваются белки плазмы (главным образом гло-
булины) и гликопротеиды. Развиваются гидратация и набухание основ-
ного межуточного вещества.
Микроскопическая картина: при окраске гематоксилин-эозином основное
вещество становится базофильным, а при окраске толуидиновым синим — си-
реневым или красным (рис. 10, см. на цветн. вкл.). Возникает феномен ме-
тахромазии, в основе которого лежит изменение состояния основного ме-
жуточного вещества с накоплением хромотропных веществ. Коллагеновые
волокна обычно сохраняют пучковое строение, но набухают и подвергаются
фибриллярному разволокнению. Они становятся малоустойчивыми к дей-
ствию коллагеназы и при окраске пикрофуксином выглядят желто-оранжевы-
ми, а не кирпично-красными. Изменения основного вещества и коллагеновых
волокон при мукоидном набухании могут сопровождаться клеточными реак-
циями — появлением лимфоцитарных, плазмоклеточных и гистиоцитарных
инфильтратов.
Мукоидное набухание встречается в различных органах и тканях, но чаще
в стенках артерий, клапанах сердца, эндокарде и эпикарде, т. е. там, где хро-
мотропные вещества встречаются и в норме; при этом количество хромо-
тропных веществ резко возрастает.
Внешний вид ткани или органа при мукоидном набухании сохранен, харак-
терные изменения устанавливаются под микроскопом с помощью гистохими-
ческих реакций.
Причины мукоидного набухания разнообразны; большое значение в его
развитии имеет гипоксия. Мукоидное набухание встречается при инфек-
ционных и аллергических заболеваниях, ревматических болезнях, атеросклеро-
зе, эндокринопатиях и др.
Исход может быть двояким: полное восстановление ткани или переход
в фибриноидное набухание.
Значение мукоидного набухания состоит в нарушении функции органа,
в котором оно развивается (например, нарушения функции сердца в связи
с развитием ревматического эндокардита — вальвулита).
Фибриноидное набухание (фибриноид)
Фибриноидное набухание — глубокая и необратимая дезорганиза-
ция соединительной ткани, в основе которой лежит деструкция ее основ-
ного вещества и волокон, сопровождающаяся резким повышением сосудистой
проницаемости и образованием фибриноида.
Фибриноид представляет собой сложное вещество, в состав которого
входят белки и полисахариды распадающихся коллагеновых волокон, основ-
ного вещества и плазмы крови, а также клеточные нуклеопротеиды. Гистохи-
мически при различных заболеваниях фибриноид различен, но обязательным
компонентом его является фибрин (рис. 11) (отсюда и термины «фибри-
ноидное набухание», «фибриноид»).
Микроскопическая картина: при фибриноидном набухании пучки коллаге-
новых волокон, пропитанные белками плазмы, становятся гомогенными,
образуя с фибрином нерастворимые прочные соединения, они жадно воспри-
нимают кислые красители — эозинофильные, пикрофуксином окрашиваются
в желтый цвет, резко ШИК-положительны и пиронинофильны при реакции
Браше, а также аргирофильны при импрегнации солями серебра. Метахрома-
зия соединительной ткани при этом не выражена или выражена слабо, что
объясняется деполимеризацией гликозаминогликанов основного вещества.
В исходе фибриноидного набухания иногда развивается ф и б р и -
ноидный некроз, характеризующийся полной деструкцией соединитель-
ной ткани. Вокруг очагов некроза обычно выражена реакция макрофагов.
Внешний вид различных органов и тканей, где встречается фибриноидное
набухание, мало изменяется, характерные изменения обнаруживаются обычно
лишь при микроскопическом исследовании.
Причины фибриноидных изменений разнообразны. Среди них наибольшее
значение имеют: инфекционно-аллергические (например, фибриноид сосудов
при туберкулезе с гиперергическими реакциями), аллергические и аутоиммун-
зз
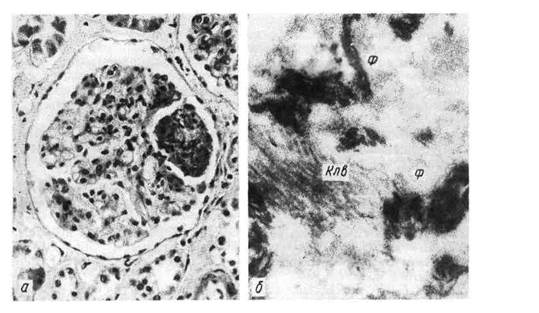
Рис. 11. Фибриноидное набухание.
а — фибриноидное набухание и фибриноидный некроз капилляров почечных клубочков (системная красная
волчанка); б — электронограмма: в фибриноиде среди набухших, потерявших поперечную исчерченность
коллагеновых волокон (КлВ), массы фибрина (Ф). х 35000 (по Гизекингу).
ные (фибриноидные изменения соединительной ткани при ревматических болез-
нях; капилляров почечных клубочков при гломерулонефрите), ангионевроти-
ческие (фибриноид артериол при гипертонической болезни и артериальных ги-
пергензиях). В таких случаях фибриноидное набухание имеет распростра-
ненный (системный) характер. В качестве проявления воспаления, особенно
хронического, фибриноидное набухание возникает местно (фибриноид
в червеобразном отростке при аппендиците, в дне хронической язвы желудка,
трофических язв кожи и т. д.).
В исходе фибриноидных изменений развивается некроз, замещение очага
деструкции соединительной тканью (склероз) или гиалиноз.
Значение фибриноидного набухания огромно. Оно ведет к нарушению,
а нередко и прекращению функции органа (например, острая почечная недо-
статочность при злокачественной гипертонии, характеризующейся фибри-
ноидным некрозом артериол клубочков).
Гиалиноз
При гиалинозе (от греч. hyalos — прозрачный, стекловидный), или
гиалиновой дистрофии, в соединительной ткани образуются одно-
родные полупрозрачные плотные массы (гиалин)2 напоминающие гиалиновый
хрящ. Появление в цитоплазме гиалиновых капель (гиалиново-капельная ди-
строфия) к гиалинозу отношения не имеет.
Гиалин — это фибриллярный белок, в образовании которого большая роль
принадлежит белкам плазмы, в частности фибрину. При иммуногистохимиче-
ском исследовании в гиалине обнаруживают не только фибрин, но и компо-
ненты иммунных комплексов (иммуноглобулины, фракции комплемента),
а также липиды. Гиалиновые массы устойчивы по отношению к кислотам,
щелочам, ферментам, хорошо окрашиваются кислыми красителями (эозин,
кислый фуксин), пикрофуксином окрашиваются в желтый или красный цвет,
ШИК-положительны.
Механизм гиалиноза сложен. Ведущими в его развитии являются деструк-
ция волокнистых структур и повышение тканево-сосудистой проницаемости
(плазморрагия) в связи с ангионевротическими (дисциркуляторными), метабо-
лическими и иммунопатолотическими процессами. С плазморрагией связаны
пропитывание ткани белками плазмы и адсорбция их на измененных волок-
нистых структурах с последующей преципитацией и образованием белка —
гиалина. Гиалиноз может развиваться в исходе разных процессов: плазмати-
ческого пропитывания, фибриноидного набухания (фибриноида), воспаления,
некроза, склероза.
Классификация гиалиноза. Различают гиалиноз сосудов и гиалиноз соб-
ственно соединительной ткани. Каждый из них может быть распростра-
ненным(системным) и местным.
Гиалиноз сосудов. Гиалинозу подвергаются преимущественно мел-
кие артерии и артериолы. Ему предшествует повреждение эндотелия, аргиро-
фильных мембран и гладкомышечных клеток стенки и пропитывание ее плаз-
мой крови.
Микроскопическая картина: гиалин выпадает в субэндотелиальном про-
странстве, гиалиновые массы оттесняют кнаружи и разрушают эластическую
пластинку, ведут к истончению средней оболочки, в результате чего арте-
риолы превращаются в утолщенные плотные стекловидные трубочки с резко
суженным или полностью закрытым просветом (рис. 12).
Гиалиноз мелких артерий и артериол носит системный характер, но наибо-
лее выражен в почках, головном мозге, сетчатке глаза, полжелудочной желе-
зе, коже. Он особенно характерен для гипертонической болезни и гипертони-
ческих состояний (гипертонический артериологиалиноз), диабетической ми-
кроангиопатии (диабетический артериологиалиноз) и заболеваний с наруше-
ниями иммунитета. Как физиологическое явление местный гиалиноз артерий
наблюдается в селезенке взрослых и пожилых людей, отражая функцио-
нально-морфологические особенности селезенки как органа депонирования
крови.
Сосудистый гиалин — вещество гематогенной природы. В его образовании
играют роль не только гемодинамические и метаболические, но и иммунные
механизмы. Руководствуясь особенностями патогенеза гиалиноза сосудов, вы-
деляют 3 вида сосудистого гиалина: 1) простой, возникающий
вследствие инсудации неизмененных или малоизмененных компонентов плазмы
крови; встречается чаще при гипертонической болезни доброкачественного те-
чения, атеросклерозе и у здоровых людей; 2) л и п о г и а л и н, содержащий
липиды и В-липопротеиды; обнаруживается чаще всего при сахарном диабете;
3) сложный гиалин, строящийся из иммунных комплексов, фибрина
и разрушающихся структур сосудистой стенки (см. рис. 12), характерен для
болезней с иммунопатологическими нарушениями, например для ревматиче-
ских заболеваний.
Гиалиноз собственно соединительной ткани. Развивается
обычно в исходе фибриноидного набухания, ведущего к деструкции коллагена
и пропитыванию ткани белками плазмы и полисахаридами.
Микроскопическая картина: соединительнотканные пучки разбухают, те-
ряют фибриллярность и сливаются в однородную плотную хрящеподобную
массу; клеточные элементы сдавливаются и подвергаются атрофии.
Подобный механизм развития системного гиалиноза соединительной ткани
особенно часто встречается при заболеваниях с иммунными нарушениями (рев-
матические болезни). Гиалиноз может завершать фибриноидные изменения
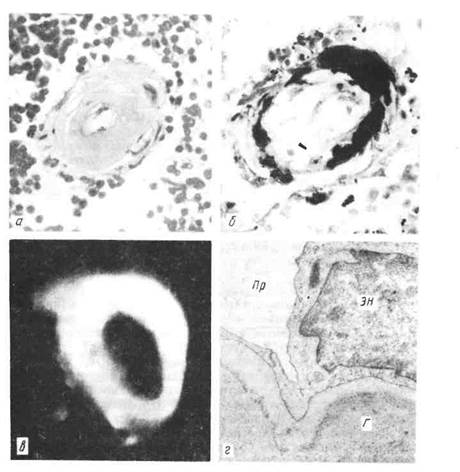
Рис. 12. Гиалиноз сосудов селезенки.
а — стенка центральной артерии фолликула селезенки представлена гомогенными гиалиноподобными
массами; 6 — фибрин среди гиалиновых масс при окраске по методу Вейгерта; в — фиксация в гиалине
иммуноглобулина класса G (антитело) иммунных комплексов; люминесцентный микроскоп; г — электро-
нограмма: массы гиалина (Г) в стенке аргериолы; Эn — эндотелий; Пр — просвет артериолы. х 15000.
в дне хронической язвы желудка, в червеобразном отростке при аппенди-
ците; подобен механизму местного гиалиноза в очаге хронического вос-
паления.
В качестве своеобразного исхода склероза гиалиноз имеет в основном так-
же местный характер: он развивается в рубцах, фиброзных спайках серозных
полостей, сосудистой стенке при атеросклерозе, инволюционном склерозе ар-
терий, при организации тромба,в капсулах(рис. 13), строме опухоли и т. д.
В основе гиалиноза в этих случаях лежат нарушения обмена в соединительной
ткани. Подобный механизм имеет гиалиноз некротизированных тканей и фи-
бринозных наложений.
Внешний вид органов при гиалинозе обычно сохранен. Однако в тех слу-
чаях, когда процесс выражен резко, ткань становится бледной, плотной и по-
лупрозрачной. Гиалиноз может вести к деформации и сморщиванию органа
(например, развитие артериолосклеротического нефроцирроза, клапанного по-
рока сердца).
Рис. 13. Гиалиноз капсулы печени —
глазурная печень (вид сверху).
Исход в большинстве слу-
чаев гиалиноза неблагоприят-
ный, но возможно и рассасы-
вание гиалиновых масс. Так,
гиалин в рубцах, так называе-
мых келоидах, может подвер-
гаться разрыхлению и рассасы-
ванию. Обратим гиалиноз мо-
лочной железы,причем расса-
сывание гиалиновых масс про-
исходит в условиях гиперфунк-
ции желез. Иногда гиалинизи-
рованная ткань ослизняется..
Функциональное значение гиалиноза различно в зависимости от его локали-
зации, степени и распространенности. Например, в рубцах он может не причи-
нять особых расстройств. Распространенный гиалиноз, напротив, ведет к зна-
чительным функциональным нарушениям и может иметь тяжелые послед-
ствия, как это наблюдается, например, при ревматизме, склеродермии,
гипертонической болезни, диабете и других болезнях.
Амилоидоз
Амилоидоз (от лат. amylum — крахмал), или амилоидная дистро-
фия, — мезенхимальный диспротеиноз, сопровождающийся глубоким наруше-
нием белкового обмена, появлением аномального фибриллярного белка
и образованием в межуточной ткани сложного вещества — амилоид а.
В 1844 г. венский патолог Рокитанский описал своеобразные изменения паренхиматозных
органов, которые, помимо резкого уплотнения, приобретали восковой, сальный вид. Заболева-
ние, при котором возникали подобные изменения органов, он назвал «сальной болезнью». Спу-

Рис. 14. Ультраструктура амилоида.
а — фибриллы амилоида (Aм), х 35 000; б — палочковидные образования, состоящие из пентагональных
структур (ПСт).х 300000 (по Гленнер и др.).
стя несколько лет Р. Вирхов показал, что изменения эти связаны с появлением в органах особо-
го вещества, которое под действием йода и серной кислоты окрашивается в синий цвет. Это
вещество Вирхов считал животным крахмалом и назвал амилоидом, а «сальную болезнь» —
амилоидозом. Белковая природа амилоида была установлена М. М. Рудневым вместе с Кюне
в 1865 г.
Амилоид представляет собой гликопротеид, основным компонентом кото-
рого являются фибриллярные белки (F-компонент). Они образуют фибриллы,
имеющие характерную ультрамикроскопическую структуру. Одни фибрил-
лярные белки амилоида связаны с легкими цепями иммуноглобулинов (белки
AL), другие не связаны с иммуноглобулинами (белки АА), но имеют аналог
в сыворотке крови (белок SAA).
Фибриллы амилоида (рис. 14) имеют диаметр 7,5 нм и длину до 800 нм, лишены поперечной
исчерченности. Каждая фибрилла состоит из двух субфибрилл (филаментов) по 2,5 нм в диаме-
тре. Фибриллярные белки амилоида синтезируются мезенхимальными клетками — амилоидобла-
стами. В отличие от коллагена они богаты триптофаном, не содержат оксипролина и связаны
с небольшим количеством нейтральных Сахаров и сиаловой кислоты.
В электронном микроскопе он представляет собой специфические палочковидные структу-
ры — «периодические палочки» (см. рис. 14) диаметром 10 нм и длиной до 400 нм, которые со-
стоят из отдельных пентагональных образований. Каждое такое образование в свою очередь
состоит из пяти триангулярных компонентов. В сывороточных гликопротеидах Р-компонента по
сравнению с фибриллами амилоида значительно больше нейтральных Сахаров и сиаловой
кислоты.
Фибриллярные белки амилоида входят в сложные соединения с белками
и полисахаридами (глюкопротеидами) плазмы крови, которые являются
вторым обязательным компонентом амилоида. Это так называемый плаз-
менный компонент (Р-компонент).
Фибриллярный и плазменный компоненты амилоида обладают антигенны-
ми свойствами.
Фибриллы амилоида и плазменный компонент вступают в соединения
с хондроитинсульфатами ткани и к образующемуся комплексу присоединяют-
ся так называемые гематогенные добавки, среди которых основное значение
имеют фибрин и иммунные комплексы.
Связи белков и полисахаридов в амилоидном веществе чрезвычайно проч-
ные, чем объясняется отсутствие эффекта при действии на амилоид раз-
личных ферментов организма.
Амилоид хорошо окрашивается конго красным. Наиболее специфичным для амилоида
является его метахроматическое красное окрашивание с метиловым (или генциановым) фиоле-
товым, а также люминесценция с тиофлавинами S или Т. Для макроскопической диагностики
амилоидоза пользуются воздействием на ткань люголевским раствором, а затем 10% рас-
твором серной кислоты. Амилоид становится сине-фиолетовым или грязно-зеленым.
Красочные реакции амилоида, определяющиеся особенностями его хими-
ческого состава, могут быть различными в зависимости от формы, вида и ти-
па амилоидоза. В ряде случаев (особенно при первичном амилоидозе и пара-
амилоидозе, см. с. 42) они отсутствуют. Тогда говорят об ахроматическом
амилоиде, или ахроамилоиде.
Содержанием фибриллярных белков обусловлено наличие у амилоида таких поляризацион-
но-оптических свойств, как дихроизм и анизотропия (спектр двойного лучепреломления лежит
в пределах 540 — 560 нм). Эти свойства позволяют отличать амилоид от других фибриллярных
белков — коллагена и эластина.
Морфогенез амилоидоза. Первая, предамилоидная, стадия ха-
рактеризуется трансформацией синтезирующих белок мезенхимальных эле-
ментов (клетки ретикулоэндотелиальной системы старых авторов) в клетки —
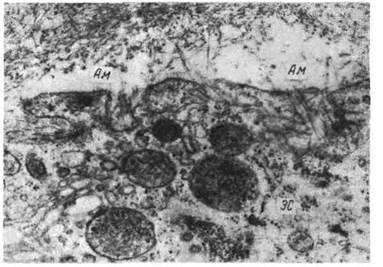
Рис. 15. Амилоидобласт. Фибриллы амилоида (Ам) в инвагинатах плазмолеммы звездчатото
ретикулоэндотелиоцита с гиперплазией гранулярной эндоплазматической сети (ЭС), свидетель-
ствующей о его высокой синтетической активности, х 30000.
амилоидобласты. Роль амилоидобластов играют в основном плазматические,
ретикулярные клетки и фибробласты; в печени ими становятся звездчатые ре-
тикулоэндотелиоциты (рис. 15), в почках — мезангиоциты. Вторая ста-
ди я — синтез амилоидобластами основного компонента амилоида — фибрил-
лярного белка (белка фибрилл). Третья стадия — агрегация фибрилл
амилоида с образованием «каркаса» амилоидного вещества сопровождается
клеточной реакцией резорбции амилоидных фибрилл (амилоидоклазия). Одна-
ко эта реакция быстро подавляется, так как к белку — антигену амилоида воз-
никает иммунологическая толерантность (терпимость). С иммунологической
толерантностью к белку амилоида можно связать безудержное накопление
амилоидного вещества в подавляющем большинстве случаев амилоидоза.
Четвертая стадия — соединение фибрилл амилоида с гликопротеидами
плазмы и хондроитинсульфатами ткани, т. е. образование сложного глико-
протеида — амилоида.
Образование амилоидного вещества происходит вне клеток и тесно связа-
но с волокнами соединительной ткани — ретикулярными или коллагеновыми.
В зависимости от отношения амилоидного вещества к фибриллярным
структурам соединительной ткани различают периретикулярный и п е -
риколлагеновый виды амилоидоза (амилоида). Для периретику-
лярного амилоидоза, при котором амилоид выпадает по ходу мем-
бран сосудов и желез, а также ретикулярной стромы паренхиматозных
органов, характерно преимущественное поражение селезенки, печени, почек,
надпочечников, кишечника, интимы сосудов мелкого и среднего калибра (па-
ренхиматозный амилоидоз). Для периколлаген ового амилоидоза,
при котором амилоид выпадает по ходу коллагеновых волокон, свойственно
преимущественное поражение адвентиции сосудов среднего и крупного ка-
либра, миокарда, поперечнополосатой и гладкой мускулатуры, нервов, кожи
(мезенхимальный амилоидоз). Таким образом,амилоидные отложения имеют
довольно типичную локализацию: в стенках кровеносных и лимфати-
ческих капилляров и сосудов в интиме или адвентиции; в строме органов по
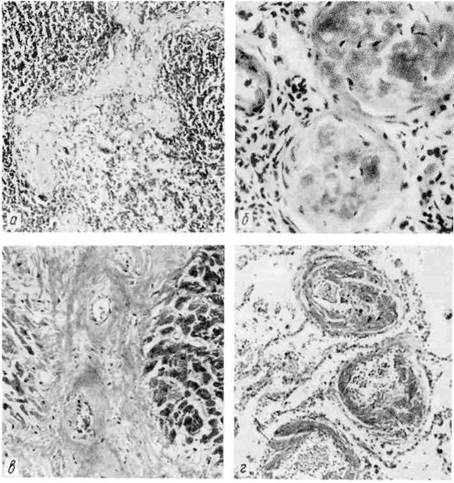
Рис. 16. Амилоидоз.
и — амилоид в фолликулах селезенки (саговая селезенка); б — амилоид в сосудистых клубочках почек;
в — амилоид между мышечными волокнами сердца; г — амилоид в стенках сосудов легких.
ходу ретикулярных или коллагеновых волокон; в собственной оболочке желе-
зистых структур.
Амилоид может выпадать как диффузно (общий, распростра-
ненный а м и л о и д о з), так и местно, на ограниченных участках
(местный а м и л о и д о з).
Внешний вид органов при амилоидозе зависит от степени процесса. Если
отложения амилоида небольшие, внешний вид органа изменяется мало и ами-
лоидоз обнаруживается лишь при микроскопическом исследовании. При вы-
раженном амилоидозе орган увеличивается в объеме, становится очень
плотным и ломким, а на разрезе имеет своеобразный восковидный или
сальный вид.
Вселезенке амилоид откладывается в лимфатических фолликулах (рис.
16) или же равномерно по всей пульпе. В первом случае амилоидно изме-
ненные фолликулы увеличенной и плотной селезенки на разрезе имеют вид
полупрозрачных зерен, напоминающих зерна саго (саговая селезенка).
Во втором случае селезенка резко увеличена, плотня, коричнево-красная, глад-
кая, имеет сальный блеск на разрезе (сальная селезенка). Саговая
и сальная селезенка представляют последовательные стадии процесса.
В почках амилоид откладывается в стенке сосудов, в капиллярных пет-
лях и мензангии клубочков, в базальных мембранах канальцев и в строме.
Почки становятся плотными, большими и «сальными». По мере нарастания
процесса клубочки и пирамиды полностью замещаются амилоидом (см. рис.
16), разрастается соединительная ткань и развивается амилоидное сморщива-
ние почек.
В печени отложение амилоида наблюдается между звездчатыми ретику-
лоэндотелиоцитами синусоидов, по ходу ретикулярной стромы долек, в стенках
сосудов, протоков и в соединительной ткани портальных трактов. По мере на-
копления амилоида печеночные клетки атрофируются и погибают. При этом
печень увеличена, плотна, выглядит «сальной».
В кишечнике амилоид выпадает по ходу ретикулярной стромы слизи-
стой оболочки, а также в стенках сосудов как слизистой оболочки, так и подсли-
зистого слоя. При резко выраженном амилоидозе железистый аппарат кишеч-
ника атрофируется.
Амилоидоз надпочечников, как правило, двусторонний, отложение
амилоида встречается в корковом веществе по ходу сосудов и капилляров.
Выраженный амилоидоз надпочечников ведет к их недостаточности, развитию
признаков аддисоновой болезни.
В сердце амилоид обнаруживается под эндокардом, в строме и сосудах
миокарда (см. рис. 16), а также в эпикарде по ходу вен. Отложение амилоида
в сердце ведет к резкому его увеличению (амилоидная кардиомегалия). Оно
становится очень плотным, миокард приобретает сальный вид.
Вскелетных мышцах, как и в миокарде, амилоид выпадает по ходу
межмышечной соединительной ткани, в стенках сосудов и в нервах. Перива-
скулярно и периневрально нередко образуются массивные отложения ами-
лоидного вещества. Мышцы становятся плотными, полупрозрачными.
В легких отложения амилоида появляются сначала в стенках разветвле-
ний легочных артерии и вены (см. рис. 16), а также в перибронхиальной со-
единительной ткани. Позже амилоид появляется в межальвеолярных перего-
родках.
В головном мозге при старческом амилоидозе амилоид находят
в сенильных бляшках коры, сосудах и оболочках.
Амилоидоз кожи характеризуется диффузным отложением амилоида
в сосочках кожи и в ретикулярном слое ее, в стенках сосудов и по периферии
сальных и потовых желез, что сопровождается деструкцией эластических во-
локон и резкой атрофией эпидермиса.
Амилоидоз поджелудочной железы имеет некоторое своеобра-
зие. Помимо артерий железы, встречается и амилоидоз панкреатических
островков (островки Лангерганса) с избирательным поражением В-клеток, что
наблюдается при сахарном диабете в глубокой старости.
Амилоидоз щитовидной железы также своеобразен. Отложения
амилоида в строме и сосудах железы могут быть проявлением не толь-
ко генерализованного амилоидоза, но и медуллярного рака железы (ме-
дуллярный рак щитовидной железы с амилоидозом стромы).
Амилоидоз стромы часто встречается в опухолях эндокринных органов
или паракринной APUD-системы (так называемые апудомы, см. с. 222): ме-
дуллярном раке щитовидной железы, инсуломе, карциноиде, феохромоцито-
ме, опухолях каротидных телец, хромофобной аденоме гипофиза, гиперне-
фроидном раке, некоторых кожных и одонтогенных опухолях. В образовании
«APUD-амилоида» доказано участие эпителиальных опухолевых клеток.
Классификация. Руководствуясь п ри ч и н н ы ми факторами и воз-
можным патогенетическим механизмом, различают пять форм
амилоидоза: 1) идиопатический (первичый),причина и механизм
развития неизвестны (не исключено, что в ряде случаев он представляет
собой спорадические варианты наследственного амилоидоза); 2) наслед-
ственный (генетический, семейный), возникающий вследствие генетическо-
го дефекта синтеза фибриллярных белков организма (наследственной фермен-
топатии); 3) приобретенный (вторичный), который может возникать
при нарушении иммунологического гомеостаза (амилоидоз как осложнение
хронических инфекций, ревматических болезней и злокачественных опухолей)
или в результате неопластической трансформации клеток белоксинтезирую-
щей системы (амилоидоз при парапротеинемических хронических лимфатиче-
ских лейкозах; амилоидоз опухолей APUD-системы — APUD-амилоид); 4)
старческий амилоидоз, в основе развития которого лежат инволютивные
нарушения обмена белков; 5) локальный опухолевидный амилои-
доз, природа которого неясна. Идиопатический, наследственный, старческий
и локальный опухолевидный амилоидоз рассматриваются в качестве нозоло-
гических форм. Приобретенный амилоидоз, встречающийся при тех или иных
заболеваниях, является осложнением этих заболеваний, «второй болезнью».
Независимо от формы амилоидоза для него характерно вытеснение спе-
циализированных элементов органов.и тканей амилоидным веществом с по-
нижением, а в финале и утратой их функции. В зависимости от преобла-
дания поражения амилоидозом тех или иных органов,
функциональная недостаточность которых становится ведущей, различают
нефропатический, кардиопатический, нейропатилеский,
гепатопатический, эпинефропатический, смешанный и
генерализованный типы амилоидоза.
Идиопатический(и первичный) амилоидоз может проявляться
в виде генерализованного, нефропатического, гепатопатического, нейропатиче-
ского и кардиопатического типов. Генерализованный первичный амилоидоз
характеризуют (Любарш): отсутствие предшествующего или сопутствующего
«причинного» заболевания; более частое поражение мезодермальных тканей
по сравнению с паренхиматозными (чаще поражаются сердечно-сосудистая
система, пищеварительный тракт, поперечнополосатые и гладкие мышцы,
нервы и кожа — периколлагеновый амилоидоз); непостоянство красочных ре-
акций амилоидного вещества (часты отрицательные результаты пробы с кон-
го красным); склонность к образованию узловатых отложений. При нефропа-
тическом и гепатопатическом типах амилоид периретикулярный (паренхима-
тозный амилоидоз), при нейропатическом и кардиопатическом — периколлаге-
новый (мезенхимальный амилоидоз).
Наследственный (генетический, семейный) амилоидоз
выделен сравнительно недавно; значение генетических факторов в развитии
амилоидоза подтверждается своеобразием его географической патологии и осо-
бой предрасположенностью определенных этнических групп населения. Разли-
чают невропатический, нейропатический и кардиопатический типы наслед-
ственного амилоидоза.
Наиболее часто встречающийся нефропатический тип наследственного амилоидоза характе-
рен для периодической болезни (семейной средиземноморской лихорадки), которая чаще наблю-
дается у представителей древних народов (евреев, армян, арабов); для семейного амилоидоза,
протекающего с лихорадкой, крапивницей и глухотой, описанного в английских семьях (форма
Маккла и Уэллса), а также семейного амилоидоза с лихорадкой и аллергией; который встре-
чается у русских (форма, описанная О. М. Виноградовой и соавт.). Наследственный нейропа-
тический амилоидоз имеет несколько вариантов (типов). Для наследственной нейропа-
тии I типа (португальский амилоидоз) характерно поражение периферических нервов ног, а для
нейропатии II типа, встречающейся в американских семьях, — поражение периферических нервов
рук. При нейропатии III типа, которая описана также у американцев, встречается сочетание ее
с нефропатией, а при нейропатии IV типа, описанной в финских семьях, отмечается сочетание не
только с нефропатией, но и сетчатой дистрофией роговицы. Наследственный кардиопатиче-
ский амилоидоз, встречающийся у датчан, мало чем отличается от кардиопатического ти-
па идиопатического амилоидоза.
При нефропатическом наследственном амилоидозе амилоидное вещество
откладывается по ходу ретикулярных волокон (периретикулярный, паренхима-
тозный амилоидоз), а при кардиопатическом и нейропатическом — по ходу
коллагеновых волокон (периколлагеновый, мезенхимальный амилоидоз).
Приобретенный (вторичный) амилоидоз встречается наиболее
часто и в отличие от других форм развивается на фоне какого-либо заболева-
ния. Это хронические инфекции, особенно туберкулез, болезни, характеризую-
щиеся гнойно-деструктивными процессами (хронические неспецифические вос-
палительные заболевания легких, остеомиелит, нагноение ран), злокачествен-
ные новообразования (плазмоцитома, лимфогранулематоз, рак), ревмати-
ческие болезни (особенно ревматоидный артрит).
Так как при вторичном амилоидозе поражаются преимущественно парен-
химатозные органы (паренхиматозный амилоидоз), то обычно развивается не-
фропатический, эпинефропатический, гепатопатический или смешанный типы
амилоидоза. Наиболее частый среди, них — нефропатический тип (амилоидоз
почек). Исключение составляет лишь вторичный амилоидоз при парапротеи-
немических лейкозах, или параамилоидоз, которому свойственна мезенхи-
мальная локализация амилоидных отложений.
При старческом амилоидозе типичны поражения сердца, артерий,
головного мозга и В -клеток островков поджелудочной железы. Эти изменения,
как и атеросклероз, обусловливают старческую физическую и психическую де-
градацию. У старых людей имеется несомненная связь между амилоидозом,
атеросклерозом и диабетом, которая объединяет возрастные нарушения
обмена.
Локальный опухолевидный амилоидоз близок первичному.
От других форм амилоидоза его отличает не только местный характер про-
цесса, но и опухолевидный рост амилоидного вещества («амилоидная опу-
холь»).
Установлена связь между определенными формами амилоидоза и видами фибриллярного
-белка амилоида: при первичном амилоидозе и амилоидозе, встречающемся при парапротеине-
мических хронических лимфатических лейкозах (особенно миеломной болезни), находят AL-ами-
лоидные белки (амилоид легких цепей иммуноглобулинов); в большинстве случаев вторичного
и некоторых видах генетического амилоидоза определяются АА-неиммуноглобулиновые белки
амилоида и их сывороточный аналог - SAA. Эти данные имеют не только теоретический инте-
рес, но и служат диагностике различных форм амилоидоза.
Патогенез. В настоящее время могут конкурировать, однако далеко не рав-
нозначно, следующие теории патогенеза амилоидоза: иммунологиче-
ская, клеточной локальной секреции и мутационная. Со-
держание некоторых из этих теорий, подчеркивающих ведущее значение того
или иного звена патогенеза, изменялось по мере появления новых фактов.
По иммунологической теории амилоид рассматривался до не-
давнего времени как продукт реакции антиген - антитело (Лёшке и Леттерер).
В настоящее время эта теория считается несостоятельной. Доказано, что им-
мунные комплексы в амилоиде являются лишь гематогенными «добавками».
Вместе с тем роль нарушений гуморального и клеточного иммунитета в раз-
витии амилоидоза можно считать доказанной; с нарушениями в иммунологи-
ческом гомеостазе в ряде случаев можно связать появление пула клеток ами-
лоидобластов, способных секретировать аномальный фибриллярный белок.
Однако такое объяснение приложимо лишь к экспериментальному амилоидо-
зу и вторичному амилоидозу у человека (исключая параамилоидоз). Механизм
же развития идиопатического, генетического (семейного) и старческого ами-
лоидоза иммунологическими нарушениями объяснить нельзя.
По теории клеточного локального синтеза (Тейлум) амилоид
рассматривается как продукт секреции клеток ретикулоэндотелиальной си-
стемы, а амилоидоз — как «мезенхимальная болезнь». Это хорошо аргументи-
рованная теория, так как синтез фибриллярного белка амилоида клетками ме-
зенхимального происхождения получил убедительные доказательства. Она
позволяет понять, где и как образуются белки и гликопротеиды амилоидного
вещества. Однако и эта теория не лишена недостатков. Она, например, не по-
зволяет раскрыть интимный механизм извращения белоксинтезирующей
функции клеток ретикулоэндотелиальной системы. Будучи приложима лишь
к вторичному амилоидозу человека и экспериментальному амилоидозу, она
не объясняет механизм развития генетического, первичного и старческого
амилоидоза.
Мутационная теория а ми л о ид о з а (В. В. Серов, И. А. Шамов)
может стать универсальной в объяснении патогенеза всех известных его форм,
если представить возможное разнообразие мутагенных факторов. При вто-
ричном амилоидозе, исключая амилоидоз при плазмоцитоме, мутации свя-
заны с длительной антигенной стимуляцией. При генетическом амилоидозе
речь идет о мутации гена, которая может произойти в различных локусах,
чем и определяются различия в составе амилоидного белка у разных людей
и животных. При старческом амилоидозе, вероятно, механизмы подобны, так
как этот амилоидоз рассматривается как фенокопия генетического. Клеточные
мутации при параамилоидозе и амилоидозе опухолей, а возможно, и при опу-
холевидном локальном амилоидозе обусловлены опухолевыми мутагенами.
Согласно мутационной теории, мутирующиеся клетки не распознаются иммунокомпетент-
ной системой и не элиминируются, так как амилоидные фибриллы являются чрезвычайно
слабыми иммуногенами. Возникает иммунологическая толерантность к фибриллярному белку
амилоида, что и определяет безудержное прогрессирование амилоидоза. Мутационная теория
амилоидоза позволяет понять его близость к опухолевому процессу.
Исход амилоидоза в общем неблагоприятный. Однако экспериментальные,
клинические и патологоанатомические наблюдения доказали возможность
амилоидоклазии — рассасывания амилоида гигантскими клетками.
Функциональное значение амилоидоза определяется степенью его развития.
Выраженный амилоидоз ведет к атрофии паренхимы и склерозу органа, вы-
ключению его функции.
Мезенхимальные жировые дистрофии (липидозы)
Мезенхимальные жировые дистрофии возникают при нару-
шениях обмена нейтральных жиров или холестерина и его эфиров.
Нарушения обмена нейтральных жиров
Нарушения обмена нейтральных жиров проявляются в уве-
личении их запасов в жировой ткани, которое может иметь общий или
местный- характер.
Нейтральные жиры — это лабильные жиры, обеспечивающие энергетические запасы организ-
ма. Они сосредоточены в жировых депо (подкожная клетчатка, брыжейка, сальник, эпикард,
костный мозг). Жировая ткань выполняет не только обменную, но и опорную, механическую
функцию. Поэтому она способна замещать атрофирующиеся ткани. Жировая ткань чрезвычайно
пластична. Наибольшее значение в регуляции жирового обмена имеют гипоталамус, симпатиче-
ская нервная система, гипофиз, половые железы, надпочечники и щитовидная железа.

Рис. 17. Разрастание жировой ткани в строме поджелудочной железы (сахарный диабет).
Рис. 18. Ожирение сердца. Под эпикардом толстой слой жира.
Общее ожирение, или тучность,- увеличение количества ней-
тральных жиров в жировых депо, имеющее общий характер. Оно выра-
жается в обильном отложении жиров в подкожной клетчатке, сальнике, бры-
жейке, средостении, эпикарде. Жировая ткань появляется также там, где она
обычно отсутствует или имеется лишь в небольшом количестве, например
в поджелудочной железе (рис. 17), строме миокарда.
Большое клиническое значение имеет ожирение сердца при тучно-
сти. Жировая ткань, разрастаясь под эпикардом, окутывает сердце, как футля-
ром (рис. 18). Она прорастает строму миокарда, особенно в субэпикар-
диальных отделах, что ведет к атрофии мышечных клеток. Ожирение обычно
резче выражено в правой половине сердца. Иногда вся толща миокарда пра-
вого желудочка замещается жировой тканью, в связи с чем может произойти
разрыв сердца.
Антиподом общего ожирения является истощение, в основе которого лежит атрофия.
Истощение наблюдается также в терминальной стадии кахексии (от греч. kakos - плохой,
hexis — состояние).
Классификация. Она основывается на различных принципах и учитывает
причину, внешние проявления болезни, степень превышения «идеальной мас-
сы» тела, морфологические изменения жировой ткани.
По этиологическому принципу выделяют первичную и вторич-
ную формы ожирения. Причина первичного ожирения неизвестна. Вто-
ричное ожирение является симптоматическим и встречается при ряде цере-
бральных эндокринных и наследственных заболеваний.
По внешним проявлениям различают симметричный (универ-
сальный), верхний, средний и нижний типы ожирения. При симметричном ти-
пе жиры относительно равномерно откладываются в разных частях тела.
Верхний тип характеризуется накоплением жира преимущественно в области
подкожной клетчатки лица, затылка, шеи, верхнего плечевого пояса, мо-
лочных желез. При среднем типе жир откладывается в подкожной клетчат-
ке живота в виде фартука, при нижнем типе — в области бедер и го-
леней.
По превышению массы тела больного выделяют несколько степеней
ожирения. При I степени ожирения избыточная масса тела составля-
ет 20-29%, при П-30-49%, при III-50-99% и при IV - до 100% и
более.
При морфологической классификации ожирения учитывают
число адипозоцитов и их размер. На этом основании выделяют гипертрофи-
ческий и гиперпластический типы общего ожирения. При гипертрофиче-
ском типе жировые клетки увеличены в 2 раза и содержат в несколько раз
больше триглицеридов, чем обычные; при этом число адипозоцитов не ме-
няется; течение злокачественное. При гиперпластическом типе число
адипозоцитов увеличено (известно, что число жировых клеток достигает мак-
симума в пубертатном периоде и в дальнейшем не меняется); течение
доброкачественное.
Механизмы развития общего ожирения разнообразны. Во-первых, оно не-
редко возникает в результате несбалансированного питания, превышающего
энергетические затраты организма (алиментарное о ж и р е н и е), что
может быть связано с семейными привычками, профессией (ожирение у пова-
ров, кондитеров). При этом большое значение в развитии ожирения имеет из-
быточное превращение углеводов в жиры, особенно при злоупотреблении бо-
гатой углеводами пищей (метаболическое ожирение). Во-вторых,
ожирение может быть связано с рядом факторов, которые ведут к понижен-
ной мобилизации жира из жировых депо И недостаточному его использова-
нию как источника энергии при нормальном питании. Среди этих факторов
большое значение имеет снижение мышечной активности, хроническая алко-
гольная интоксикация, гипотиреоз и др. В-третьих, к развитию ожирения ве-
дут нарушения нейроэндокринной регуляции жирового обмена (соотношение
липолитических и антилиполитических гормонов). О церебральном
ожирении говорят при развитии патологического процесса (опухоль, энце-
фалит, травма) в подкорковых узлах,- промежуточном мозге. Эндокринное
ожирение возникает при гиперкортицизме (синдром Иценко — Кушинга),
климаксе и евнухоидизме. Ярким примером нейроэндокринного ожи-
рения является адипозогенитальная дистрофия, в основе которой лежит по-
ражение гипофиза и промежуточного мозга. Наконец, в-четвертых, в развитии
ожирения велика роль наследственных (семейно-конституциональных) факто-
ров.
Значение общего ожирения огромно. Будучи проявлением ряда заболева-
ний, оно определяет развитие тяжелых осложнений. Избыточная масса тела,
например, является одним из факторов риска при ишемической болезни
сердца.
Исход общего ожирения редко бывает благоприятным.
При увеличении количества жировой клетчатки, имеющем местный
характер, говорят о липоматозах, Среди них наибольший интерес
представляет болезнь Деркума (lipomatosis dolorosa), при которой в подкож-
ной клетчатке конечностей и туловища появляются узловатые болезненные
отложения жира, похожие на липомы. В основе заболевания лежит полиглан-
дулярная эндокринопатия. Местное увеличение количества жировой ткани не-
редко является выражением вакатного ожирения (жирового замеще-
ния) при атрофии ткани или органа (например, жировое замещение почки или
вилочковой железы при ее атрофии).
Антиподом липоматозов служат регионарные липодистрофии, сущность которых
состоит в очаговой деструкции жировой ткани и распаде жиров нередко с воспалительной реак-
цией и образованием липогранулем (например, липогранулематоз при рецидивирующем
ненагнаивающемся панникулите, или болезни Вебера -Крисчена).
Дата добавления: 2015-11-26 | Просмотры: 1289 | Нарушение авторских прав
|