|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
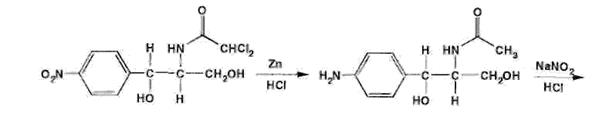
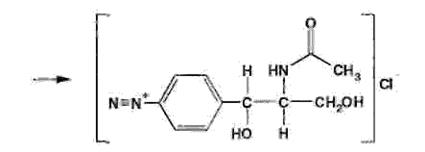
Количественное определение. Около 0,5 г препарата (точная навеска) помещают в коническую колбу емкостью 200-250 мл, прибавляют 20 мл концентрированной соляной кислоты и осторожноОколо 0,5 г препарата (точная навеска) помещают в коническую колбу емкостью 200-250 мл, прибавляют 20 мл концентрированной соляной кислоты и осторожно, небольшими порциями, 5 г цинковой пыли. Затем прибавляют еще 10 мл концентрированной соляной кислоты, обмывая стенки колбы, и после полного растворения цинковой пыли (можно подогреть), раствор количественно переносят в стакан для диазотирования, охлаждаемый льдом; прибавляют 3 г бромида калия и медленно титруют 0,1 мол раствором нитрита натрия. Титрование считают законченным, когда капля жидкости, взятая через 3 минуты после прибавления раствора нитрита натрия, будет вызывать немедленное посинение йодкрахмальной бумаги. 1 мл 0,1 мол раствора нитрита натрия соответствует 0,03231 г C11H12Cl2N2O5, которого в препарате должно быть не менее 98,5%.
Тлев/NaNO2 = (323,13 *0,1)/1000 = 0,0323 a=0,5 Vт = 3,4 мл Х = (3,4*1*0,0323)\0,5 = 0,22 % = (0,22 – 0,108/0,108)* 100% = ± 4% Вывод: ЛФ приготовлена удовлетворительно.
Химический анализ №14 Rp: Sol. Glucosi 5% - 1000 ml Sterilisa! D.S: внутривенно капельно.
Состав: Глюкозы безводной - 50 г Раствора соляной кислоты 0,1 н. - до рН 3,0--4,0 Натрия хлорида - 0,26 г Воды для иньекций - до 1 л
Описание. Бесцветные кристаллы или белый мелкокристаллический порошок без запаха, сладкого вкуса.Растворим в 1,5 ч. воды, трудно растворим в 95% спирте, практически нерастворим в эфире.
Подлинность.
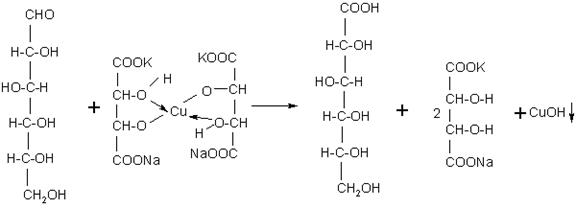
К раствору глюкозы прибавляют 10 мл реактиваФелинга и нагревают до кипениясодержимое пробирки на небольшом пламени спиртовки. По мере нагревания интенсивно – синий цвет реактива Фелинга изменяется. Первоначально появляется желтый осадок гидрата закиси меди, который постепенно переходит в закись меди и выпадает на дно пробирки в виде ярко-красного осадка.
2CuOH → Cu2O ↓ + H2O
Дата добавления: 2015-12-15 | Просмотры: 1402 | Нарушение авторских прав |