|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Plasmodium
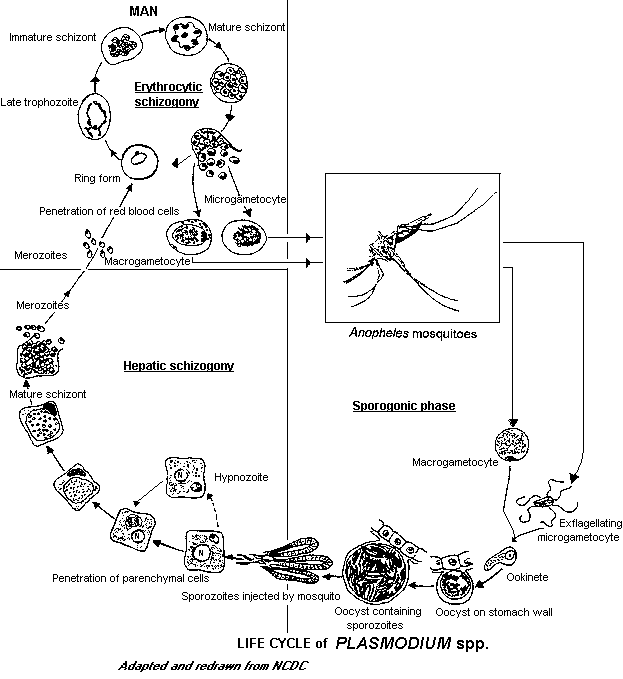
Род включен в состав типа Apicomplexa класса Sporozoea отряда Eucoccidiida подотряда Haemosporma. Род включает более 100 видов, паразитирующих в организмах рептилий птиц и животных. Четыре вида патогенно для человека и вызывает малярию — трансмиссивное заболевание человека, характеризующееся преимущественным поражением ретикулогистиоцитарной системы и эритроцитов, приступами лихорадки, анемией и гепатоспленомегалией. Plasmodium vivax — возбудитель трехдневной малярии, Р. malariae — возбудитель четырехдневной малярии, Р. falciparum — возбудитель тропической малярии, Р. ovale — возбудитель малярии овале (типа трехдневной). Возбудителя малярии (микрогаметы Р. falciparum) в крови человека впервые обнаружил Лаверан (6 ноября 1880 г). Принадлежность возбудителя к споровикам установил И. И. Мечников (1886). Цикл развития паразита в организме, стадии и закономерности появления приступов были установлены Гольджи (1889). Следует отметить, что известны случаи заболевания человека малярией обезьян в эндемичных очагах. Жизненный цикл (Рис. 40) различных видов плазмодиев практически одинаковый (основные различия связаны с образованием поколений поражающих эритроциты) включает бесполую стадию (шизогония), проходящую в организме человека, и половую стадию (спорогония), проходящую в организме переносчика — самок комаров рода Anopheles (цикл Росса).
Рисунок 1. Жизненный цикл различных плазмодиев
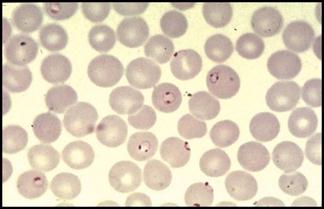
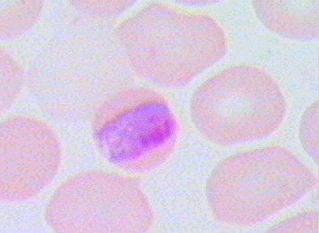
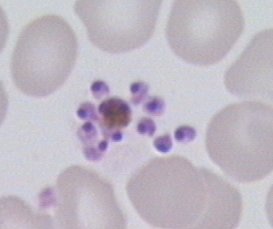
Спорогония малярийного плазмодия происходит в клетках эпителия ЖКТ комара и продолжается 1-3 нед. Процесс начинается с проникновения мужских и женских гамет (гамонтов) в организм комара с кровью больного. Гамонты сливаются попарно в зиготы, проникающие в стенку кишки и образующие там ооцисты. Содержимое ооцист претерпевает процесс спорогонии — многократно делится и образует спорозоиты (веретенообразные клетки длиной 11-15 мкм), диссеминирующие по всему организму насекомого. Часть из них проникает в слюнные железы, делая комара переносчиком болезни. Тканевая или экзоэритроцитарная шизогония плазмодия происходит в гепатоцитах человека и продолжается 1-2 нед (цикл размножения Р. falciparum и Р. malarie впечени варьирует в пределах 10-18 сут). Через час после кровососания спорозоиты проникают с кровотоком в клетки печени где размножаются и делятся. В результате деления образуются мерозоиты (каждый спорозоит может образовать от 2000 до 40 000 мерозоитов), разрушающие гепатоциты и проникающие в кровоток. Эритроцитариая шизогония происходит после проникновении мерозоитов в эритроциты. Проникшие в клетки мерозоиты превращаются в трофозоиты (растущие формы) размером 2 мкм, микроскопия пораженных эритроцитов выявляет покоящиеся формы, содержащие ядро с одним хроматиновым зерном (Рис. 41), и формы с псевдовакуолью, внешне напоминающие перстень или кольцо (Рис. 42).
Рисунок 2. Покоящиеся формы, содержащие ядро с одним хроматиновым зерном (Р falciparum)
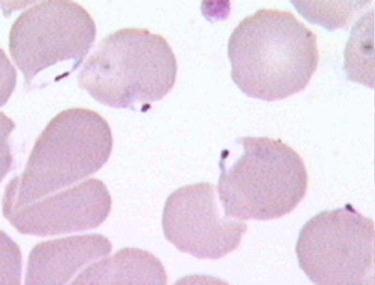
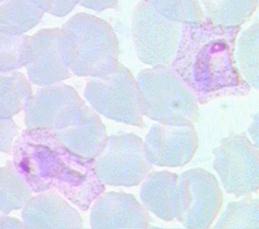
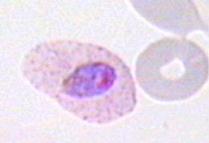
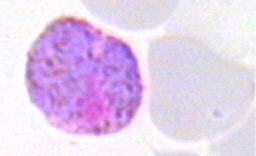
Рисунок 3. Формы с псевдовакуолью, внешне напоминающие перстень или кольцо (Р. falciparum) Размеры трофозоитов Р. falciparum меньше половины эритроцита и не вызывают его деформации. Трофозоиты Р. vivax больше по размерам, имеют псевдоподии и способны передвигаться внутри эритроцита (отсюда vivax — живой), вызывая увеличение и деформацию клеток (Рис. 43).
Рисунок 4. Трофозоиты Р. vivax Несмотря на наличие нескольких псевдоподий, трофозоиты Р malariae практически неподвижны в мазках часто выглядят как тельца включений или ленты. Пораженные эритроциты не деформированы (Рис. 44).
Рисунок 5. Трофозоиты Р. malariae
Поскольку Р. ovale занимает промежуточное положение между Р. vivax и Р. malariae, то он деформирует около 60% инфицированных эритроцитов делая их овальными (Рис. 45).
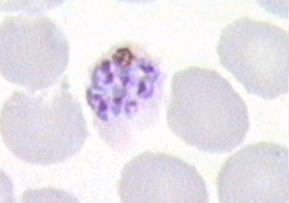
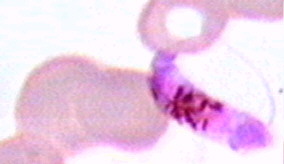
Рисунок 6. Трофозоиты Р. ovale Трофозоиты позднее увеличиваются и образуют многоядерные шизонты (делящиеся формы). Шизонты образуют новое поколение мерозоитов. Каждая клетка может образовывать 6-24 дочерних мерозоита инфицирующих другие эритроциты (Рис. 46, 47).
Рисунок 7. Многоядерныйшизонт
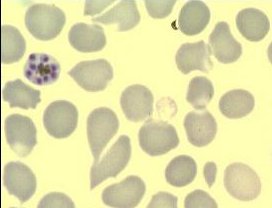
Рисунок 8. Многоядерныйшизонт Выход мерозоитов из эритроцита сопровождается его разрушением (Рис. 48).
Рисунок 9. Выход мерозоитов из эритроцита
Указанный цикл развития для Р. malariae составляет 72 ч, для других видов — 48 ч. С наступлением эритроцитарной шизогонии размножение Р. malariae и Р. falciparum в печени прекращается, однако у Р. vivax и Р. ovale часть спорозоитов (гипнозоиты) остаётся в гепатоцитах, образуя «дремлющие» очаги, дающие отдалённые рецидивы. В некоторых эритроцитах из макрогаметоцитов (Рис. 49) развиваются женские, из микрогаметоцитов (Рис. 50) мужские гамонты, завершающие своё развитие только в организме комара в течение 7-45 сут (в зависимости от температуры воздуха).
Рисунок 10. Макрогаметоцит
Рисунок 11. Микрогаметоцит
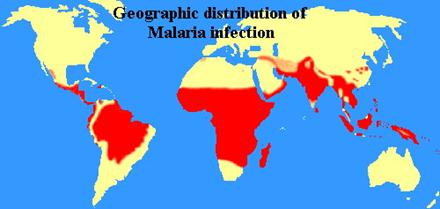
Эпидемиология. История заболевания насчитывает не одно тысячелетие. В Европе первое упоминание относят к V в. и связывают с именем Гиппократа. Позже древнеримский писатель Варрон (Varro, 116-28 гг. до н.э.) указывал на наличие в болотистых местах неких мельчайших, невидимых глазу существ, проникающих с «дурным воздухом» (mal'aria) в организм, что дало начало известной «миазматической» теории развития заболеваний. В опубликованном в 1717 г. сочинении «De noxiis paludum effluviis eurumque remedies» («O вредных испарениях болот») итальянский естествоиспытатель Ланчизи подчёркивал роль стоячих водоёмов в распространении болотной лихорадки. Распространение. Малярию выявляют повсеместно (Рис 51) от 45° северной до 40° южной широты (но чаще в тропиках и субтропиках) на высоте от 0 до 1 800 м над уровнем моря. В странах с умеренным климатом более часто выделяют Р. vivax, реже — Р. malariae. В тропиках основной возбудитель — Р. falciparum, и лишь спорадически в африканских странах выделяют Р. ovale. В 40-50-х гг. значительная часть очагов малярии в Европе и США была уничтожена применением инсектицидов, в частности ДДТ.
Рисунок 12. Распространение малярии Заболеваемость. Ежегодно в 104 эндемичных странах заболевают около 250 млн человек. Смертельные исходы чаще всего наблюдают среди детей, но также регистрируют среди неиммунизированных взрослых (1-2 млн ежегодно). Заболеваемость напрямую зависит от размеров популяции комаров и количества больных, служащих резервуаром инфекции. В связи с развитием индустрии туризма заболевание выявляют в странах, лежащих за пределами естественного ареала. Анализ эпидемиологических факторов показывает, что передача инфекционного агента в большинстве случаев носит горизонтальный характер (распространение в течение эпидемического сезона возможно только через комара); что касается вертикальной передачи (наличие преемственной связи между сезонами), то она встречается редко. Подобные ситуации опосредуют лица-гамонтоносители, количество которых часто недооценивают. Следует учитывать, что в селезёнке количество гамонтов превышает таковое в периферической крови. Фактическое количество гамонтоносителей составляет 20-80% всех паразитоносителей. Клинические проявления. В зависимости от вида возбудителя инкубационный период при малярии варьирует от 8 до 25 сут (при трёхдневной малярии может достигать 8-14 мес). Для всех форм типичны лихорадка, анемия и нарушения кровообращения. Проявления заболевания развиваются при разрушении эритроцитов периферической крови. Наиболее тяжело протекает тропическая малярия. Лихорадка наблюдается в момент выхода мерозоитов из разрушенных эритроцитов; интервалы между проявлениями приступов зависят от биологического цикла паразита. Начало острое, температура тела может достигать 40-41,7 °С (обычно подъём наблюдают в дневное время). Через несколько часов она литически снижается до 35-36 °С. При разрушении эритроцитов в кровь выделяется эндопироген, структура которого остаётся неидентифицированной (определённая роль может принадлежать гематину). Определённую роль в развитии лихорадочной реакции могут играть ИЛ-1 и фактор некроза опухолей, выделяемые макрофагами, активируемыми во время утилизации остатков эритроцитов. Анемия — следствие массивного лизиса эритроцитов и фагоцитоза поражённых клеток фагоцитами. При тропической малярии, вызванной Р. falciparum, развивается черно-водная лихорадка (гемоглобинурийная лихорадка). Характерны острый массивный гемолиз, гемолитическая желтуха, боли в пояснице, гемоглобинурия. Может развиться как осложнение малярии, возникающее после приёма хинина и примахина; чаще возникает у лиц с повышенной ломкостью эритроцитов. Вследствие наследственного дефекта глюкозо-6-фосфатдегидрогеназы по типу анемии Маркиафавы-Микели, а также как реакция ГЗТ на хинин; комплексы хинин-АТ сорбируются на мембранах эритроцитов, активируют комплемент, что приводит к их генерализованному разрушению. Значительно реже и лишь при тропической малярии наблюдают внутрисосудистый гемолиз. Нарушения кровообращения в первую очередь опосредованы подъёмами температуры тела. Дилатация сосудов приводит к снижению ОЦК и АД. Последующий спазм сосудов, повышенная вязкость крови, закупорка капилляров остатками эритроцитов приводят к ишемии органов и тканей. Иногда тропическую (falciparum) малярию сопровождает острый гломерулонефрит. При хроническом заболевании, вызванном Р. malariae, может развиться прогрессирующая почечная недостаточность. Механизмы нефропатологии при малярии по большей части опосредованы аутоиммунными механизмами. Заболевание часто сопровождают спленомегалия (увеличение не всегда соответствует тяжести заболевания) и тромбоцитопения. Поражения органов ЖКТ достаточно многообразны — от гангренозно-язвенных до холероподобных. Печень обычно увеличена, гиперемирована и окрашена в тёмно-коричневый цвет. При хронических поражениях её масса достигает 3-5 кг. Нередки поражения поджелудочной железы вплоть до фиброзного панкреатита. Иммунные реакции Проникновение плазмодиев в кровоток индуцирует развитие иммунного ответа, направленного на подавление активности возбудителя и значительно смягчающего тяжесть клинических проявлений. Отмечены случаи абсолютной резистентности к инфекции, опосредованные иммунными и генетическими механизмами, передающимися по наследству. Поскольку заболевание носит длительный циклический характер, уровень иммунного ответа постоянно нарастает. Под воздействием иммунных механизмов цикл шизогоний постепенно замещается спорогониями со смягчением симптоматики. В редких случаях возможно спонтанное выздоровление. В подавлении размножения плазмодиев задействованы гуморальное и клеточное звенья иммунного ответа. Однако, степень их участия неопределена. Дата добавления: 2015-02-02 | Просмотры: 1517 | Нарушение авторских прав |