|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Toxoplasma gondii
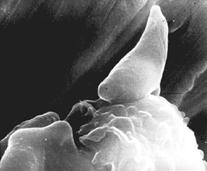
Вид включен в состав типа Apicomplexa класса Sporozoea отряда Eucoccidiida подотряда Eirnenina семейства Emeriidae. Вызывает токсоплазмоз — паразитарную инфекцию, характеризующуюся хроническим течением, поражением нервной системы, увеличением печени и селезенки, частым поражением скелетных мышц и миокарда. Toxoplasma gondii — внутриклеточный паразит морфологически напоминающий вытянутую дольку апельсина (рис. 59).
Рисунок 59.Рисунок 52. Toxoplasma gondii. Электронная микрофотография
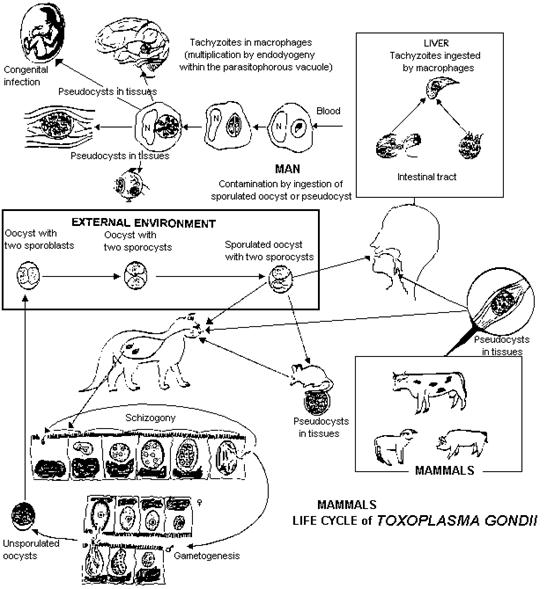
Длина 4-7 мкм, один конец закруглен. По Романовскому-Гимзе цитоплазма окрашивается в голубой цвет, ядро — в красно-фиолетовый. В 1908 г. впервые возбудитель выделен Ш. Николем и А. Мансо в Тунисе у грызунов гонди (Ctenodactylus gundi) и А. Сплендоре в Бразилии у кроликов. Заболевание распространено повсеместно. Возбудитель выделен практически от всех млекопитающих и многих птиц. Заражение человека происходит алиментарным путем при проникновении ооцист или тканевых цист (при употреблении сырых или полусырых мясных продуктов, но чаще с немытыми овощами и фруктами), реже через кожу (при разделке туш, работах с лабораторным материалом) и трансплацентарно от беременных (в среднем 1:2700 нормальных родов). Вероятность заболевания токсоплазмозом увеличивается с возрастом. Серологическое обследование установило инфицированность Т. gondii 50% взрослых американцев. Инфицированность населения разных стран составляет от 4 до 68%. Жизненный цикл включает стадии полового и бесполого размножения (рис. 60).
Рисунок 60.Рисунок 53. Жизненный цикл
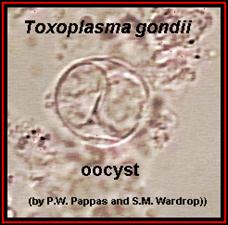
Первичные и основные хозяева — домашние кошки и прочие представители семейства кошачьих, в организме которых происходит половое размножение возбудителя. Первичное заражение кошек происходит при поедании грызунов содержащих ооцисты, из которых выходят паразиты (спорозоиты) проникающие в клетки кишечника и превращающиеся в трофозоиты которые размножаются бесполым путем (шизогония). Половое размножение возбудителя также происходит в клетках слизистой оболочки кишечника. Образовавшиеся в результате бесполого размножения мерозоиты разрушают эпителиальные клетки и проникают в подлежащие слои кишечной стенки, где трансформируются в гаметоциты. Слияние разнополых гаметоцитов приводит к образованию зиготы (ооцисты). Ооцисты — округлые образования с плотной бесцветной двухслойной оболочкой диаметром 9-14 мкм (рис. 61, 62). Из организма кошек выделяются с испражнениями. Ооцисты хорошо сохраняются в почве, животные в том числе грызуны заражаются при их заглатывании. Весь цикл репродукции в организме окончательного хозяина занимает 1-3 нед.
Рисунок 61.Рисунок 54. Ооцисты. Неокрашенный препарат.
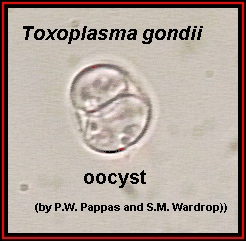
Рисунок 62.Рисунок 55. Ооцисты. Неокрашенный препарат.
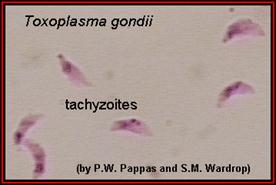
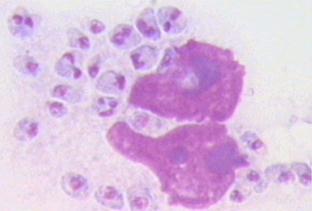
Промежуточные хозяева. Токсоплазмы поражают человека, многих диких и домашних животных и птиц, в организме которых паразит проходит бесполый цикл развития и размножения. Из проникших в организм ооцист выходят паразиты, активно поглощаемые макрофагами. Фагоцитоз носит незавершенный характер. Возбудитель (спорозоиты) диссеминирует по лимфатическим сосудам с макрофагами. В цитоплазме макрофагов начинается первый этап шизогонии. На более поздних этапах шизогонии макрофаги погибают и высвободившиеся (рис. 63) паразиты (тахизоиты) инвазируют в клетки организма (подвержены любые ядросодержащие клетки).
Рисунок 63.Рисунок 56. Высвобождение тахизоитов из клетки
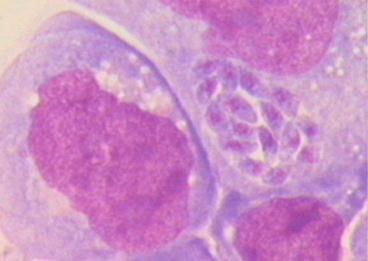
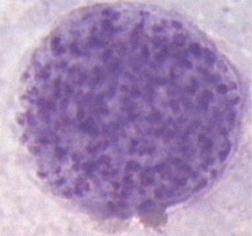
Для острой стадии инфекции характерно образование в пораженных клетках скоплений (рис. 64, 65) токсоплазм (псевдоцисты). При их разрушении паразиты инвазируют соседние клетки и цикл повторяется. Паразитемия развивается только в острой стадии.
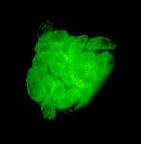
Рисунок 64.Рисунок 57. Образование псевдоцист
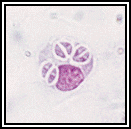
Рисунок 65.Рисунок 58. Образование псевдоцист (Обработка люминесцирующими моноклональными антителами) При хронических процессах возбудитель образует истинные цисты (рис. 66) с плотной оболочкой (средний размер 100 мкм). Каждая циста содержит более сотни паразитов (брадизоиты), расположенных так плотно, что на препаратах видны одни ядра. Эта фаза — конечная для паразита в организме всех животных, исключая окончательного хозяина, в котором завершается жизненный цикл.
Рисунок 66.Рисунок 59. Циста. Содержит более сотни паразитов (брадизоиты), расположенных так плотно, что на препарате видны одни ядра. Клинические проявления. Большинство случаев токсоплазмоза протекает бессимптомно. На характер проявлений существенно влияет общее состояние организма. У здоровых людей токсоплазмоз может проявляться умеренной лимфаденопатией (обычно шейных лимфатических узлов). Прочие проявления могут включать фарингит лихорадку, сыпь гепатоспленомегалию и атипичный лимфоцитоз. Часто заболевание имитирует инфекционный мононуклеоз. В тяжелых случаях можно наблюдать менингоэнцефалит, пневмонию, хориоретинит, эндокардит и поражения внутренних органов. У лиц с иммунодефицитами, включая СПИД, заболевание приобретает тяжелый преимущественно фатальный характер. Наиболее часто наблюдают активизацию латентной инфекции на фоне приема иммунодепрессантов. У подобных пациентов острое заболевание может приводить к некротизирующему энцефалиту, эндокардиту и пневмониям. Наиболее частое и грозное осложнение — энцефалит (выявляют у 50% больных), дающий до 90% всех летальных исходов при токсоплазмозе. Врождённый токсоплазмоз. При заражении беременной женщины возбудитель проникает в плод через плаценту. В результате плод либо погибает (выкидыш, мертворожде ние), либо рождается с симптомами острого врожденного токсоплазмоза — интоксикацией, лихорадкой, желтушностью, поражениями печени, селезёнки, лимфатических узлов и ЦНС. Нарушения более выражены при заражении в I триместр беременности. Лабораторная диагностика. Выявление возбудителя проводят микроскопией полученных образцов, возможно выделение токсоплазм из биоптатов и биологических жидкостей с последующим культивированием на 10-11 суточных куриных эмбрионах или клетках HeLa. В лечебных учреждениях наиболее доступны серологические тесты на выявление возбудителя. Микроскопия. При подозрении на токсоплазмоз исследуют кровь, СМЖ, пунктаты лимфатических узлов, остатки плодных оболочек, а также трупный и биопсийный материалы К результатам микроскопии следует относиться с осторожностью, т. к. необходимо дифференцировать острую инфекцию от латентной хронической. Мазки и срезы окрашивают по Романовскому-Гимзе или Райту. Выявление Т. gondii в тканях мозга осуществляют электронной микроскопией, либо различными иммунофлюоресцентными методами. Биологическая проба. Наибольшую ценность имеет выделение токсоплазм, полученных от животных, зараженных клиническим материалом. Белым мышам парентерально вводят кровь лиц, подозрительных на наличие токсоплазм, что помогает выявить острую форму болезни микроскопией образцов тканей зараженных животных. Серологическая диагностика. AT к токсоплазмам выявляют с помощью РСК, РПГА, латекс агглютинации. Определение IgM. AT появляются на ранних сроках заболевания. Этот факт используют для диагностики наследственного токсоплазмоза, т. к. IgM не проходят через плаценту и их наличие у новорожденного свидетельствует об инфицировании. AT можно идентифицировать методом непрямой иммунофлюоресценции. Титры равные 1:80 и выше указывают на наличие токсоплазмоза. Тесты относительно неспецифичны, трудно поддаются стандартизации и в широкой практике не применяются у новорожденных и пациентов с иммунодефицитами. Определение IgG. Образование AT достигает своего пика на 4-8 нед. Обычные титры AT — 1:1000 и выше. Наибольшее распространение получил метод непрямой иммунофлюоресценции. Высокоспецифична и чувствительна проба Сэбина- Фельдмана на окрашивание токсоплазм. Тест технически труден и не совсем безопасен, но до развития иммунофлюоресцентных методов сохранял свое значение как самый надёжный способ серологической диагностики. Необходимо использовать парные сыворотки, 4-кратное увеличение титров свидетельствует об острой инфекции. В настоящее время разработаны ИФА и РИА, основанные на выделении IgG. Особенно широко их используют у новорождённых и пациентов с иммунодефицитами. Наиболее доступный способ диагностики — кожная проба с токсоплазмином. Проба положительна с 4 нед заболевания и сохраняется в течение многих лет. Положительный результат свидетельствует лишь о заражении в прошлом и указывает на необходимость более тщательного обследования. Дата добавления: 2015-02-02 | Просмотры: 1644 | Нарушение авторских прав |