 |
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
ОСНОВЫ ЯДЕРНОЙ ФИЗИКИРадиоактивность - это свойство ядер атомов определенных элементов самопроизвольно (т.е. без каких-либо внешних воздействий) превращаться в ядра атомов других элементов с испусканием при этом ионизирующих излучений. Превращение элементов в таких случаях называется радиоактивным распадом. Радиоактивные явления, встречающиеся у природных изотопов, называются естественной радиоактивностью, а происходящие в искусственно полученных изотопах химических элементов - искусственной радиоактивностью. Для понимания явления радиоактивности необходимо вспомнить строение атома. Он состоит из положительно заряженного ядра и вращающихся вокруг него отрицательно зараженных электронов. Ядро состоит из протонов и нейтронов, которые объединяются общим понятием - нуклоны. В нейтральном атоме число протонов в ядре равно числу электронов в оболочке. Нуклоны в ядре непрерывно обмениваются особыми частицами, которые называются π-мезонами, или квантами ядерного поля. Атомный номер Z равен числу протонов в ядре, а следовательно, и заряду ядра. Атомы одного и того же химического элемента имеют одинаковый атомный номер и массу. Масса нуклона примерно в 1840 раз больше массы электрона. В связи с незначительностью массы электрона его массу принято считать равной нулю, поэтому масса атома определяется массой ядра. Массовое число А равно числу нуклонов в ядре. Массовое число атома указывается вверху слева от символа химического элемента. Атомный номер (заряд) элемента записывается внизу слева от символа элемента.
Альфа-распад. Характерен для ядер тяжелых элементов с малыми энергиями связи. В процессе внутриядерных превращений из ядра атома выбрасывается альфа-частица. Заряд ядра уменьшается на 2 единицы, а атомная масса - на 4 единицы. Альфа-частица представляет собой ядро атома гелия. Ее атомная масса составляет 4 единицы. Заряд равен +2. При относительно крупных размерах и большом заряде частица обладает высокой энергией (3-10 Мэв), для нее характерны большая линейная передача энергии (ЛПЭ) и значительная линейная плотность ионизации (ЛПИ). Размер, заряд и энергия альфа-частицы обусловливают ее многочисленные столкновения с атомами вещества. При увеличении плотности и атомной массы вещества повышается ЛПЭ. Одновременно увеличивается сила торможения частиц и повышается ЛПИ. Она максимальна в конце пути пробега частицы. Естественно, обладая большой массой, зарядом и энергией, альфа-частица не может иметь значительной проникающей способности, так как быстро тормозится веществом. Так, в зависимости от энергии, пробег альфа-частиц в разных средах невелик: в воздухе он составляет 2-10 см, в алюминии - 15-70 мкм, в воде и биологических тканях - 30-130 мкм, т.е. в коже альфа-частицы задерживаются эпидермисом, не достигая глубоких слоев эпителия. Обыкновенный лист бумаги является для них абсолютным экраном. Поэтому внешнее воздействие альфа-излучения на человека практически безопасно. Однако поступление альфа-частиц внутрь организма, например с пищей и, особенно, с воздухом в виде радона - крайне опасно, поскольку значительно повышается риск канцерогенного действия. Альфа-частицы в таких условиях легко проникают через слизистые оболочки и создают внутри тканей и органов высокую плотность ионизации, чем и обусловлен выраженный патогенный эффект. Электронный бета-распад характерен для превращений естественных и искусственных радионуклидов. При данной схеме распада бета-излучение - это поток электронов. Электронный бета-распад возникает в тех случаях, когда в ядре неустойчивость вызвана превышением количества нейтронов над числом протонов. При этом в ядре появляется электрон, а один из нейтронов превращается в протон. Электрон выбрасывается из ядра, заряд ядра увеличивается на единицу, а массовое число остается без изменения. Бета-излучение одного и того же элемента содержит электроны различной энергии - от самой малой до некоторой максимальной величины. Поэтому спектр излучения непрерывный или сплошной. Установлено, что вместе с бета-частицей из ядра выбрасываются нейтральные частицы ничтожно малой массы, составляющие с электронами некую постоянную величину. Эти частицы носят название антинейтрино. Возвращение возбужденного ядра в основное состояние сопровождается испусканием гамма-квантов. Позитронный fi-распад наблюдается у некоторых искусственных радионуклидов. Позитрон - это элементарная частица, подобная электрону, но обладающая положительным зарядом. При выбросе позитрона один из протонов в ядре превращается в нейтрон. Вместе с позитронами выбрасываются нейтрино, которые вместе с позитроном составляют некоторую постоянную величину энергии. Спектр излучения, как и при электронном распаде, сплошной. Позитронный бета-распад также сопровождается гамма-излучением. Удельная плотность ионизации для бета-частиц - в несколько сотен раз меньше, чем у альфа-частиц. При этом за счет меньшей массы, заряда и энергии у бета-частиц в 100 и более раз увеличивается длина пробега в веществе. Так, в воздухе она составляет от нескольких метров до нескольких десятков метров, а в биологических тканях - нескольких десятков сантиметров. Бета-частицы имеют разную энергию, поэтому при защите от внешнего воздействия бета-излучения следует использовать экран, поглощающий бета-частицы с максимальной энергией. Применяются экраны из легких материалов с малым атомным номером, например из стекла, полимерных материалов, алюминия. При изготовлении экранов из тяжелых металлов бета-частицы будут генерировать тормозное рентгеновское излучение, от которого также необходима защита. К-захват является еще одним видом радиоактивных превращений. При избытке протонов в ядре атома ядро захватывает электрон с ближайшей к ядру К-оболочки, а на его место переходит электрон с более дальних оболочек. Образуется частица нейтрино, которая является единственной частицей, вылетающей из ядра атома при К-захвате. Поскольку энергия генерируется на электронных оболочках при переходах электронов, то возникает характеристическое рентгеновское излучение с дискретным линейчатым спектром, свойственным для тех уровней, на которых происходят переходы электронов в атоме данного вещества. Деление ядер тяжелых элементов. Этот процесс характерен для ядер атомов элементов с большой атомной массой, таких как 235U, 239Pu и др. В результате ядерного превращения образуются ядра легких элементов с большими энергиями связи и избыточное количество нейтронов. Новые ядра нестабильны и могут превращаться в ядра более легких элементов. При этом выделяется большое количество энергии. Образующиеся нейтроны используются в дальнейших повторных превращениях ядер тяжелых элементов. Подобный принцип получения энергии с помощью управляемой цепной реакции деления ядер тяжелых элементов лежит в основе работы энергетических ядерных реакторов. Если же эта реакция становится неуправляемой, то увеличение числа нейтронов и количества энергии происходит в геометрической прогрессии. Такая цепная реакция приводит к ядерному взрыву. Термоядерные реакции. Кроме естественных ядерных превращений, возможно также искусственное превращение ядер легких элементов (изотопов водорода дейтерия и трития) в ядра более тяжелых элементов. Такая реакция используется при взрыве термоядерной (водородной) бомбы, где роль пускового механизма создания исходной высокой температуры, необходимой для придания большой кинетической энергии и сближения ядер легких элементов, принадлежит плутониевому запалу. После запуска плутониевого запала создаются условия неуправляемой термоядерной реакции. Следует отметить, что и распад ядер тяжелых элементов, и термоядерные реакции сопровождаются выделением мощных потоков гамма-излучения. Удельная плотность ионизации у гамма-квантов минимальная, заряд и масса отсутствуют, поэтому длина пробега у них довольно большая и может достигать в воздухе нескольких сотен метров. Биологические ткани практически не являются экранами. Поэтому гамма-излучение является весьма опасным источником внешнего облучения для человека. В связи с этим экраны для защиты от гамма-излучения должны быть из материалов с высокой плотностью, с большим количеством ядер и большими электронными оболочками атомов. Количественная характеристика радиоактивности. Изучение скорости радиоактивного распада ядер радионуклидов позволило выявить определенную закономерность. Установлено, что распаду подвергаются не все атомы одновременно, а за каждый промежуток времени распадается строго постоянная доля атомов радиоактивного изотопа. Эта величина индивидуальна и постоянна для каждого радиоактивного элемента. Она называется постоянной распада и обозначается λ (1/сек = сек-1). Постоянная распада показывает долю атомов, которые распадаются в массе радиоактивного вещества за единицу времени. Соответственно, закон радиоактивного распада может быть сформулирован следующим образом: за равные промежутки времени происходит превращение равных долей радиоактивных атомов изотопа. Математически его выражение выглядит следующим образом:
Зная постоянную распада, можно рассчитать время, за которое распадется половина атомов изотопа, т.е. период полураспада (Т):
уменьшатся вдвое, а сама экспонента бесконечно приближается к горизонтальной линии, но никогда ее не пересекает. В радиационной гигиене принято, что активность радиоактивного элемента становится незначительной через 8-10 периодов полураспада. Периоды полураспада значительно различаются у разных изотопов. Короткоживущими считаются такие изотопы, у которых период полураспада составляет от долей секунды до нескольких суток, долгоживущими - у которых этот период колеблется от нескольких месяцев до миллиардов лет. Например: для Т 24Na = 15,06 ч, 131I - 8,06 суток, 60Со - 5,3 года, 90Sr - 29 лет, 129I - 15,7 млн лет. Активность радиоактивного вещества показывает скорость распада ядер в изотопе за единицу времени. Поэтому активность радиоактивного вещества возрастает с увеличением массы изотопа, а также с уменьшением атомной массы и периода полураспада. За единицу активности радиоактивного вещества в системе СИ принят беккерель (Бк) -такая активность, при которой в источнике происходит одно превращение ядра за 1 с. Чтобы представить величину данной единицы, следует отметить, что допустимая радиоактивность питьевой воды по бета-излучению составляет 1 Бк/л, а по альфа-излучению - 0,1 Бк/л. Однако исторически сложилось так, что первой установленной единицей активности является кюри (Ки)1. Она была впервые предложена Марией Кюри и названа в честь Пьера и Марии Кюри. Кюри - это очень большая единица по величине активности: 1 Ки = 3,7 х 1010 Бк. Дата добавления: 2014-12-12 | Просмотры: 1512 | Нарушение авторских прав |
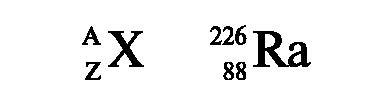 Атомы, ядра которых состоят из одинакового числа протонов, но различного числа нейтронов, называются изотопами (изо...+ гр. topos - место).
Атомы, ядра которых состоят из одинакового числа протонов, но различного числа нейтронов, называются изотопами (изо...+ гр. topos - место).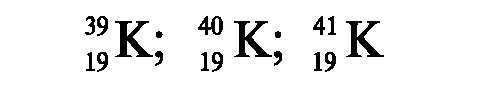 Различают несколько видов радиоактивных превращений ядер, сопровождающихся различными видами ионизирующих излучений.
Различают несколько видов радиоактивных превращений ядер, сопровождающихся различными видами ионизирующих излучений.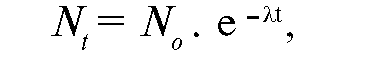 где N - количество активных атомов в изотопе через промежуток времени t; No - количество активных атомов в изотопе в начальных условиях; λ - постоянная распада изотопа; e - основание натуральных логарифмов.
где N - количество активных атомов в изотопе через промежуток времени t; No - количество активных атомов в изотопе в начальных условиях; λ - постоянная распада изотопа; e - основание натуральных логарифмов. Графически эта зависимость выглядит в виде экспоненты, где количество активных атомов через каждый период полураспада
Графически эта зависимость выглядит в виде экспоненты, где количество активных атомов через каждый период полураспада