|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Причины развития ишемии толстой кишки после аортальных реконструкцийРазвитие толстокишечной ишемии после аортальных реконструкций процесс, как правило, многофакторный [Покровский А.В., 1979]. Развитие острых нарушений висцерального кровообращения, а следовательно, и кишечной ишемии после аортальных реконструкций связывается со многими факторами: 1) необоснованным или непра 2) объемом поражения висцеральных ветвей и значимостью этих артерий в висцеральном кровообращении; 3) состоянием и функционированием межбрыжеечного анастомоза. Среди различных причин возникновения острых нарушений мезенте-риального кровообращения и развития толстокишечной ишемии выдвигается и фактор "обкрадывания", возникающий после аортобедрен-ных реконструкций, вследствие перераспределения большого потока крови в нижние конечности. Этот феномен известен в литературе под названием "синдром аортоподвздош-ного обкрадывания". А.В. Покровский и соавт. (1979) считают, что синдром "аортопод-вздошного обкрадывания" имеет ге-модинамическое значение при условии гемодинамически значимого поражения висцеральных артерий и наличия клинической картины "angina abdominalis". Последствия толстокишечной ишемии сопровождаются воздействием токсичных метаболитов на молекулярную оксигенацию, образованием супероксидаз и гидроксильных свободных радикалов. Ксантиноксидаза является источником супероксидных радикалов. Супероксид сам по себе очень токсичен для внутриклеточного матрикса и клеточных мембран. Такое ишемически-реперфузионное повреждение может быть непосредственной причиной снижения рН на слизистой сигмовидной кишки. В процессе ишемии ксантиндегид-рогеназа, в большом количестве содержащаяся в слизистой оболочке кишечника, превращается в ксантин-оксидазу, обеспечивающую механизм образования свободных радикалов с развитием в последующем деструкции клеток слизистой толстой кишки с потерей интеграции для обеспечения клеточного кишечного барьера. Утрата кишечного барьера влечет за собой попадание патогенных бактерий из просвета кишечника в системный кровоток. Развивающиеся в результате эндотоксемия и сепсис могут спровоцировать возникновение полиорганной недостаточности. Клиническая картина ишемии толстой кишки. В зависимости от тяжести развития циркуляторных расстройств висцерального кровообращения после аортальных реконструкций клинические проявления толстокишечной ишемии варьируют от субклинических форм до развития гангрены и перфорации толстой кишки с последующим обычно тяжелым каловым перитонитом. Данные литературы утверждают, что у целого ряда пациентов ишемия толстой кишки протекает в виде субклинических форм, изменения в кишечнике носят обратимый характер, поэтому часто остаются нераспознанными [Покровский А.В. и др., 1979; Ernst et al., 1976]. Однако подобное преходящее течение толстокишечной ишемии наблюдается далеко не всегда. Значительно чаще наблюдаются те случаи, когда после обширного по объему оперативного вмешательства, неминуемо сопровождающегося в послеоперационном периоде развитием болевого синдрома, нередко тяжелого пареза кишечника, забрю-шинной гематомы, гипертермии и других системных реакций, клинические проявления тяжелой толсто-кишечной ишемии нередко могут быть смазаны и замаскированы, что, естественно, приводит к запоздалой диагностике, развитию обширного по объему некроза кишки, калового перитонита и высокой летальности. B.C. Савельев и И.В. Спиридонов (1979) считают, что при возникновении острых нарушений мезентери-ального кровообращения начало заболевания может быть острым, постепенным, в два этапа и с продромой. Авторы также выделяют 3 стадии течения патологического процесса: 1) стадию ишемии; 2) стадию инфаркта; 3) стадию перитонита. После реконструкции аорты клинические симптомы могут возникать в течение 14 дней, однако у 75 % пациентов они наступают уже в первые 24—48 ч после оперативного вмешательства. Стадия ишемии начинается сразу же после возникновения нарушения мезентериального кровообращения и более чем у половины больных продолжается в течение первых 6 ч, а у остальных пациентов может длиться до 3—4 сут. Быстрое течение этой стадии характерно для атероэмболиз-ма с развитием окклюзии дистальных ветвей висцеральных артерий, при неправильной перевязке нижней брыжеечной артерии или при пересечении во время реконструктивного вмешательства основных коллатеральных магистралей. У остальных пациентов стадия ишемии носит более продолжительный характер и нередко может быть обратимой. Продолжительность стадии инфаркта обычно 12—24 ч. Однако у ряда больных она протекает до 48 ч и более. В основном это зависит от объема поражения кишечника. Клинически стадия перитонита становится более отчетливой через 12—24 ч после ее возникновения, но особенно она выражена на 2-е, 3-й и 4-е сутки. Клинические проявления толсто-кишечной ишемии могут быть замаскированы или осложнены системными реакциями. В стадии ишемии состояние больных то ухудшается, то улучшается (транзиторная ишемия). Периодически возникают вздутие живота, тошнота, резкая слабость, больные беспокойны. Затем живот опадает, появляется, как правило, жидкий стул, общее состояние пациентов улучшается. Такая клиническая картина может продолжаться несколько дней и либо исчезает, либо развивается стадия инфаркта. В стадии перитонита большинство больных лежат, не двигаясь, не делая резких движений, так как при этом усиливаются боли. Боли в животе — основной и наиболее яркий симптом заболевания. Однако, учитывая тот факт, что пациенты в послеоперационном периоде получают обезболивающие средства, болевой синдром может быть не столь интенсивен, а главное, неправильно интерпретирован. Правосторонняя локализация болей наблюдается при поражении слепой кишки и правой половины толстой. Чаще возникает левосторонняя локализация болевого синдрома вследствие поражения левой половины толстой и сигмовидной кишки. Тошнота и рвота — характерные признаки болезни. Большое диагностическое значение приобретает рвота с примесью крови. Источником кровотечения нередко могут быть остро развившиеся эрозии слизистой оболочки желудка, возникшие вследствие сопутствующей рефлекторной ишемии. Для острых нарушений мезентери-ального кровообращения характерным является сохранение эвакуатор-ной функции кишечника. Задержка стула и газов наблюдается довольно редко и преимущественно в стадии перитонита. Сифонная клизма при острой толстокишечной ишемии является грубой тактической ошибкой, так как может привести к перфорации кишечной стенки и развитию разлитого калового перитонита. В стадии ишемии очень важным в диагностическом плане является появление после начала болей одно-, двукратного жидкого стула. Этот симптом принято называть "ишемичес-ким опорожнением кишечника". У ряда больных в стадии ишемии возникает длительная диарея — один из наиболее частых симптомов толстокишечной ишемии. Появление диареи объясняется частичным сохранением кровотока в ишемизиро-ванной зоне кишечника. Очень важный диагностический симптом — появление крови в испражнениях. Правда, этот симптом обычно появляется в стадии инфаркта, но довольно часто и в стадии перитонита. Выделения с примесью крови по виду напоминают "малиновое желе". По мнению B.C. Савельева и И.В. Спиридонова (1979), болезненность живота в стадии ишемии отсутствует более чем у половины больных. В стадии инфаркта и перитонита последняя наблюдается практически у всех больных. Развитие перитонита при поражении левой половины толстой и сигмовидной кишки имеет свои характерные особенности. В первую очередь, как правило, развиваются деструктивные изменения в сигмовидной кишке. Вследствие слабого, но довольно длительно сохраняющегося коллатерального притока крови деструкция может продолжаться в течение длительных сроков, поэтому довольно часто в сигмовидной кишке образуются язвы, перфорация которых ускоряет развитие перитонита. Перитонит начинает формироваться обычно в левой подвздошной области, внизу живота. В этих отделах и появляется симптом Щеткина—Блюмбер-га. Если перфорация сигмовидной кишки возникает на участке неполной деструкции кишечной стенки, то быстро развивается клиническая картина прободного перитонита, но с преимущественной локализацией внизу живота. В тех случаях, когда деструкция происходит на значительном протяжении и перфорация возникает на значительном участке разрушенной кишечной стенки, перитонит клинически развивается более медленно, так как появляется отграниченный процесс. Перитонеаль-ные симптомы могут быть стертыми и маловыраженными. В начале заболевания у целого ряда больных определяется нормальная или даже усиленная перистальтика. Однако скоро она ослабевает (в стадии ишемии и инфаркта). Характерным признаком считается полное отсутствие аускультативных шумов в животе вследствие паралича и гангрены кишечника. На фоне "полной тишины" слышны сердечные тоны и систолический шум с аортобедрен-ного протеза. Наличие же перистальтических шумов свидетельствует о том, что кишечник остается пока еще жизнеспособным. Из лабораторных методов диагностики следует отметить лейкоцитоз, который при остром нарушении кровообращения в бассейне толстой кишки достигает чрезвычайно высоких цифр (до 50 000 ЕД/мм3), не встречающийся ни при каком другом заболевании органов брюшной полости. Сдвиг лейкоцитарной формулы влево до палочкоядерных и юных ней-трофилов отмечается уже в стадии ишемии, но наиболее выражен в стадиях инфаркта и перитонита. Возникающий после аортальных реконструкций необъяснимый метаболический ацидоз, развивающаяся гипотензия, отсутствие сепсиса или тяжелой гиповолемии не специфич- ны, но должны насторожить хирурга на возможность развития инфаркта толстой кишки. Развивающаяся тяжелая тромбо-цитопения (менее 90 • 109/л) расценивается как специфический маркер кишечного некроза и в сочетании с другими симптомами должна усилить подозрение на возможность возникновения данного осложнения. Рентгенологические признаки кишечного инфаркта можно выявить у большинства больных, если исследование производится через достаточно большой срок с момента начала ишемии. Однако вывод о том, что у всех больных рентгенологические признаки острого нарушения мезен-териального кровообращения появляются в поздние сроки с момента заболевания, был бы не совсем правильным. У ряда пациентов с быстро прогрессирующим течением рентгенологические признаки инфаркта толстой кишки могут обнаруживаться и в более ранние сроки (от 5 до 12ч). Из эндоскопических методов исследований наиболее эффективной является колоноскопия. Повторные исследования, проводимые в течение нескольких дней, как правило, подтверждают прогрессирование ишеми-ческого колита. Для выявления патологических изменений обычно достаточно продвижения колоноскопа не далее 40 см, что позволяет идентифицировать ишемические поражения более чем у 95 % пациентов. Ишемия вышележащих сегментов толстой кишки без вовлечения левой половины встречается редко. Если толстокишечная ишемия диагностирована, то колоноскопическое исследование следует прекратить. Продвижение колоноскопа за вовлеченный сегмент толстой кишки опасно развитием его перфорации. Важно и то обстоятельство, что колоноскопическое исследование возможно проводить непосредственно у постели пациента и отпадает необходимость транспортировать больного в специализированное отделение. 6 - 4886 Ранние изменения толстой кишки, выявляемые с помощью коло-носкопии, включают в себя наличие циркуляторных петехиальных геморрагии и отека. Появление псевдомембран, эрозий и язвенных дефектов подтверждает прогрессирование ишемического процесса. Выявление же желто-зеленых некротических участков, а также резко атонических участков кишки подтверждает развитие гангрены кишки. Имеются сообщения, что лапароскопия может оказать помощь в выявлении небольших по объему участков ишемии толстой кишки. Диагностическая ценность лапароскопии снижается, когда оценивается степень ишемии распространенных сегментов кишечника. Прогрессирование же ишемического колита, подтвержденное ухудшением общего статуса пациентов, появлением интоксикации и лихорадки, повышением лейкоцитоза, возникновением тромбоцитопении и диареи с примесью крови, а также симптомов раздражения брюшины, указывает на необходимость немедленного выполнения релапаротомии. В тех же случаях, когда под влиянием проводимой терапии наблюдается объективное улучшение общего состояния пациента, перитонеальные симптомы отсутствуют, уменьшается или ичезает диарея, улучшаются лабораторные параметры, а проводимая повторная колоноскопия указывает на регресс ишемических нарушений, допускается проведение консервативного лечения. Помимо коррекции водно-электролитных нарушений, поддержания адекватной гемодинамики и проведения мощного дезин-токсикационного лечения, целесообразны декомпрессия кишечника путем назогастральной интубации и введение мощных антибиотиков широкого спектра действия. Обычно обратимые ишемические нарушения разрешаются в течение 7—10 дней, что указывает на восстановление компенсаторных возмож- ностей коллатерального кровообращения. Профилактика развития острых нарушений мезентериального кровообращения после реконструкции брюшной аорты. При выполнении аортобед-ренных реконструкций необходимо учитывать имеющийся объем поражения висцеральных артерий. В клинике А.В. Покровского с 1982 г. объем поражения висцеральных ветвей брюшной аорты первоначально оценивается с помощью комплекса ультразвуковых методов диагностики ("В"-сканирование торако-абдоминальной аорты, цветовое доп-плеровское сканирование), которые позволяют неинвазивно документировать поражение указанных артерий, а в трудных для диагностики ситуациях способствуют установлению генеза, окклюзирующего поражения. При дуплексном исследовании висцеральных артерий хорошо визуализируется чревная и верхняя брыжеечная артерии. Нижняя брыжеечная артерия ввиду небольшого ее диаметра при ультразвуковом исследовании не видна. При сужении просвета устий и стволов чревной и верхней брыжеечной артерий более чем на 60 % (ге-модинамически значимый стеноз), наблюдается увеличение линейной скорости кровотока с локальными изменениями его спектра, свидетельствующие о турбулентном характере кровотока. Существенным преимуществом метода дуплексного сканирования по сравнению с рентгеноконтрастной ангиографией является возможность визуализировать атеросклеротичес-кую бляшку, определять ее размеры, протяженность и структуру, наличие изъязвлений на ее поверхности, что принципиально важно в плане развития, в частности, эмболических осложнений. К преимуществам метода следует отнести также возможность проведения его в динамике. Как уже подчеркивалось выше, по данным А.В. Покровского и соавт. (1979), межбрыжеечный анастомоз был не развит в 14,4 % наблюдений. Приблизительно аналогичные сведения приводят и другие авторы [Ernst et al., 1978; Crawford et al., 1981]. Таким образом, хорошее развитие межбрыжеечного анастомоза наблюдается далеко не всегда, а следовательно, и не во всех случаях при лиги-ровании нижней брыжеечной артерии гарантирован адекватный кровоток в бассейне ее кровоснабжения, что оправдывает активную хирургическую тактику в отношении этой артерии при аортобедренных реконструкциях. При анализе серийных ангиограмм необходимо обращать внимание на состояние внутренних подвздошных артерий. В тех случаях, когда нижняя брыжеечная артерия лигирована или из-за пролонгированного ее поражения восстановление по ней кровотока технически невозможно, внутренние подвздошные артерии берут на себя важную роль в кровоснабжении прямой и сигмовидной кишки. Сегодня большинство авторов [Покровский А.В. и др., 1979; Crawford et al, 1981; Ernst et al., 1986] являются принципиальными сторонниками восстановления кровотока по нижней брыжеечной артерии при аортобедренных реконструкциях, когда для этого имеются соответствующие условия. Как показывает практика, причиной развития ишемического колита после резекции аневризмы брюшной аорты в большинстве случаев является перевязка нижней брыжеечной артерии. Неправильное ее лигирова-ние (на протяжении) разрывает коллатеральные связи между левой ободочной артерией и сигмоидальными артериями. Для того чтобы сохранить эти ветви, нижняя брыжеечная артерия должна быть пересечена и перевязана у основания или прошита изнутри аневризмы после вскрытия последней. Во время вскрытия аневризмати-ческого мешка и удаления тромботи-ческой чаши следует опасаться эмбо- лии фрагментами тромба в нижнюю брыжеечную артерию. Поэтому перед вскрытием аневризмы целесообразно наложить клипсу на артерию. Чрезмерная тракция крючками может вызвать сдавление левой ободочной артерии и артерий брыжейки сигмовидной кишки. При разрыве аневризмы аорты коллатеральные сосуды могут быть сдавлены образовавшейся обширной гематомой. При интраоперационной оценке следует в первую очередь определить состояние нижней брыжеечной артерии: окклюзирована она или нет. При проходимой артерии важно оценить наличие ретроградного кровотока. При хорошем ретроградном кровотоке допустимо лигирование нижней брыжеечной артерии, при плохом — необходимо восстанавливать ее проходимость. Для оценки используются две методики жизнеспособности толстой кишки, позволяющие определить, допустимо ли лигирование нижней брыжеечной артерии или необходимо в обязательном порядке выполнять ее реконструкцию. Это, во-первых, ультразвуковая допплерография или дуплексное сканирование, определяющие кровоток по нижней брыжеечной артерии, дуге Риолана и на серозной поверхности толстой кишки до и после пережатия артерии (рис. 6.18). Вторая методика состоит в прямом определении артериального давления в нижней брыжеечной артерии. Привлекают внимание еще два других метода контроля за адекватностью кровообращения в толстой кишке. Первый включает в себя непрямое определение интрамурального рН с помощью силиконового тонометра, введенного в просвет кишки. В случае, когда наблюдается падение интрамурального рН ниже 6,86, то можно заподозрить развитие толстокишечной ишемии [Ernst, 1983]. Информативность этой методики была доказана и другими авторами на большом
б*
Рис. 6.18. Определение кровотока по дуге Риола-на во время пережатия нижней брыжеечной артерии при помощи ультразвуковой допплерогра-фии. ВБА — верхняя брыжеечная артерия; НБА — нижняя брыжеечная артерия. количестве пациентов. При этом во время пережатия аорты возникало падение уровня рН, однако в нео-сложненных ситуациях после восстановления аортального кровотока показатели рН возвращались к нормальным значениям через 4—6 ч. Измерение интрамурального рН в сигмовидной кишке привлекает внимание исследователей еще и потому, что оно применимо в случаях как ок-клюзирующих поражений аорты, так и при ее аневризмах. Более того, мо-ниторирование за уровнем интрамурального рН возможно при необходимости продолжить в реанимационном отделении. Hobson и соавт. (1979), использовав метод ультразвуковой допплеро-графии, считают, что адекватный кровоток по дуге Риолана при окклюзии нижней брыжеечной артерии свидетельствует о хороших компенсаторных возможностях висцерального кровообращения. В то же время выявление коллатерального кровотока или его отсутствие свидетельствует о реальном развитии толстокишечной ишемии в послеоперационном периоде, что диктует необходимость выполнения реконструкции нижней брыжеечной артерии. Такого же мнения придерживаются и А.В. Покровский и соавт. (1993). В случаях, когда артериальное давление в устье нижней брыжеечной артерии выше 40 мм рт.ст., допустимо ее дотирование, даже если пульсация внутренних подвздошных артерий не определяется. Артериальное давление ниже 40 мм рт.ст. должно настораживать хирурга в плане развития в послеоперационном периоде ишемического колита. Следует, однако, подчеркнуть, что полагаться на результаты измерения артериального давления в нижней брыжеечной артерии можно лишь в том случае, если уровень интра-и послеоперационного артериального давления не ниже артериального давления на момент измерения его в нижней брыжеечной артерии. Методы реконструкции висцеральных артерий. Развитие острого нарушения мезентериального кровооб-
Рис. 6.19. Трансаортальная эндартерэктомия из нижней брыжеечной артерии через аортотомичес-кий разрез, выполненный при наложении проксимального анастомоза при бифуркационном аорто-бедренном шунтировании. ращения в бассейне толстой кишки реально у больных, имеющих объективные предрасполагающие факторы, а также у пациентов без таковых, так как не во всех случаях имеется реальная возможность комплексной оценки функционального состояния висцерального кровообращения. В связи с этим реконструкция нижней брыжеечной артерии должна проводиться во всех случаях, когда для этого имеются соответствующие условия. В первую очередь это продиктовано тем, что как при резекции аневризмы брюшной аорты, так и при аортобедренных реконструкциях, выполненных по поводу окклю-зирующих поражений аорты, указанная артерия находится в зоне оперативного вмешательства, выполняемого по поводу патологии аорты. При стенозирующих поражениях аорты восстановление кровотока по нижней брыжеечной артерии целесообразно выполнять методом трансаортальной эндартерэктомии через тот же аортотомический разрез, который был произведен для наложения проксимального анастомоза протеза с аортой (рис. 6.19). Однако трансаортальная эндартерэктомия возможна лишь в тех случаях, когда ок-клюзирующий процесс распространяется не дистальнее 1,5—2 см от устья артерии. В противном случае при выполнении эндартерэктомии возможны фрагментация атероскле- ротической бляшки и эмболия в дис-тальное сосудистое русло [Покровский А.В. и др., 1979, 1989; Спиридонов А.А. и Клионер Л.И., 1989]. При резекции аневризмы брюшной аорты, а также при средней и
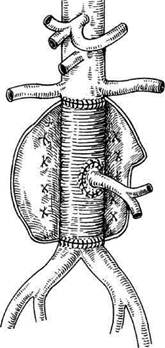
Рис. 6.20. Имплантация нижней брыжеечной артерии в протез на аортальной площадке при линейном протезировании аорты. высокой окклюзиях брюшной аорты выполняется резекция аорты (аневризмы) с аортобедренным аллопро-тезированием, а для восстановления кровотока по нижней брыжеечной артерии используется метод имплантации последней на аортальной площадке в основную браншу аллопроте-за, позволяющий облегчить наложение анастомоза с узкой по диаметру артерией и предупредить сужение ее просвета (рис. 6.20). Заключение. Профилактика развития острых циркуляторных расстройств мезентериального кровообращения значительно целесообразнее, нежели последующее лечение наступающих тяжелых осложнений после реконструкции аорты, связанных с развитием ишемии толстой кишки, которые сопровождаются крайне высокой летальностью. Во избежание возникновения этих грозных осложнений необходимы выявление пациентов с высоким риском их возникновения, тщательное соблюдение всех деталей оперативной техники, учитывающие особенности кровоснабжения кишечника в условиях поражения висцеральных артерий, использование доступных и информативных методов контроля за адекватностью висцерального кровообращения, а также при показаниях для выполнения реконструкции висцеральных артерий (наиболее часто нижней брыжеечной артерии). Литература Аничков М.Н., Лев ИД. Атлас патологии аорты. — Л.: Медицина, 1967. Покровский А.В., Казанчян П.О., Дюжи-ков А.А. Диагностика и лечение хронической ишемии органов пищеварения. — Изд-во Ростовского университета, 1982. Покровский А.В., Казанчян П. О., Юдин В.И. Показания к реваскуляризации висцеральных ветвей при аортобедренных реконструкциях // Хирургия. — 1989. — № 3. — С. 11-17. Поташов Л.В., Князев МД., Ненашев A.M. Ишемическая болезнь органов пищеварения. — Л.: Медицина, 1985. Савельев B.C., Спиридонов И.В. Острые нарушения мезентериального кровообращения. — М.: Медицина, 1979. Савельев B.C. и др. Особенности висцерального кровообращения при хронической ишемической болезни органов пищеварения и дислипопротеидемии // Грудная и сердечно-сосудистая хирургия. — 1999. — № 4. - С. 40-45. Шалимов А.А., Дрюк Н.Ф. Хирургия аорты и магистральных артерий. — Киев: Здоровье, 1979. 6.6. Почечные осложнения при реконструкции брюшной аорты Дата добавления: 2015-02-06 | Просмотры: 1144 | Нарушение авторских прав |