|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Опухоли пищевода7.9.1. Доброкачественные опухоли и кисты Доброкачественные опухоли и кисты пищевода наблюдаются редко. Патологоанатомическая картина. Опухоли по отношению к стенке пищевода могут быть внутрипросветными (полипообразными) и внутристе-ночными (интрамуральными). Внутрипросветные опухоли располагаются чаще в проксимальном или дистальном отделе пищевода, внутристеночные — в нижних двух третях его. По гистологическому строению опухоли делят на эпителиальные (адено-матозные полипы, папилломы) и неэпителиальные (лейомиомы, рабдомио-мы, фибромы, липомы, гемангиомы, невриномы, хондромы, миксомы и др.). Наиболее часто встречается лейомиома, развивающаяся из гладких мышечных волокон. Второе по частоте место занимают кисты (ретенцион-ные, бронхогенные, энтерогенные). Кисты представляют собой тонкостенные образования, содержащие светлую тягучую жидкость. Стенка кисты состоит из фиброзной ткани с примесью гладких мышечных волокон и хряща. Внутренняя поверхность стенки выстлана мерцательным эпителием при бронхогенной кисте и цилиндрическим или плоскоклеточным — при энте-рогенной. Ретенционные кисты располагаются в подслизистой основе пищевода и образуются в результате закупорки протоков желез. Они никогда не достигают больших размеров. Клиническая картина и диагностика. Доброкачественные опухоли и кисты пищевода растут медленно, не вызывают клинических симптомов и обнаруживаются случайно при рентгенологическом исследовании. Наиболее частым симптомом является медленно нарастающая на протяжении многих лет дисфагия.
Рис. 7.7. Доброкачественные опухоли пищевода. Рентгенограмма. При интрамуральных опухолях, циркулярно охватывающих пищевод, дисфагия может носить постоянный характер, иногда больные отмечают боли, ощущение давления или переполнения за грудиной. При опухолях шейного отдела пищевода, имеющих длинную ножку, может возникать регур-гитация опухоли в глотку с развитием асфиксии. При изъязвлении полипа или повреждении слизистой оболочки пищевода, растянутой над большой интрамуральной опухолью, возможно изъязвление и кровотечение, кисты пищевода нагнаиваются. Вследствие сдавления опухолью трахеи, бронхов, сердца, блуждающих нервов могут возникать кашель, одышка, цианоз, сердцебиение, боли в области сердца, аритмия и другие расстройства. Возможно злокачественное перерождение доброкачественных опухолей и кист пищевода. Диагноз доброкачественной опухоли пищевода ставят на основании анализа клинической картины заболевания, данных рентгенологического исследования и эзофагоскопии. Для доброкачественных опухолей пищевода характерны следующие рентгенологические признаки (рис. 7.7): четкие ровные контуры дефекта наполнения, располагающегося на одной из стенок пищевода, сохранность рельефа слизистой оболочки и эластичности стенок в области дефекта, четкий угол между стенкой пищевода и краем опухоли. Всем больным с доброкачественными заболеваниями пищевода показана эзофагоскопия для уточнения характера образования, его локализации и протяженности, состояния слизистой оболочки. Биопсию можно производить только при деструкции слизистой оболочки и при внутрипросветных новообразованиях. Лечение. Основным методом лечения доброкачественных опухолей является хирургический. Цель операции — удаление опухоли, профилактика возможных осложнений. Опухоли небольших размеров на тонкой ножке могут быть удалены через эзофагоскоп с помощью специальных инструментов или разрушены (электрокоагуляция). Внутрипросветные опухоли на широком основании иссекают с участком стенки пищевода. Интрамураль-ные опухоли и кисты пищевода почти всегда удается энуклеировать без повреждения слизистой оболочки. Отдаленные результаты операций хорошие. 7.9.2. Злокачественные опухоли 7.9.2.1. Рак Рак составляет 60—80 % всех заболеваний пищевода. На долю других злокачественных его поражений (саркома, меланома, злокачественная нев-ринома и др.) приходится около 1 %. Среди всех злокачественных заболеваний рак пищевода в нашей стране — шестое по частоте заболевание, встречающееся в большинстве случаев у мужчин в возрасте 50—60 лет. Смертность от рака пищевода составляет 6,4 на 100 000 жителей. Заболеваемость раком пищевода неодинакова в разных районах мира, что объясняется своеобразием питания населения (состав пищи, различные приправы к ней, особенности приготовления), геолого-минералогическими особенностями почвы и воды. Этиология и патогенез. В развитии рака большую роль играет хроническое воспаление слизистой оболочки пищевода вследствие механического, термического или химического раздражения. Риск развития рака существенно увеличивают курение (в 2—4 раза), злоупотребление алкоголем (в 12 раз), ахалазия, пищевод Баррета, папилломы и рубцовые изменения в пищеводе после ожога едкими веществами. Предраковым заболеванием считают синдром Пламмера—Винсона (си-деропенический синдром), который развивается преимущественно у женщин старше 40 лет, страдающих железодефицитной анемией. Возникает атрофия слизистых оболочек ротовой полости, глоссит, ногти становятся ломкими, ложкообразными. Причиной дисфагии обычно является перемычка в шейном отделе пищевода, хотя нельзя исключить нарушение сократительной способности мышц. Для лечения применяют дилатацию пищевода бужами и коррекцию питания с учетом выявленных дефицитов. Патологоанатомическая картина. Рак пищевода развивается чаще в местах физиологических сужений: устье пищевода, на уровне бифуркации трахеи, над нижним пищеводным сфинктером. Рак поражает среднегрудной отдел (60 %), затем — нижнегрудной и абдоминальный отделы пищевода (30 %), шейный и верхнегрудной (10 %). Различают три основные формы рака пищевода: экзофитный (узловой, грибовидный, папилломатозный); эндофитный (язвенный); инфильтратив-ный склерозирующий (циркулярная форма). Бывают смешанные формы роста. Узловые формы составляют около 60 %, имеют экзофитный рост, представлены разрастаниями, похожими на цветную капусту. Опухоль легко травмируется, распадается и кровоточит. При распаде и изъязвлении узлов макроскопическая картина мало отличается от картины язвенного рака. Язвенные (эндофитные) формы рака пищевода в начальной стадии представляют узелки в толще слизистой оболочки, быстро изъязвляющиеся. Опухоль растет преимущественно вдоль пищевода, поражая все слои его стенки и распространяясь на окружающие органы и ткани, рано метастази-руя в регионарные и отдаленные лимфатические узлы. Местному распространению рака благоприятствует отсутствие у пищевода серозной оболочки. В стенке пищевода на протяжении 5—6 см от края опухоли часто развивается раковый лимфангит. Инфильтративные (склерозирующие) формы рака пищевода составляют около 10—-15 %. Опухоль развивается в глубоких слоях слизистой оболочки, быстро поражает подслизистую основу и распространяется по окружности пищевода. Разрастаясь, она захватывает все слои стенки пищевода, обтури-рует его просвет. В дальнейшем опухоль изъязвляется, возникает перифо-кальное воспаление. Супрастенотическое расширение пищевода при раке редко бывает значительным, так как опухоль развивается в сравнительно короткий период времени. Распространение рака пищевода происходит путем непосредственного прорастания в окружающие ткани лимфогенного и гематогенного метаста-зирования. Сравнительно поздним осложнением является прорастание опухоли в соседние органы с образованием свища между пищеводом и трахеей или бронхом, развитием нагноительных процессов в легких и плевре. При прорастании опухоли в аорту может возникать смертельное кровотечение. Диссеминация раковых клеток по лимфатическим сосудам в стенке пищевода может распространяться на 10—15 см от видимой границы опухоли. В связи с этим при резекции пищевода ткань его по линии разреза должна подвергаться срочному гистологическому исследованию. Раковый лимфангит чаще встречается при локализации процесса в верхней и средней трети пищевода. Опухоли, расположенные в шейном и верхнегрудном отделах пищевода, метастазируют главным образом в медиастинальные, над- и подключичные лимфатические узлы. Рак нижней трети пищевода метастазирует в лимфатические узлы, расположенные вокруг пищевода и кардии, забрюшинные лимфатические узлы по ходу чревного ствола и его ветвей. При локализации опухоли в среднегрудном отделе пищевода метастазы распространяются в околотрахеальные, прикорневые и нижнепищеводные лимфатические узлы. Однако при раке среднегрудного отдела пищевода опухоль может метаста-зировать и в лимфатические узлы в области кардии, по ходу чревного ствола и его ветвей. Поэтому некоторые хирурги рекомендуют операцию при раке пищевода всегда начинать с лапаротомии и ревизии органов брюшной полости и забрюшинного пространства для того, чтобы произвести лимфаден-эктомию узлов вокруг чревного ствола и кардии, определить операбель-ность. Отдаленные метастазы чаще всего встречаются в печени, реже — в легких, костях и других органах. Гематогенное распространение рака происходит в поздней стадии заболевания, когда рак из местного заболевания превращается в системное. В подавляющем большинстве случаев рак пищевода бывает плоскоклеточным. Реже (8—10 %) встречаются аденокарциномы, преимущественно при пищеводе Баррета. Аденокарциномы растут также из эктопированной в пищевод слизистой оболочки желудка или из кардиальных желез, имеющихся в нижнем отделе пищевода. Изредка развивается коллоидный рак. Из других злокачественных опухолей пищевода следует отметить адено-акантому, состоящую из железистых и плоскоклеточных элементов, и кар-циносаркому (сочетание рака и саркомы). Международная классификация рака пищевода по системе TNM (1997 г.) Т — первичная опухоль Тх — недостаточно данных для оценки первичной опухоли. Т0 — первичная опухоль не определяется. Tis — преинвазивная карцинома (carcinoma in situ). T1 — опухоль инфильтрирует стенку пищевода до подслизистой основы. Т2 — опухоль инфильтрирует стенку пищевода до мышечного слоя. ТЗ — опухоль инфильтрирует стенку пищевода до адвентиции. Т4 — опухоль распространяется на соседние структуры. N — регионарные лимфатические узлы Nx — недостаточно данных для оценки регионарных лимфатических узлов.
N1 — имеется поражение регионарных лимфатических узлов метастазами. М — отдаленные метастазы Мх — недостаточно данных для определения отдаленных метастазов. М0 — нет признаков отдаленных метастазов. Ml — имеются отдаленные метастазы. Категории Ml и рМ1 могут быть дополнены в зависимости от локализации метастазов в тех или других органах следующими символами: легкие PUL, костный мозг MAR, кости OSS, плевра PLE, печень HEP, брюшина PER, головной мозг BRA, кожа SKI, лимфатические узлы LYM другие отн. G — гистопатологическая дифференцировка Gx — степень дифференцировки не может быть установлена. G1 — высокая степень дифференцировки. G2 — средняя степень дифференцировки. G3 — низкая степень дифференцировки. G4 — недифференцированные опухоли. В клинической практике иногда удобнее пользоваться делением рака по стадиям по клинико-морфологическим признакам, которые легко можно выразить и по системе TNM. Стадии рака I — четко отграниченная небольшая опухоль, прорастающая только сли II — опухоль, прорастающая мышечную оболочку, но не выходящая за III — опухоль, циркулярно поражающая пищевод, прорастающая всю его IV— опухоль прорастает все оболочки стенки пищевода, выходит за пре Клиническая картина и диагностика. Основными симптомами рака пищевода являются: ощущение дискомфорта за грудиной при проглатывании пищи, дисфагия, боль за грудиной, гиперсаливация, похудание. Начало заболевания бессимптомное (доклиническая фаза). Этот период может длиться 1—2 года. Когда опухоль достигает значительных размеров и начинает суживать пищевод, появляются первые признаки нарушения пассажа пищи, перерастающие в выраженную дисфагию. Дисфагия встречается у 70—85 % больных и по существу является поздним симптомом, возникающим при сужении просвета пищевода опухолью на 2/3 и более. Для рака характерно прогрессирующее нарастание дисфагии. Нарушение проходимости пищевода связано не только с сужением его просвета опухолью, но и с развитием перифокального воспаления, спазмом пищевода. В начальном периоде заболевания дисфагия возникает при проглатывании плотной или недостаточно пережеванной пищи. Больные ощущают как бы прилипание ее к стенке пищевода или временную задержку на определенном уровне. Глоток воды обычно устраняет эти явления. В дальнейшем перестает проходить даже хорошо прожеванная пища, в связи с чем больные вынуждены принимать полужидкую и жидкую пищу. Иногда после стойкого периода дисфагии возникает улучшение проходимости пищевода, связанное с распадом опухоли. Возникновению дисфагии могут предшествовать ощущения инородного тела в пищеводе, чувство царапанья за грудиной, болезненность на уровне поражения, появляющиеся при проглатывании твердой пищи. Боль отмечается у 33 % больных. Обычно она появляется за грудиной во время приема пищи. Постоянная боль, не зависящая от приема пищи или усиливающаяся после еды, обусловлена прорастанием опухоли в окружающие пищевод ткани и органы, сдавлением блуждающих и симпатических нервов, развитием периэзофагита и медиастинита. Причиной боли могут быть метастазы в позвоночник. Срыгивание пищей и пищеводная рвота (23 % больных) появляются при значительном стенозировании просвета пищевода и скоплении пищи над местом сужения. При раке пищевода, как и при стенозах другой этиологии, развивается усиленное слюнотечение. Обильные кровотечения из пищевода в связи с распадом опухоли бывают редко — при разрушении опухолью стенки крупного сосуда. Общие проявления заболевания (слабость, прогрессирующее похудание, анемия) бывают следствием голодания и интоксикации. При прорастании опухолью возвратных нервов развивается охриплость голоса. Поражение узлов симпатического нерва проявляется синдромом Бернара—Горнера. При прорастании опухоли в трахею и бронхи возникают пищеводно-трахеальный или бронхопищеводный свищи, проявляющиеся кашлем при приеме жидкости, аспирационной пневмонией, абсцессом или гангреной легкого. Вследствие перехода инфекционного процесса с пищевода на окружающие ткани могут развиться периэзофагит, медиастинит, перикардит. Клиническое течение болезни зависит от уровня поражения пищевода. Рак верхнегрудного и шейного отделов пищевода протекает особенно мучительно. Больные жалуются на ощущение инородного тела, царапанье, жжение в пищеводе во время еды. Позднее появляются симптомы глоточной недостаточности — частые срыгивания, поперхивание, дисфагия, приступы асфиксии. При раке среднегрудного отдела на первый план выступают дисфагия, боли за грудиной. Затем появляются симптомы прорастания опухоли в соседние органы и ткани (трахея, бронхи, блуждающий и симпатический нервы, позвоночник и др.). Рак нижнегрудного отдела проявляется дисфагией, болью в эпигастральной области, иррадиирующей в левую половину грудной клетки и симулирующей стенокардию. Важнейшими методами диагностики являются рентгенологическое исследование, эзофагоскопия с биопсией опухоли. В последнее десятилетие появилась возможность эндоскопического ультразвукового исследования, позволяющего определить глубину поражения стенки пищевода и метастазы в лимфатические узлы средостения.
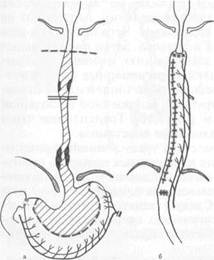
Рентгенологическое исследование с контрастированием пищевода взвесью бария выявляет опухоль, ее локализацию, длину поражения и степень сужения пищевода, изменения в легких и плевральных полостях. Характерные симптомы рака — дефект наполнения, "изъеденные" контуры его, сужение просвета, ригидность стенок пищевода, обрыв складок слизистой оболочки вблизи опухоли, престено-тическое расширение пищевода (рис, 7.8). Для определения границ распространения опухоли на соседние органы применяют компьютерную томографию.
Отсутствие рентгенологических данных при наличии дисфагии или боли при прохождении пищи не позволяет исключить рак пищевода. Диагноз уточняют с помощью эндоскопического исследования с прицельной биопсией и последующим морфологическим исследованием полученного материала. Очень ценную информацию при раннем раке может дать эндоскопическое ультразвуковое исследование, позволяющее не только выявить опухоль, но и определить глубину проникновения ее в стенку пищевода. Эзофагоскопия показана во всех случаях при подозрении на рак пищевода. Начальные формы рака могут выглядеть как плотный белесоватый бугорок или полип. При инфильтративной форме рака отмечают ригидность стенки пищевода, выявляемую при надавливании на нее концом эзофагоскопа. При экзофитных опухолях значительных размеров видна бугристая масса, покрытая сероватым налетом. Поверхность опухоли легко кровоточит при прикосновении. Опухоль вызывает концентрическое или одностороннее сужение просвета пищевода. Биопсия легко осуществима при экзофитных опухолях, труднее получить участок ткани для исследования при язвенном и инфильтративном раке. В сомнительных случаях биопсию следует повторить. Цитологическое исследование в сочетании с биопсией в большинстве случаев позволяет подтвердить или отвергнуть диагноз рака. Дифференциальная диагностика. При раке пищевода следует исключить другие заболевания, сопровождающиеся дисфагией: ахалазию, рубцовые сужения после химических ожогов, доброкачественные стенозы у больных с пептическим эзофагитом, доброкачественные опухоли, туберкулез и др. Следует исключить также оттеснение пищевода извне опухолями заднего средостения, внутригрудным зобом, аневризмой аорты, увеличенными лимфатическими узлами, заполненным большим дивертикулом. Рентгенологическим признаком сдавления пищевода является его смещение. Даже значительное увеличение соседних органов длительное время не вызывает дисфагии, так как смещаемость пищевода достаточно велика. Сдавление и нарушение проходимости пищевода могут быть обусловлены фиброзным медиастинитом (рубцовым изменением клетчатки средостения), возникающим после воспалительных заболеваний легких и лимфатических узлов средостения. Эндоскопическое исследование в сочетании с биопсией из разных мест опухоли повышает точность диагностики до 90 %. Таким образом, план исследования больного при раке пищевода должен включать рентгенологическое исследование с контрастированием пищевода, эзофагоскопию с множественной биопсией, эндоскопическое УЗИ при возможности провести инструмент через суженный участок пищевода, компьютерную томографию легких, средостения и печени, ультразвуковое исследование печени, по показаниям — медиастино- и бронхоскопию. Лечение. Хирургическое удаление пораженного пищевода является наиболее радикальным из имеющихся методов лечения рака. Показания к операции зависят от распространенности и локализации опухоли, возраста и общего состояния пациента. Операция противопоказана при отдаленных метастазах, парезе возвратных нервов, прорастании опухоли в трахею или бронхи, тяжелом общем состоянии больного. Объем хирургического вмешательства — радикальные и паллиативные операции — может быть точно определен только во время операции. Радикальная операция предусматривает удаление пищевода с одномоментным пластическим замещением его трубкой, выкроенной из большой кривизны мобилизованного желудка, или толстой кишкой. Паллиативные оперативные вмешательства предпринимают для устранения дисфагии без удаления опухоли. При локализации рака в абдоминальном и нижнегрудном отделах производят одномоментное оперативное вмешательство из левостороннего торакоабдоминального доступа. Он дает возможность удаления пищевода, регионарных лимфатических узлов и мобилизации желудка. После удаления опухоли призводят пластику пищевода желудком, который перемещают в плевральную полость и соединяют пищеводно-желудочным анастомозом (рис. 7.9). При локализации рака в сред н е груд н ом отделе производят правосторонний торакоабдоминальный разрез или отдельно торакальный, затем абдоминальный разрезы. Этот оперативный доступ дает возможность мобилизовать пищевод вместе с окружающей клетчаткой и региональными лимфатическими узлами. Через абдоминальный разрез создается хороший доступ к желудку и абдоминальному отделу пищевода. Он позволяет мобилизовать желудок и удалить лимфатические узлы. После удаления пищевода производят одномоментную пластику его мобилизованным желудком с наложением пищеводно-желудочного анастомоза в плевральной полости (по Lewis) (рис. 7.10) Недостатком чресплевральных доступов является частота дыхательных осложнений и высокая летальность (15—30 %), опасность расхождения швов анастомоза в плевральной полости и рецидивов рака на уровне анастомоза, рефлюкс-эзофагит. В течение последних 20 лет предпочитают производить трансгиатальную резекцию пищевода из абдоминоцервикального доступа без торакотомии (рис. 7.11). Независимо от уровня поражения пищевод удаляют полностью. Для пластики пищевода используют трубку, выкроенную из большой кривизны мобилизованного желудка, или весь желудок, который выводится на шею через заднее средостение и соединяется анастомозом с оставшейся частью шейного отдела пищевода. Разрезы делают на шее, кпереди от m.ster-
Рис. 7.9. Одномоментная резекция нижней трети пищевода и кардии с эзофагопластикой. а — операционный доступ; б — уровень резекции пищевода и желудка; в — наложение узофагогастроана-стомоза.
Рис. 7.10. Пластика пищевода изопери-стальтической желудочной трубкой. а — уровень резекции пищевода и выкраивание из желудка; б — завершение операции эзофагопластикой.
Рис. 7.11. Цервикально-абдоминальное удаление пищевода.
nocleidomastoideus, а на животе производят верхнюю срединную лапаро-томию. Желудок мобилизуют по обычной методике с перевязкой левой желудочной и желудочно-саль-никовой артерий и удалением лимфатических узлов в области чревного ствола и кардии. Во избежание спазма привратника производят пилоро-миотомию. Пищевод мобилизуют снизу через дифрагмальное отверстие и сверху — через разрез на шее, затем пересекают его в шейном отделе и низводят грудной отдел в брюшную полость. Выкроенную из большой кривизны желудка трубку или толстую кишку через заднее средостение перемешают на шею и накладывают пищеводно-желудочный (внеплев-ральный!) анастомоз. Более аккуратно грудной отдел пищевода может быть мобилизован с помощью видео-торакоскопической техники (рис. 7.12). Для этого в положении больного на животе в правую плевральную полость вводят несколько троакаров, через которые под визуальным мони-торным контролем с помощью специальных эндоскопических инструментов выделяют грудной отдел пищевода и видимые лимфатические узлы. Пищевод, так же как при трансгиатальном выделении, пересекают на границе с шейным отделом и низводят до диафрагмы. Через разрез на шее мобилизуют и выводят в рану шейный отдел пищевода. Затем поворачивают пациента на спину, производят срединную лапаротомию, мобилизуют абдоминальный отдел пищевода и желудка, удаляют регионарные лимфатические узлы. После удаления пищевода, низведенного до пищеводного отверстия диафрагмы, производят пластику его трубкой, выкроенной из большой кривизны желудка, или толстой кишкой (см. рис. 7.10). Трансплантат через заднее средостение выводят на шею для наложения анастомоза. При этом типе операции нет необходимости в травматичной торакото-мии, исключается опасность инфицирования плевральных полостей, уменьшается частота послеоперационных осложнений. Летальность при этой операции составляет 5 %. Пятилетняя выживаемость увеличивается в 2—3 раза и достигает у некоторых хирургов 27 %. Следует заметить, что выживаемость в значительной мере зависит от биологических свойств клеток опухоли, сопротивляемости организма, тщательности лимфаденэктомии, величины кровопотери во время операции. Двухэтапную операцию Добромыслова—Торека (рис. 7.13) раньше применяли для удаления рака среднегрудного отдела пищевода. Из правостороннего чресплеврального доступа удаляли грудной отдел пищевода. Через абдоминальный разрез накладывали гастростому. В последующем (спустя 3—6 мес) создавали искусственный пищевод из толстой или тонкой кишки.
Рис. 7.13. Многоэтапная операция Добромыслова—Торека и создание искусственного пишс-вода из толстой кишки. а — операционный доступ; б — уровень резекции пищевода; в — выкраивание трансплантата из толстой кишки; г — эзофагопластика. Трансплантат выводили на шею через подкожный тоннель или ретростер-нально и накладывали анастомоз с шейным отделом пищевода. В настоящее время эту операцию не применяют, потому что значительная часть больных погибала, не дождавшись второго этапа. Из числа обратившихся за хирургической помощью лишь 50—60 % подвергаются оперативному вмешательству и только у 30—40 % удается выполнить резекцию пищевода. Летальность после операций на пищеводе колеблется в пределах 3— 15 %. Наиболее частыми причинами смерти при трансторакальных доступах являются расхождение швов анастомоза (36 %), пневмония (37 %), кровотечение (9 %), сепсис (6 %) и другие причины (12 %). При удалении пищевода через абдоминоцервикальный доступ с внеплевральным анастомозом на шее послеоперационная летальность и частота осложнений существенно снизились, а пятилетняя выживаемость возросла. Результаты операций на пищеводе далеко не утешительные. Пятилетняя выживаемость в большинстве статистик и по результатам многоцентрового исследования не превышает 5—10 %. В среднем продолжительность жизни оперированных равна 16,4 мес. Выживаемость зависит от стадии рака. При II стадии она составляет 25 %, при III — только 6 %. Оперативное удаление опухоли нечасто дает излечение больных, но оно улучшает качество жизни оперированных, устраняет один из самых тягостных симптомов — дис-фагию. Разочарование в результатах хирургического лечения рака пищевода заставило искать комбинированные способы в надежде на улучшение выживаемости больных. Для этих целей используют различные комбинации хирургического лечения с лучевой и химиотерапией. В настоящее время применяют: 1) предоперационную лучевую терапию; 2) предоперационную и послеоперационную химиотерапию; 3) комбинацию предоперационной лучевой терапии с химиотерапией в надежде на разный механизм воздействия их на раковые клетки; 4) химиотерапию и лучевую терапию без хирургического вмешательства и 5) только лучевую терапию с использованием различных источников облучения, применяя соответствующие схемы и дозы. Предоперационное облучение проводят с целью уменьшения опухоли, повышения абластичности операции и подавления роста метастазов в регионарные лимфатические узлы. В известной мере у небольшого числа пациентов это удается. Примерно у 14 % опухоль исчезает, число лимфатических узлов с метастазами сокращается в 3—4 раза, однако, как показали результаты хорошо спланированных рандомизированных исследований, предоперационное облучение в дозе 4000—5000 кГр не улучшает пятилетнюю выживаемость по сравнению с оперативным лечением без предоперационного облучения. Химиотерапия. Для химиотерапии до операции и после нее используют цисплатин, блеомицин, виндезин, 5-фторурацил и другие препараты в различных сочетаниях. Рандомизированное изучение эффективности предоперационной и послеоперационной химиотерапии и сравнение с результатами только хирургического лечения рака пищевода показали, что предоперационная химиотерапия дала положительный результат у 47 %, позволила снизить частоту послеоперационных осложнений, однако не оказала никакого влияния на резектабельность. Пред- и послеоперационная химиотерапия не повлияла на пятилетнюю выживаемость больных. Указанные виды комбинированной терапии не имеют преимуществ перед чисто хирургическим методом лечения. При строгом отборе больных для комбинированной терапии и небольшом числе наблюдений некоторые
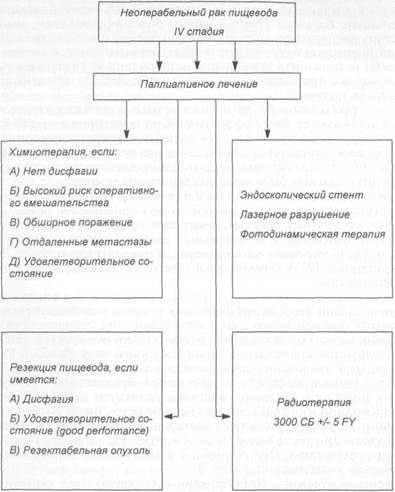
Предоперационная химиотерапия в сочетании с облучением не оказалась более эффективной по сравнению с только хирургическим методом лечения, хотя у 17 % больных к моменту операции опухоль исчезла, на короткий период уменьшалась или исчезала дисфагия. Резекта-бельность, послеоперационная летальность и пятилетняя выживаемость в обеих группах больных были практически одинаковыми. Химиотерапия в сочетании с облучением без хирургического вмешательства (см. схему) применяется редко, преимущественно для лечения больных, у которых хирургическое вмешательство невозможно. Более чем у 50 % больных удается получить положительный эффект, опухоль уменьшалась в размерах, в ряде случаев исчезала, пациенты по критериям TNM переходили в группу ТО. Некоторые из них могли быть оперированы. Лучевая терапия без хирургического вмешательства при первой стадии хорошо дифференцированного плоскоклеточного рака, при размерах опухоли менее 5 см и отсутствии циркулярного поражения у 80 % больных дает положительный результат. Опухоль уменьшается в размерах, улучшается прохождение пищи по пищеводу у 50—75 % больных. Однако по мере увеличения дозы радиации в процессе лечения у больных развивается лучевой эзофагит с последующим образованием стриктуры. Более чем у половины длительно живущих пациентов возникает необходимость в дилатации пищевода. Использование источников высоких энергий (тормозного излучения и быстрых электронов), обеспечивающих подведение к опухоли пищевода высокой дозы излучения, не дало существенного улучшения результатов. При облучении в дозе 4000—5000 кГр пятилетняя выживаемость колеблется от 3 до 9 %. Применение лучевой и химиотерапии как дополнение к хирургическому вмешательству оправдано, особенно при соответствующем отборе больных, так как к моменту выявления рака пищевода болезнь принимает системный характер, при котором локальное воздействие на опухоль становится малоэффективным. Хирургическое лечение остается наиболее эффективным методом улучшения качества жизни больных. К паллиативным операциям относят паллиативные резекции пищевода, обходное шунтирование, реканализацию опухоли (эндопротези-рование трубкой, реканализация лучом лазера, фотодинамической терапией, дилатацией), наложение гастростомы. Обходное шунтирование наложением анастомоза между пищеводом (выше опухоли) и выключенной по Ру петлей тощей кишки было предложено Киршнером для лечения неудалимых опухолей в 1885 г. Паллиативные резекции пищевода стали делать много позже. Обе операции избавляют больных от дисфагии, улучшают качество жизни, средняя продолжительность которой не превышает 3—4 мес. Недостатком этих операций является высокая летальность (свыше 30 %) и большое число легочных осложнений. Интубация (эндопротезирование, с тент) пищевода произ-
водится трубками различной конструкции (Целестин, Аткинсон, Вильсон-Кук и др.), которые проводят либо сверху с помощью эндоскопа, либо снизу через гастротомический разрез. Трубка Аткинсона имеет несомненное преимущество, потому что ее проводят с помощью эндоскопа после дилата-ции пищевода по проволочному проводнику. При этом отпадает необходимость в разрезе и общем обезболивании, уменьшается число осложнений и длительность пребывания больного в стационаре. Интубация пищевода необходима для больных с трахеопищеводным свищом для оттока слюны. Лазерная реканализация обтурированного опухолью пищевода проводится свободным пучком лучей либо специальным инструментом для подведения лазерного излучения наконечником из сапфира. Разрушение опухоли позволяет на 2—3 мес восстановить проходимость пищевода, избавить больного от дисфагии. Если необходимо, производится повторное вмешательство. При этой процедуре у ряда больных (до 10 %) наблюдалась перфорация пищевода. Фотодинамическая терапия — метод частичного разрушения опухоли, предварительно сенсибилизированной фотосенсибилизаторами лазерным лучом с длиной волны 630 нм. В качестве фотосенсибилизаторов используют дериваты гематопорфирина, аминолевуленовую кислоту, фотосенс и др. Фотосенсибилизаторы избирательно накапливаются в опухоли в большей концентрации, чем в здоровых тканях. Под влиянием облучения в опухоли образуются активные радикалы, разрушающие ткани опухоли на глубину проникновения лазерного луча (3—4 мм). Одновременно с этим тромбируются мелкие сосуды, питающие опухоль. Это приводит к частичному некрозу опухоли, улучшению проходимости пищевода. Частичное разрушение опухоли улучшает проходимость жидкой и мягкой пищи, уменьшает степень дисфагии. Осложнения бывают в виде отека слизистой оболочки пищевода на 2—3 дня, фотодерматита при воздействии прямых солнечных лучей. Значительно реже наблюдается плевральный выпот, образование пищеводно-трахеальной фистулы. Дилатация пищевода бужами позволяет на некоторое время полностью устранить дисфагию у 26 %. Проходимость пищевода частично улучшается у 42 % больных и остается без улучшения у 32 %. Паллиативное и симптоматическое лечение показано больным с неоперабельным раком пищевода. Результаты паллиативного лечения плохие потому, что временное улучшение проходимости никак не влияет на распространение и рост опухоли и исходы лечения. 7.9.2.2. Саркома Саркома — злокачественная неэпителиальная опухоль. Составляет 1 — 1,5 % всех злокачественных опухолей пищевода, чаще встречается у мужчин (75 %). Патологоанатомическая картина. Саркомы пищевода очень разнообразны по гистологическому строению. Они могут развиваться из мышечной ткани (лейомиосаркома, рабдомиосаркома), из соединительной ткани (фибросаркома, хондросаркома, липосаркома, остеосаркома, миксосарко-ма), из сосудов (ангиосаркома). Встречается опухолевый ретикулез пищевода (лимфосаркома, ретикулосаркома). Из злокачественных неэпителиальных опухолей наиболее часто в пищеводе развивается лейомиосаркома, локализующаяся в основном в средней и нижней третях его. Саркомы могут располагаться интрамурально и расти за пределы стенки пищевода, инфильтрируя клетчатку средостения и прилежащие органы. Метастазируют саркомы пищевода реже, чем раковые опухоли. Клиническая картина и диагностика. Основным симптомом заболевания является дисфагия. Боли за грудиной, в подложечной области появляются в далеко зашедшей стадии. Другими проявлениями заболевания бывают слабость, прогрессирующая потеря массы тела, анемия. При распаде опухоли, прорастающей вдыхательные пути, образуется пищеводно-трахеальный или бронхопищеводный свищ. Диагноз саркомы пищевода ставят на основании анализа клинической картины, данных рентгенологического исследования и эзофагоскопии с биопсией. Лечение. Принципы хирургического лечения при саркоме такие же, как и при раке пищевода. Некоторые виды сарком хорошо поддаются лучевой терапии. В запущенных случаях заболевания проводят симптоматическую терапию. Глава 8. ДИАФРАГМА
Диафрагма — сухожильно-мышечная перегородка, разделяющая грудную и брюшную полости. Она имеет вид двух сухожильных куполов с вдавлением между ними. Мышечная часть расположена по периферии. В ней различают грудинный, реберный и поясничные отделы. Между грудинным и реберным отделами имеется грудинореберное пространство (треугольники Морганьи, Ларрея), заполненное клетчаткой. Поясничный и реберный отделы разделены пояснично-реберным пространством (треугольник Бохдалека). Поясничный отдел диафрагмы образован с каждой стороны тремя связками (ножками): наружной (латеральной), промежуточной и внутренней (медиальной). Сухожильные края обеих внутренних ножек диафрагмы создают на уровне 1 поясничного позвонка, слева от срединной линии, дугу, ограничивающую отверстие для аорты и грудного протока. Пищеводное отверстие диафрагмы образовано в большинстве случаев за счет правой внутренней ножки диафрагмы, реже — за счет левой ножки (10 % случаев). Через пищеводное отверстие диафрагмы проходят также блуждающие нервы. Через межмышечные шели поясничного отдела диафрагмы проходят симпатические стволы, внутренностные нервы, непарная и полунепарная вены. Отверстие для нижней полой вены расположено в сухожильном центре диафрагмы (рис. 8.1). Сверху диафрагма покрыта внутригрудной фасцией, плеврой, а в центральной части — перикардом, снизу — внутрибрюшной фасцией и брюшиной. К забрюшинной части диафрагмы прилежат поджелудочная железа, двенадцатиперстная кишка, окруженные жировой капсулой почки и надпочечники. К правому куполу диафрагмы прилежит печень, к левому — селезенка, дно желудка, левая доля печени. Между этими органами и диафрагмой имеются соответствующие связки. Правый купол диафрагмы расположен выше (четвертое межреберье), чем левый (пятое межреберье). Высота стояния диафрагмы зависит от конституции, возраста, наличия патологических процессов в грудной и брюшной полостях. Кровоснабжение осуществляют верхняя и нижняя диафрагмальные артерии, отходящие от аорты, мышечно-диафрагмальная и иерикардодиафрагмальная артерии, отходящие от внутренней грудной, а также шесть нижних межреберных артерий. Отток венозной крови происходит по одноименным венам, непарной и полунепарной венам, а также венам пищевода. Лимфоотток происходит по лимфатическим сосудам, расположенным вдоль пищевода, аорты, нижней полой вены и другим сосудам и нервам, проходящим через диафрагму. Поэтому воспалительный процесс может распространиться по лимфатическим сосудам из брюшной полости в плевральную и наоборот. Лимфатические сосуды отводят лимфу сверху через ретроперикарди-альные и задние медиастинальные лимфатические узлы, снизу — через парааортальные и околопищеводные. Иннервация осуществляется диафрагмальными и межреберными нервами. Функции диафрагмы. Выделяют статическую и динамическую функции диафрагмы. Статическая состоит в поддержании разницы давления в грудной и брюшной полостях и нормальных взаимоотношений между их органами. Динамическая проявляется воздействием движущейся при дыхании диафрагмы на легкие, сердце и органы брюшной полости. Движения диафрагмы способствуют расправлению легких на вдохе, облегчают поступление венозной крови в правое предсердие, способствуют оттоку венозной крови от печени, селезенки и органов брюшной полости, движению газов в пищеварительном тракте, акту дефекации, лимфообращению. Дата добавления: 2015-01-18 | Просмотры: 1655 | Нарушение авторских прав |

 NO — нет признаков метастатического поражения регионарных лимфатических узлов.
NO — нет признаков метастатического поражения регионарных лимфатических узлов.







 авторы показали, что такой подход к лечению рака пищевода оправдан, так как комбинированная терапия рака позволяет угнетать рост раковых клеток за пределами локализации опухоли, повысить 2- и 5-летнюю выживаемость оперированных больных. Поиски новых, более эффективных химиотера-певтических препаратов и способов их применения продолжаются. Возможно, такие препараты будут найдены. В экспериментальных исследованиях изыскивают возможность применения методов генной инженерии для лечения рака, однако при клинических испытаниях эффекта от имеющихся методов пока не получено.
авторы показали, что такой подход к лечению рака пищевода оправдан, так как комбинированная терапия рака позволяет угнетать рост раковых клеток за пределами локализации опухоли, повысить 2- и 5-летнюю выживаемость оперированных больных. Поиски новых, более эффективных химиотера-певтических препаратов и способов их применения продолжаются. Возможно, такие препараты будут найдены. В экспериментальных исследованиях изыскивают возможность применения методов генной инженерии для лечения рака, однако при клинических испытаниях эффекта от имеющихся методов пока не получено.