 |
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Опухоли печени 5 страница
В моче отмечается резкое повышение реакции на уробилин и уробили-ноген. Билирубинурия имеет перемежающийся характер. При тяжелом поражении печеночной паренхимы билирубинурии нет. Функциональные пробы печени имеют важное дифференциально-диагностическое значение только на ранних стадиях развития желтухи. При обтурационной желтухе длительностью более 4 нед за счет вторичного повреждения гепатоцитов функциональные пробы изменяются так же, как и при печеночной желтухе. При обтурационной желтухе кожные покровы приобретают желтовато-зеленую окраску, а при обтурирующих желчевыводящие пути опухолях — характерный землистый оттенок. В случае длительного существования обтурационной желтухи кожные покровы становятся черновато-бронзовыми. При желчнокаменной болезни вначале возникают характерные приступообразные боли по типу печеночной колики, иногда желтуха появляется на фоне острого холецистита, при опухолях панкреатодуоденальной зоны без предшествующих болевых ощущений. Кожный зуд особенно выражен при желтухе, вызванной опухолью, при очень высоком уровне билирубине-мии. Печень в большинстве случаев не увеличена или увеличена незначительно. У половины больных с опухолями панкреатодуоденальной зоны выявляют положительный симптом Курвуазье. Селезенка при обтурационной желтухе не увеличена, не пальпируется, периферические лимфатические узлы также не увеличены. Испражнения имеют светлую окраску, а при полной непроходимости желчных путей (чаще вызванной опухолью) — ахолич-ные. Моча приобретает темную окраску цвета пива. В анализах крови отмечают увеличение СОЭ, лейкоцитоз (при остром холецистите в сочетании с холедохолитиазом). Концентрация прямого и непрямого билирубина в крови резко повышена, особенно при обтурирующих опухолях панкреатодуоденальной зоны. При холедохолитиазе, особенно при так называемых вентильных конкрементах, билирубинемия имеет ремиттирующий характер, билирубинурия и уробилинурия — перемежающийся. При опухолях, вызывающих полную непроходимость желчевыводящих путей, уробилинурия отсутствует при сохраненной билирубинурии. Уровень холестерина в крови повышен, концентрация сывороточного железа в норме или даже несколько снижена. Транс-аминазы крови умеренно увеличены, а при длительной желтухе могут возрастать. Значительно повышается уровень щелочной фосфатазы, особенно при желтухах опухолевой природы. Фруктозобисфосфат-альдолаза повышена незначительно, концентрация протромбина в крови снижена. Особенности клинического течения того или иного вида желтухи обусловлены характером заболевания, вызвавшего желтуху. Этот факт создает дополнительные трудности в дифференциальной диагностике желтух. Кроме перечисленных выше клинических и лабораторных методов, важную роль в диагностике желтух играют рентгенологические (в том числе и ан-гиографические), эндоскопические, радиологические, ультразвуковые методы исследования и компьютерная томография. Они позволяют получить ценную информацию, необходимую для дифференциальной диагностики различных видов желтух. В клинической практике хирург чаще всего имеет дело с обтурационной желтухой, реже — с печеночной, вызванной холестатическим гепатитом, хо-лангитом. Лечение. В предоперационном периоде во время обследования больного необходимо проводить комплекс мероприятий, направленных на нормализацию нарушенных функций организма, ликвидацию холангита, нарушений свертывающей и противосвертывающей систем крови. Тщательная предоперационная подготовка больных с желтухой позволяет выполнить оперативное вмешательство в более безопасных условиях, уменьшить частоту послеоперационных осложнений. Обтурационная желтуха является абсолютным показанием к операции. Выжидание очень опасно, так как приводит к глубокому поражению паренхимы печени и нарушению ее функций, ухудшению прогноза после операции вследствие развития инфекции (гнойный холангит) и возможности появления кровотечения, обусловленного недостатком резорбции витамина К. Срочные показания к операции возникают при гнойном холангите. Даже при ранних хирургических вмешательствах летальность достигает 5—15 % и более. Операции, применяемые при обтурационной желтухе, разнообразны и зависят от причины и уровня препятствия для оттока желчи. Холедохотомия с дренированием протока показана при желтухе, вызванной холедохолитиазом. При забытых конкрементах в холедохе чаще прибегают к их эндоскопическому ретроградному удалению. Используют также экстракцию конкрементов через Т-образный дренаж с помощью петли Дор-миа, промывание протока через дренаж растворами желчных кислот, гепарина и др. Трансдуоденальная папиллосфинктеротомия показана при стенозирую-щем папиллите, ущемившихся конкрементах в терминальном отделе общего желчного протока. В настоящее время обычно производят эндоскопическую папиллосфинктеротомию для извлечения конкрементов и восстановления проходимости протока. Билиодигестивные анастомозы формируют для отведения желчи из желчных протоков в тонкую кишку при доброкачественных заболеваниях (стриктуры, трубчатые протяженные стенозы, ранения протоков). При неоперабельных опухолях желчных протоков наложение анастомозов является паллиативным вмешательством. Холецистоэнтеростомию производят в случае проходимости пузырного протока при неоперабельных опухолях, закрывающих просвет дистальной части общего желчного протока. Дно пузыря соединяют с выключенной по Ру петлей тощей кишки или с двенадцатиперстной кишкой. Холедохо- или гепатикодуоденостомия показана при опухолях, закрывающих просвет дистального отдела общего желчного протока, рубцовых стриктурах, трубчатых стенозах его терминального отдела при хроническом панкреатите. При этой операции общий желчный или общий печеночный проток соединяют анастомозом с выключенной по Ру петлей тощей кишки. Глава 14 ПОДЖЕЛУДОЧНАЯ ЖЕЛЕЗА Поджелудочная железа и желчные протоки в процессе филогенеза формируются вместе с двенадцатиперстной кишкой. Поэтому довольно часто они поражаются одновременно. Поджелудочная железа расположена забрюшинно на уровне I —II поясничных позвонков, занимая положение между двенадцатиперстной кишкой и воротами селезенки. Длина ее составляет 15 — 20 см, ширина 3—6 см, толщина 2—3 см, масса железы в среднем 70—90 г. В поджелудочной железе различают головку, тело и хвост. Головку огибает двенадцатиперстная кишка; тело поджелудочной железы своей передней поверхностью предлежит к задней поверхности желудка. Эти органы отделены друг от друга узкой шелью — сальниковой сумкой (bursa omentalis). Задняя поверхность поджелудочной железы предлежит к нижней полой вене, верхнебрыжсечной вене и одноименной артерии, брюшной аорте, нижняя — соприкасается с нижнегоризонтальной ветвью двенадцатиперстной кишки. Позади поджелудочной железы в месте перехода ее головки в тело проходят верхние мезентериальные сосуды, а на уровне верхнего края железы по направлению к ее хвосту — селезеночная артерия. Селезеночная вена расположена позади железы (рис. 14.1). Главный проток поджелудочной железы (вирсунгов проток) образуется из слияния мелких дольковых протоков. Диаметр его колеблется от 0,5 до 2 мм в хвостовой части, 2—6 мм — в области большого дуоденального сосочка. В головке поджелудочной железы вирсунгов проток соединяется с добавочным протоком. В 10 % случаев добавочный проток берет на себя основную дренажную функцию поджелудочной железы. Взаимоотношения конечных отделов общего желчного протока и протока поджелудочной железы различны. Более часто оба протока образуют общую ампулу, которая открывается на большом сосочке двенадцатиперстной кишки (67 %), иногда ампула отсутствует (30 %). Общий желчный проток и проток поджелудочной железы при этом варианте впадают в двенадцатиперстную кишку раздельно. Иногда они соединяются друг с другом на значительном расстоянии от большого сосочка двенадцатиперстной кишки (3 %) и открываются одним отверстием, не образуя ампулу. В ряде случаев добавочный проток впадает в двенадцатиперстную кишку самостоятельно в малом дуоденальном сосочке, расположенном на 2—3 см выше большого дуоденального сосочка. Кровоснабжение поджелудочной железы осуществляется ветвями панкреатодуоденальной артерии (a. pancreaticoduodenalis), которая снабжает кровью большую часть головки. Ветви верхней брыжеечной артерии обеспечивают кровоснабжение головки и тела, а ветви селезеночной артерии (a. lienalis) — тела и хвоста поджелудочной железы. Вены идут совместно с артс-
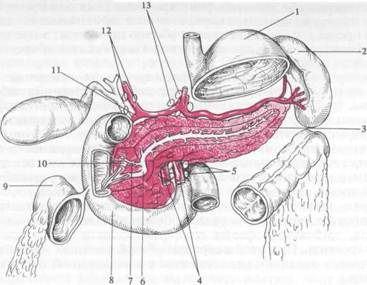
Рис. 14.1. Анатомия поджелудочной железы. I — желудок; 2 — селезенка; 3 — поджелудочная железа; 4 — верхние брыжеечные артерии и вена; 5 — брыжеечные лимфатические узлы; 6 — проток поджелудочной железы; 7 — добавочный проток поджелудочном железы; S — двенадцатиперстная кишка; 9 — толстая кишка; 10 — общий желчный проток; 11 — верхняя панкреатодуоденальная артерия; 12 — печеночные лимфатические узлы; 13 — парааортальные лимфатические узлы. риями и впадают в верхнюю брыжеечную и селезеночную вены, по которым кровь оттекает в поротную вену (v. porta). Лимфоотток происходит в лимфатические узлы, расположенные по верхнему краю поджелудочной железы, в воротах селезенки и печеночно-двенадцатиперстной связке. Частично лимфа оттекает в забрюшинные лимфатические узлы по ходу абдоминального отдела аорты и нижней полой вены. Лимфатическая система поджелудочной железы тесно связана с лимфатической системой желудка, кишечника, двенадцатиперстной кишки и желчевыводящих путей. Иннервации поджелудочной железы осуществляется ветвями чревного, печеночного, селезеночного и верхнебрыжеечного сплетений. Имеется тесная связь с иннервацией поджелудочной железы, двенадцатиперстной кишки, печени, желчевыводящих путей и желчного пузыря, что во многом определяет их функциональную взаимозависимость. Паренхима поджелудочной железы состоит из множества долек, отделенных друг от друга прослойками соединительной ткани. Каждая долька состоит из эпителиальных клеток, образующих ацинусы. За сутки железа выделяет 1000—1500 мл прозрачного щелочного (рН 7,0— 8,0) панкреатического сока. Особые паренхиматозные клетки поджелудочной железы образуют скопления неличиной 0,1 — 1 мм (панкреатические островки, островки Лангерганса), они имеют округлую или овальную форму, хорошее кровоснабжение и иннервацию. Панкреатические островки не имеют выводных протоков. В них выделяют четыре типа клеток: а, [!, 6 и f-клетки, обладающие различными функциональными свойствами. а-Клстки вырабатывают глюкагон, являющийся антагонистом инсулина. р-Клетки продуцируют инсулин, который увеличивает поглощение глюкозы тканями, снижает содержание сахара в крови, способствует фиксации гликогена в клетках печени. В противоположность инсулину глюкагон способствует выделению глюкозы из запасов в клетках печени и поддержанию уровня сахара а крови на оптимальном физиологическом уровне. 8-Клетки продуцируют сома-тостатин, оказывающий ингибирующес действие на желчеобразоватсльную функцию печени, продукцию желудочного, кишечного сока и внешнесекреторную функцию поджелудочной железы. Кроме того, соматостатин тормозит секрецию гормона роста, f-Клетки сскретируют панкреатический полипептид, физиологическая роль которого пока не установлена. Клетки поджелудочной железы сскретируют липокаин, который оказывает липолитическое действие, предотвращает гиперлипемию и жировую дистрофию печени. Протсолитичсские, липолитические и амилолитическис энзимы синтезируются и сохраня- ются в ацинарных клетках как гранулы зимогена, отделенные от других протеинов клеток. Энзимы внутри клетки сохраняются в неактивном состоянии, благодаря чему поджелудочная железа не подвергается разрушению. Поджелудочная железа обладает внешнесекреторной и инкреторной функциями. Внсш несекреторная функция железы заключается в продукции ацинарными клетками сока, богатого ферментами и бикарбонатами, обеспечивающими расщепление белков, жиров и углеводов до ингредиентов, способных всасываться в кишечнике. Протеолитиче-ские энзимы (трипсин, химотрипсин, карбоксипептидаза и эластаза) выделяются в протоковую систему железы в неактивном состоянии. В двенадцатиперстной кишке под влиянием фермента энтерокиназы они переходят в активную форму, принимая участие в расщеплении белков до полипептидов и аминокислот. Липаза поступает в протоковую систему железы в активном состоянии. Фосфолипаза А выделяется как проэнзим В неактивном состоянии, подвергается активации трипсином в двенадцатиперстной кишке. Гликолитический фермент а-амилаза, расщепляющая углеводы до мо-но- и дисахаридов, выделяется в протоковую систему в активной форме Регуляция внешнесекреторной деятельности поджелудочной железы осуществляется ней-рогуморальным путем. Стимулирующее воздействие оказывают блуждающие нервы и некоторые гастроинтестинальные гормоны (секретин, холецистокинин-панкреозимин, гастрин). Тормозное влияние обеспечивают соматостатин и глюкагон. Эндокринная функция поджелудочной железы осуществляется указанными клетками островков железы. На долю р-клеток приходится 60—70 % клеточного состава островков. Основным стимулятором выделения инсулина является пиша, богатая белками и углеводами. Компенсаторные возможности поджелудочной железы настолько велики, что лишь при удалении 70—80 % ее паренхимы могут появиться клинические проявления инсулиновой недостаточности (сахарный диабет). 14.1. Аномалии и пороки развития Добавочная (аберрантная) поджелудочная железа встречается очень редко, располагается в стенках желудка или двенадцатиперстной кишки, тощей кишки или ее брыжейке, дивертикуле подвздошной кишки. Аберрантная железа проявляется клиническими симптомами достаточно редко. Чаще всего она является случайной находкой при лапаротомии, выполняемой по поводу другого заболевания (как правило, по поводу язвенной болезни или калькулезного холецистита). Следует отметить, что аберрантная ткань железы имеет точно такое же строение, как и нормальная ткань поджелудочной железы, включая и выводной проток, открывающийся в просвет полого органа (желудок, тонкая кишка). Вот почему возможно развитие острого панкреатита в аберрантной железе, включая и деструктивные формы. Существенно реже наблюдают изъязвление слизистой оболочки с последующим желудочно-кишечным кровотечением в зоне, где выводной проток аберрантной железы открывается в просвет полого органа. Лечение. Добавочную поджелудочную железу удаляют хирургическим путем. Кольцевидная поджелудочная железа. Это редкий порок развития, при котором нисходящая часть двенадцатиперстной кишки оказывается частично или полностью окруженной тканью головки поджелудочной железы. Двенадцатиперстная кишка при этом сужена, что является причиной частичной хронической дуоденальной непроходимости. Клиническая картина и диагностика. Наблюдается рвота после приема пищи. Если препятствие располагается дистальнее впадения общего желчного протока, вместе с рвотой выделяется желчь. Стеноз двенадцатиперстной кишки обычно выявляется в детском возрасте, реже — в зрелом. Часто кольцевидная поджелудочная железа только является случайной интраопе-рационной находкой. Диагноз устанавливают с помощью рентгенологического исследования. При обзорной рентгеноскопии обнаруживают стеноз двенадцатиперстной кишки с расширением ее проксимальных отделов, скопление газа в луковице двенадцатиперстной кишки и желудке. Наиболее четко патологические изменения выявляются при проведении релаксационной дуоденографии, ультразвукового исследования. Лечение. Хирургическое вмешательство показано при нарушении эвакуации содержимого из желудка и выраженных клинических проявлениях. Обычно с учетом местных изменений формируют анастомозы в обход суженного участка двенадцатиперстной кишки: анастомоз между расположенным выше сужения расширенным участком дуоденум и участком, расположенным ниже; дуоденоеюноанастомоз с расширенным верхним отрезком кишки. При растянутом подвижном желудке можно наложить гастродуоде-нальный анастомоз с участком кишки, расположенным ниже препятствия. Не рекомендуется производить резекцию участка железы во избежание острого панкреатита или свища. 14.2. Повреждения поджелудочной железы Различают открытые и закрытые повреждения поджелудочной железы. Открытые повреждения возникают при огнестрельных и ножевых ранениях, закрытые — при тупой травме живота. Повреждения могут быть изолированными или сочетаться с повреждениями соседних органов (двенадцатиперстная кишка, желудок, тонкая кишка). Последние виды травмы из-за особенностей расположения поджелудочной железы наблюдаются чаще. При закрытых травмах чаще повреждается тело поджелудочной железы, которое в момент ушиба и повышения внутрибрюшного давления оказывается более плотно прижатым к позвонкам, чем другие ее отделы. Различают четыре степени тяжести травм поджелудочной железы: I) ушиб и кровоизлияние в ткань железы; 2) поверхностный разрыв капсулы и паренхимы поджелудочной железы; 3) глубокий разрыв паренхимы без повреждения протока поджелудочной железы; 4) разрыв поджелудочной железы с повреждением протока. При повреждении головки поджелудочной железы, в которой располагаются крупные сосуды, превалируют признаки внутрибрюшного кровотечения, а при повреждении тела и хвоста — симптомы острого посттравматического панкреатита и его осложнений (кисты и свищи поджелудочной железы). Клиническая картина и диагностика. При массивной травме возникают кровотечение в брюшную полость, симптомы травматического шока. В более поздние сроки появляются признаки травматического панкреатита, а в случае повреждения полых органов возникает перитонит. Больные предъявляют жалобы на резкие боли в верхнем отделе живота, иррадиирующие в спину, нередко носящие характер опоясывающих, тошноту, рвоту. Диагностика повреждений поджелудочной железы из-за отсутствия па-тогномоничных симптомов затруднена. Для ранней диагностики целесообразно использовать УЗИ, с помощью которого обнаруживают скопление крови или экссудата, определить состояние поджелудочной железы и других органов брюшной полости и забрюшинного пространства. Скопление крови в брюшной полости можно обнаружить с помощью "шарящего" катетера, который вводят в брюшную полость через небольшой разрез. В полученной при этой процедуре жидкости необходимо определить содержание амилазы, что позволит подтвердить повреждение поджелудочной железы. В условиях хорошо оснащенной больницы можно воспользоваться лапароскопией, ко- торая позволяет более четко выявить характер повреждения и даже произвести некоторые манипуляции или оперативные вмешательства, такие как остановка кровотечения из поврежденных сосудов, подведение дренажей к поврежденной железе и т. п. Наличие значительного скопления крови в брюшной полости является показанием к срочной лапаротомии. Лечение только хирургическое. Операция должна проводиться до развития воспалительных процессов в самой поджелудочной железе, в брюшной полости и в забрюшинной клетчатке. При небольших разрывах поджелудочной железы удаляют образовавшуюся гематому, ушивают разрывы паренхимы отдельными швами и дренируют сальниковую сумку через контрапертуру в поясничной области. При повреждении левой половины поджелудочной железы с нарушением целости протоков производят резекцию ее тела и хвоста. При размозжении головки поджелудочной железы с разрывом главного панкреатического протока выполняют панкреатэктомию или панкреатодуо-денальную резекцию, хотя эти операции довольно сложны и травматичны, а послеоперационная летальность достигает 60—80 %. 14.3. Острый панкреатит Острый панкреатит — заболевание поджелудочной железы, возникающее в результате аутолиза тканей поджелудочной железы липолитическими и активированными протеолитическими ферментами, проявляющееся широким спектром изменений — от отека до очагового или обширного геморрагического некроза. В большинстве случаев (около 90 %) наблюдается незначительный аутолиз тканей, сопровождающийся только отеком поджелудочной железы и умеренными болями. В тяжелых случаях возникает жировой или геморрагический некроз ткани с тяжелыми метаболическими нарушениями, гипотензией, секвестрацией жидкости, полиорганной недостаточностью и летальным исходом. После перенесенного острого панкреатита функции поджелудочной железы, как правило, приходят к норме. При хроническом панкреатите сохраняются остаточные явления с нарушением функций поджелудочной железы и периодическим обострением. Среди неотложных хирургических заболеваний органов брюшной полости острый панкреатит по частоте занимает 3-е место, уступая лишь острому аппендициту и острому холециститу. Более часто заболевают лица зрелого возраста (30—60 лет), женщины — в 2 раза чаще, чем мужчины. Этиология и патогенез. Патогенез острого панкреатита недостаточно изучен. Основной этиологический фактор — аутолиз паренхимы поджелудочной железы, возникающий обычно на фоне гиперстимуляции экзокринной функции, частичной обтурации ампулы большого дуоденального сосочка, повышения давления в вирсунговом протоке, рефлюкса желчи в вирсунгов проток. Остро развивающаяся внутрипротоковая гипертензия вызывает повреждение и повышение проницаемости стенок терминальных протоков. Создаются условия для активизации энзимов, выхода их за пределы протоков, инфильтрации паренхимы и аутолиза ткани поджелудочной железы. У больных желчнокаменной болезнью временное затруднение оттока желчи приводит к повышению давления и рефлюксу ее в панкреатический проток. Эти изменения связывают с миграцией мелких конкрементов или песка (микролитиаз). Благоприятным условием для желчной гипертензии является наличие общего канала (ампулы) для оттока желчи и панкреатического сока. В поддержку этой теории можно привести тот факт, что общий канал (ампула), по данным холангиографии, у лиц, болевших панкреатитом, наблюдается почти в 90 %, а у лиц с желчнокаменной болезнью, не имевших в анамнезе эпизоде- панкреатита, — всего у 20—30 %. Часто причиной острого панкреатита является чрезмерное употребление алкоголя и прием жирной пищи. Известно, что алкоголь усиливает тонус и резистентность сфинктера Одди. Это может послужить причиной затруднения оттока экзокринного секрета поджелудочной железы и повышения давления в мелких протоках. Экспериментальными исследованиями доказано, что энтеральное введение алкоголя повышает давление в протоках поджелудочной железы и увеличивает проницаемость стенок мелких протоков для макромолекул панкреатического сока. Имеются сообщения о том, что крупные молекулы белка могут вызвать затруднение оттока панкреатического сока. Алкоголь усиливает секрецию желудочного сока и продукцию соляной кислоты, которая стимулирует продукцию секретина, вызывающего экзо-кринную гиперсекрецию поджелудочной железы, создает предпосылки для повышения давления в протоках. Таким образом, создаются условия для проникновения энзимов в паренхиму, активации протеолитических ферментов и аутолиза клеток поджелудочной железы. В зависимости от причины внутрипротоковой гипертензии различают билиарный и алкогольный панкреатит. Эти разновидности панкреатита составляют 90 % всех панкреатитов. Каждый из них имеет определенные особенности в клиническом течении и исходе болезни. К более редким причинам развития острого панкреатита относятся открытые и закрытые травмы живота, интраоперационные повреждения ткани железы, атеросклеротиче-ская окклюзия висцеральных ветвей абдоминального отдела аорты, портальная гипертензия, некоторые лекарственные препараты (кортикостерои-ды, эстрогенные контрацептивы и антибиотики тетрациклинового ряда). Некроз панкреоцитов и клетчатки, окружающей дольки поджелудочной железы, в самом начале процесса происходит под влиянием липазы. Липаза проникает внутрь клетки, гидролизует внутриклеточные триглицериды с образованием жирных кислот. В поврежденных клетках железы развивается внутриклеточный ацидоз со сдвигом рН до 3,5—4,5. В условиях ацидоза неактивный трипсиноген трансформируется в активный трипсин, который активирует фосфолипазу А, высвобождает и активирует лизосомальные ферменты (эластазу, коллагеназу, химотрипсин и др.). Содержание фосфо-липазы А и лизолецитина в ткани поджелудочной железы при остром панкреатите существенно увеличивается. Это свидетельствует о ее роли в ауто-лизе ткани железы. Под воздействием липолитических, активированных протеолитических ферментов появляются микроскопические или макроскопически заметные очаги жирового некроза паренхимы поджелудочной железы. На этом фоне эластаза подвергает лизису стенки венул и междоль-ковые соединительнотканные перегородки. В результате этого возникают обширные кровоизлияния, происходит трансформация жирового панкрес некроза в геморрагический. Таким образом, протеолитическая и липолити-ческая фазы развития острого деструктивного панкреатита взаимосвязаны друг с другом. К очагам первичного некроза устремляются лейкоциты. Скопление лейкоцитов вокруг очагов некроза означает развитие защитной воспалительной реакции, сопровождающейся гиперемией и отеком. Для отграничения очагов некроза и элиминации некротической ткани макрофаги, лейкоциты, лимфоциты, клетки эндотелия выделяют провоспалительные (ИЛ-1; ИЛ-6; ИЛ-8) и антивоспалительные (ИЛ-4; ИЛ-10 и др.) интерлейкины, активные кислородные радикалы. Небольшие очаги некроза в результате этой реак-
При обширном некрозе макрофаги, нейтрофильные лейкоциты, лимфоциты подвергаются избыточной стимуляции, продукция интерлейкинов и кислородных радикалов возрастает, выходит из-под контроля иммунной системы. Изменяется соотношение про- и антивоспалительных интерлейкинов. Они повреждают не только ткани железы, но и другие органы. Некроз тканей вызывают не столько сами интерлейкины, сколько активные кислородные радикалы, оксид азота (N0) и наиболее агрессивный перокси-нитрил (ONOO). Интерлейкины лишь подготавливают почву для этого: снижают тонус венозных капилляров, повышают их проницаемость, вызывают тромбоз капилляров. Изменения в микроциркуляторном русле вызываются преимущественно оксидом азота. Воспалительная реакция прогрессирует, зона некроза расширяется. Местная реакция на воспаление превращается в системную, развивается синдром системной реакции на воспаление (Systemic Inflammatory Respons Syndrome). Тяжесть состояния больного коррелирует с высоким содержанием в крови ИЛ-6, ИЛ-8. При повышенной концентрации их в крови с высокой степенью вероятности можно прогнозировать полиорганную дисфункцию и недостаточность. Изменения в микроциркуляторном русле приводят к перемещению значительной части жидкости организма в интерстициальное пространство. Происходит обезвоживание, снижается ОЦК, наступают водно-электролитные нарушения и нарушение кислотно-основного состояния. На фоне повышенной концентрации интерлейкинов и гиперферментемии появляются очаги некроза на сальнике и брюшине. Выпот в брюшной полости содержит амилазу и другие энзимы поджелудочной железы в высокой концентрации. Токсичные продукты, циркулирующие в крови, оказывают прямое токсическое действие на сердце, почки, печень, ЦНС. Тяжесть синдрома системного ответа на воспаление возрастает в соответствии с нарастающей ишемией, увеличением концентрации N0, цитокинов, гипоксией и дистрофией в жизненно важных органах. Интоксикация в сочетании с гиповолемией быстро приводит к развитию шока. Возникают диссеминированное внутрисо-судистое свертывание (ДВС-синдром) и полиорганная недостаточность. В последующем через 10—15 дней наступает фаза секвестрации и расплавления омертвевших участков. Секвестры и накопившаяся вблизи них жидкость могут некоторое время оставаться асептическими. Инфицирование и нагноение их с образованием парапанкреатических и забрюшинных абсцессов происходят в связи с транслокацией бактерий из просвета парализованного кишечника, возникающей в ответ на патологические изменения в поджелудочной железе и забрюшинной клетчатке. В позднем периоде в зоне некроза образуются ложные кисты поджелудочной железы. Классификация. По характеру изменений в поджелудочной железе выделяют: 1) отечный или интерстициальный панкреатит; 2) жировой панкрео-некроз и 3) геморрагический панкреонекроз. Отечная или абортивная форма панкреатита развивается на фоне незначительного, микроскопического повреждения клеток поджелудочной железы. Фаза отека может в течение 1—2 дней превратиться в фазу некроза. При прогрессирующем панкреатите развивается жировой панкреонекроз, который по мере развития кровоизлияний превращается в геморрагический с образованием обширного отека в забрюшинной клетчатке и появлением геморрагического выпота в брюшной полости (панкреатогенный асептический перитонит). В ряде случаев наблюдаются смешанные формы панкреа-
тита: геморрагический панкреатите очагами жирового некроза и жировой панкреонекроз с кровоизлияниями (рис. 14.2). В зависимости от распространенности процесса различают очаговый, субототальный и тотальный панкреонекроз. Дата добавления: 2015-01-18 | Просмотры: 929 | Нарушение авторских прав |
 ции отграничиваются, подвергаются лизису с последующей элиминацией продуктов распада. Эти процессы вызывают в организме умеренную местную реакцию на воспаление.
ции отграничиваются, подвергаются лизису с последующей элиминацией продуктов распада. Эти процессы вызывают в организме умеренную местную реакцию на воспаление.