|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Нарушения ритма 10 страница
Вместо традиционной рентгеноконтрастной флебографии в сложных для дифференциальной диагностики случаях может быть использована магнитно-резонансная флебография. Тромботические массы при неокклюзивном тромбозе на МР-флебограммах выглядят как дефекты наполнения на фоне яркого сигнала от движущейся крови. При тромбе, окклюзирующем просвет вены, МР-сигнал от венозного сегмента, выключенного из кровообращения, отсутствует. Лечение. Обычно используют консервативное, значительно реже оперативное лечение. При неполноценном лечении тромбоза глубоких вен почти у 50 % больных может возникнуть эмболия легочных артерий на протяжении трехмесячного периода. Адекватное лечение острых тромбозов глубоких вен нижних конечностей антикоагулянтами уменьшает риск распространения тромба и эмболии легочной артерии до 5 % и меньше. Для большинства больных методом выбора в лечении тромбоза глубоких вен и эмболии легочной артерии является болюсное (одноразовое) внутривенное введение 5000 ЕД гепарина с последующим внутривенным капельным (или с помощью инфузомата) введением гепарина со скоростью 1000— 1200 ЕД/ч. В общей сложности для адекватной гепаринотерапии за сутки вводят до 30 000—40 000 ЕД, чтобы увеличить активированное частичное тромбопластиновое время в 1,5 раза и более от исходного уровня. При этих условиях риск рецидива тромбоза глубоких вен уменьшается до 2 % и менее. Внутривенную гепаринотерапию в таком объеме продолжают 7—10 дней. В течение последних 4—5 дней этого периода добавляют непрямые антикоагулянты на срок до 3 мес. Вместо обычного гепарина в этой схеме лечения может быть использован низкомолекулярный гепарин, который вводят подкожно 1—2 раза в сутки. Высокая эффективность этого метода лечения подтверждена многочисленными рандомизированными клиническими исследованиями в ряде медицинских центров. Комплексное консервативное лечение сочетают с ранней активизацией больных. Ножной конец кровати целесообразно приподнять под углом 15— 20°. Постельный режим показан пациентам только в начальной стадии заболевания при наличии болей и отека пораженной конечности. После стихания болей и уменьшения отека целесообразно назначить комплекс специальных гимнастических упражнений, улучшающих венозной отток. Занятия проводят под контролем методиста лечебной физкультуры. Вопрос об активизации больных с повышенным риском развития тромбоэмболии следует решать крайне осторожно. К этой группе относят лиц с предшествующими эмболическими осложнениями, больных с изолированным тромбозом бедренно-подколенного сегмента справа, а также пациентов с илеофеморальным венозным тромбозом.
Тромбэктомия из глубоких вен при помощи катетера Фогарти находит ограниченное применение в связи с большой частотой повторных тромбозов и тромбоэмболии. Применение ее возможно лишь в первые 4— 7 сут от момента возникновения тромбоза, пока не произошла плотная фиксация тромба к стенкам вены. Тромбоз магистральных вен чаще носит восходящий характер. Он берет начало в венах голени, из которых удалить тромб невозможно. Поэтому после тромбэктомии из крупных вен часто развиваются ранние послеоперационные ретромбозы. Шунтирующие операции не получили распространения в связи со сложностью их выполнения и частыми тромбозами шунтов. С целью профилактики тромбоэмболии легочной артерии ранее часто в нижней полой вене устанавливали самофиксирующиеся кава-фильтры, имеющие форму зонтика с отверстиями для прохождения крови (рис. 19.13). Фильтр устанавливали в инфрареналь- ном сегменте нижней полой вены путем чрескожного введения специального устройства, в котором кава-фильтр находится в свернутом состоянии. Проводник вместе с кава-фильтром может быть введен через яремную вену или бедренную вену контралатеральной стороны. Противоэмболическая функция фильтра может быть нарушена скоплением фрагментов тромба в отверстиях фильтра или вследствие отрыва верхушки тромба, способного вызвать окклюзию нижней полой вены ниже кава-фильтра. Разрастание тромба выше фильтра не наблюдается, вследствие того что мощный кровоток из почечных вен не дает образоваться тромбу над фильтром. При невозможности имплантации кава-фильтра, по показаниям, производили пликацию нижней полой вены. При этой процедуре ниже почечных вен стенка полой вены прошивается редко расположенными (через одну скрепку) металлическими скрепками или специальным устройством. Показания к установке кава-фильтра или пликации в настоящее время ограничены в связи с опасностью тромбоза полой вены ниже фильтра. Установка кава-фильтров более оправдана для профилактики повторных эмболии ветвей легочной артерии и при флотирующем тромбе, создающем реальную угрозу массивной тромбоэмболии легочной артерии. Включение в лекарственную терапию тромболитических препаратов практически невозможно в связи с большим числом ограничений и крайне высокой опасностью кровотечения в ближайшем послеоперационном периоде. Менее 10 % больных с тяжелым илеофеморальным тромбозом могли бы быть кандидатами на тромболитическую терапию. Сравнительное рандомизированное исследование показало, что частота развития хронической венозной недостаточности у больных, леченных гепарином, не отличается от таковой у леченных тромболитическими препаратами. Профилактика. Предупреждение тромбозов глубоких вен имеет большое значение, так как избавляет больных от таких грозных осложнений этого заболевания, как тромбоэмболия легочной артерии, посттромбофлебитиче- 38-2375 ский синдром. Необходимость проведения профилактики тромбозов особенно велика у пациентов с высоким риском: у лиц пожилого возраста, у больных с онкологическими и тяжелыми сердечно-сосудистыми заболеваниями; при ожирении, при тяжелых травматичных операциях. Профилактика флеботромбозов особенно показана у перечисленной категории больных при гинекологических, онкологических и травматологических операциях. Профилактические мероприятия должны быть направлены на предотвращение венозного стаза, ускорение кровотока в глубоких венах с помощью бинтования ног эластичными бинтами, устранение гиперкоагуляции, снижение агрегационной активности тромбоцитов соответствующими препаратами. Пассивная профилактика предусматривает бинтование нижних конечностей (до коленных суставов) специальными эластичными бинтами до оперативного вмешательства, сразу после поступления в стационар. Сдавление поверхностных вен бинтами ускоряет кровоток в глубоких венах, препятствует образованию мелких тромбов в суральных синусах икроножных мышц. Пациенту предлагается быть активным, возможно больше двигаться. Антикоагулянтные препараты до операции не применяют. Эластичные бинты сохраняются на ногах во время операции и в течение 3—4 нед после операции. Пассивная профилактика показана при низкой степени риска. В некоторых учреждениях во время операции или сразу после нее применяют интермиттирующую волнообразную пневматическую компрессию голеней и бедер с помощью специальных аппаратов с надувными манжетками, которые надевают на ноги. Поочередное сокращение манжеток сначала на голени, затем на бедре ускоряет кровоток в глубоких венах, препятствует застою крови в венах голени, предупреждает тромбообразо-вание. Активная профилактика основана на применении антикоагулянтов прямого действия в сочетании с методом пассивной профилактики. Во всех группах риска профилактику следует начинать до операции, так как тромбоз глубоких вен более чем в 50 % начинается уже на операционном столе. Первую дозу обычного нефракционного гепарина или низкомолекулярного фракционированного гепарина рекомендуется вводить за 2 ч до начала операции и продолжать после операции под контролем определения величины частичного тромбопластинового времени. При умеренном риске флеботромбоза больным вводят один раз в день 20 мг фракционированного низкомолекулярного гепарина (фраксипарин, фрагмин и др.) или 5000 ЕД обычного гепарина 2—3 раза в сутки. При высоком риске дозу препаратов увеличивают в два раза. Гепаринотерапию продолжают в течение 7—10 дней, затем переходят на непрямые антикоагулянты. Наряду с гепарином во время операции и в течение нескольких дней после нее вводят препараты, улучшающие реологические свойства крови и микроциркуляцию (реополиглюкин, полиглюкин), антиагреганты (куран- тил, трентал и другие). Устранение венозного стаза после операции достигается не только наложением эластичных бинтов, но и ранними физическими упражнениями, ранним вставанием с постели, переводом больного на общий режим. Эластическую компрессию голеней и стоп с помощью эластичных бинтов или чулок необходимо продолжать в течение 2—3 нед после операции. Комбинированный способ профилактики позволяет свести до минимума риск эмболии легочной артерии. 19.7. Окклюзии ветвей верхней полой вены Тромбоз подключичной вены (синдром Педжета—Шреттера). Развитию тромбоза способствуют топографоанатомические особенности расположения подключичной вены в узком подключично-реберном пространстве в окружении костных и сухожильно-мышечных образований. При сильных напряжениях мускулатуры плечевого пояса, сочетающихся с движениями в плечевом суставе, размеры подключично-реберного пространства уменьшаются, и вена оказывается сдавленной между ключицей и I ребром. При этом возникают благоприятные условия для повреждения и нарушения оттока крови по подключичной вене, а следовательно, и тромбообразования. Синдром Педжета—Шреттера наблюдается, преимущественно,у молодых людей в возрасте 20—40 лет с хорошо развитой мускулатурой. Тромбоз подключичной вены наблюдается при высоком стоянии I ребра, гипертрофии подключичной мышцы и мышечно-сухожильной части малой грудной мышцы (синдром верхней апертуры грудной клетки). Кроме того, причиной обструкции могут быть опухоли средостения, шейное ребро, экзостоз, тромбоз, вызванный травмой. Ятрогенный тромбоз подключичной вены часто наблюдается после установки центральных венозных катетеров или водителей сердечного ритма. Клиническая картина. Основными клиническими признаками острого тромбоза подключичной вены являются выраженный отек руки, боли, цианоз кожных покровов в области кисти и предплечья, напряжение и расширение подкожных вен верхней конечности и плечевого пояса на соответствующей стороне (чаще справа). Отек плотный, характеризуется отсутствием ямок при надавливании. Нередко он захватывает не только руку и плечевой пояс, но и переходит на верхнюю половину грудной клетки. Расширение и напряжение подкожных вен в ранние сроки заболевания заметны лишь в области локтевой ямки. Впоследствии локализация расширенных вен соответствует границам распространения отека. При распространении тромбоза на подкрыльцовую и плечевую вены заболевание протекает тяжело. Нарастающий отек тканей в ряде случаев ведет к сдавлению артериальных стволов, вследствие чего ослабевает пульс на лучевой артерии и снижается температура конечности. Нарушения артериального кровообращения иногда настолько значительны, что возникает опасность развития гангрены. После стихания острых явлений наступает обратное развитие клинической картины. Однако у части больных полного регресса заболевания не происходит, развивается хроническая стадия синдрома. Диагностика острого тромбоза подключичной вены в большинстве случаев не представляет трудностей. Она основывается на наличии указанных выше симптомов и на частой связи заболевания с физической нагрузкой. Ценным методом исследования, позволяющим судить о локализации и распространенности тромбоза, степени развития коллатеральных сосудов, является ультразвуковая допплерография и рентгенологическая флебография, при которой контрастное вещество вводят в кубитальную вену или в одну из вен тыльной поверхности кисти. Для диагностики также применяется дуплексное сканирование. Лечение. В основном применяют консервативное лечение. Показания к хирургическому лечению возникают при угрозе развития венозной гангрены, выраженных регионарных гемодинамических нарушениях. 19.8. Эмболия ле. очной артерии Этим термином обозначают синдром, обусловленный полной или частичной закупоркой легочной артерии или ее ветвей эмболами, состоящими из тромбов (тромбоэмболия), капель жира (жировая эмболия), пузырьков воздуха (воздушная эмболия). Эмболия легочной артерии и тромбофлебит глубоких вен по сути дела являются фазами одного заболевания. Эффективное предупреждение тромбоэмболии легочной артерии основано на трех принципах: I) правильной профилактике, 2) ранней диагностике и 3) полноценном лечении тромбоза глубоких вен. Этиология и патогенез. Наиболее часто встречается тромбоэмболия ветвей легочной артерии вследствие переноса током крови частей оторвавшегося тромба в легочную артерию. В США ежегодно умирают от тромбоэмболии легочной артерии 175 000 пациентов. Она является одной из наиболее частых причин внезапной смерти. По данным вскрытия, частота ее колеблется от 4,4 до 14,7 %. Тромбоз вен голени, бедра и таза является наиболее частым источником эмболов, вызывающих тромбоэмболию легочной артерии. Реже причиной образования эмболов в венозной системе является тромбоз вен верхней конечности или образование тромбов в правых отделах сердца. Эмболы могут закупоривать ветви легочной артерии или ее основные стволы. В зависимости от этого выключается из кровообращения большая или меньшая часть сосудистого русла легкого. В соответствии с этим различают малую, субмассивную, массивную (две и более долевых артерии) и молниеносную, или смертельную, эмболию, когда происходит закупорка основных стволов легочной артерии с выключением из кровообращения свыше 50—75 % сосудистого русла легких. Вслед за эмболией ветвей легочной артерии в 10—25 % случаев развивается инфаркт легкого или инфарктная пневмония. Окклюзия легочной артерии приводит к резкому повышению давления в ней вследствие возрастания сопротивления току крови. Это влечет за собой перегрузку правого желудочка сердца и правожелудочковую недостаточность. Параллельно с этим уменьшается приток крови в левое предсердие и желудочек, уменьшается сердечный выброс, начинает снижаться артериальное давление, нарушается газообмен в легких, возникает гипоксемия. Указанные нарушения уменьшают коронарный кровоток, что может привести к левожелудочковой недостаточности, отеку легких и смерти. В соответствии с распространенностью окклюзии ветвей легочной артерии (по данным ангиографии легочной артерии) и клиническими симптомами выделяют 4 степени тяжести тромбоэмболии легочной артерии (табл. 19.1). Малая и субмассивная тромбоэмболия легочной артерии (I и II степени) проявляется незначительными клиническими симптомами иногда в виде инфарктной пневмонии или плеврита. Массивная тромбоэмболия (III степень) сопровождается тяжелым шоковым состоянием, а молниеносная (IV степень) развивается, когда из кровообращения выключается более 50 % артериального русла легкого, обычно заканчивается смертью в течение нескольких минут. Клиническая картина и диагностика. Классическими симптомами тромбоэмболии легочной артерии являются внезапное ощущение нехватки воздуха (тахипноэ, диспноэ), кашель, тахикардия, боли в груди, набухание шейных вен, цианоз лица и верхней половины туловища, влажные хрипы, иногда кровохарканье, шум трения плевры, Таблица 19.1. Клиническая и функциональная характеристика эмболии легочной артерии
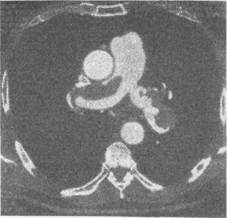
повышение температуры тела, коллапс. Оптимальный современный подход к диагностике тромбоэмболии легочной артерии включает определение ЭКГ, газов крови, рентгенограмму и ангиограмму сосудов легких, дуплексное сканирование вен таза и нижних конечностей и компьютерную томографическую ангиографию легочных артерий, определение содержания Д-димера в крови. Детальное инструментальное исследование при подозрении на тромбоэмболию легочной артерии целесообразно проводить после предварительного болюсного введения 5000 ЕД нефракционированного гепарина. В зависимости от степени тяжести эмболии выделяют легочно-плевральный, кардиальный и церебральный синдромы. Легочно-плевральный синдром чаще возникает при малой и субмассивной тромбоэмболии, т. е. при окклюзии периферических ветвей легочной артерии или одной долевой. Он проявляется одышкой, болями в груди (чаще в нижних отделах ее), кашлем, иногда сопровождающимся выделением мокроты с примесью крови. Кардиальный синдром более характерен для массивной тромбоэмболии. Для него типичны тахикардия, набухание шейных вен, боли и ощущение тяжести за грудиной, усиленный сердечный толчок, грубый систолический шум. Расщепление II тона указывает на развитие выраженной легочной гипертензии. Нередко наблюдается повышение центрального венозного давления, шок, потеря сознания. Достаточно часто единственным симптомом при исследовании сердечно-сосудистой системы оказывается тахикардия. ЭКГ может выявить признаки ишемии миокарда правого желудочка, отклонение электрической оси сердца вправо, блокаду правой ножки пучка Гиса, нарушение ритма. Типичным считают подъем сегмента SТ выше изоэлектрической линии, отрицательный зубец Т в III отведении и снижение сегмента ST в I и II отведениях. Отсутствие перечисленных изменений ЭКГ не исключает эмболию легочной артерии. При анализе газов крови выявляется дыхательный алкалоз, гипоксия, ги-покапния (снижение концентрации кислорода и углекислоты в артериальной крови). При более тяжелой степени эмболии или прогрессировании ее возникает ацидоз, нарастает гипоксия. Церебральный синдром связан с гипоксией мозга; чаще наблюдается у пожилых пациентов; проявляется потерей сознания, судорогами, гемиплегией, непроизвольным выделением мочи и кала. Указанные синдромы и свойственные им симптомы могут сочетаться в различных комбинациях в зависимости от степени тяжести тромбоэмболии. Диагностика тромбоэмболии легочной артерии трудна. Прижизненная диагностика осуществляется лишь в 30—40 % наблюдений, т. е. правильный диагноз является скорее исключением, чем правилом. Рентгенологическое исследование недостаточно информативно. Наиболее важными признаками являются высокое стояние диафрагмы, затемнение в базальных сегментах (ателектаз, инфарктная пневмония), плевральный экссудат. Нормальная рентгенограмма легких не исключает эмболии. Селективная ангиография легочной артерии (ангиопуль-монография) позволяет наиболее достоверно поставить диагноз, так как этот метод высокочувствителен и специфичен. На ангиограммах выявляются прямые признаки тромбоэмболии легочной артерии: изображение тромба, внутрисосудистые дефекты наполнения, обусловленные его наличием, полная обтурация сосуда с расширением его проксимальнее закупорки и отсутствие контуров сосуда дистальнее расположения эмбола. Для диагноза важны и непрямые признаки: уменьшение кровенаполнения периферических участков легкого дистальнее закупорки, удлинение артериальной фазы вследствие повышения периферическрго сопротивления сосудистого русла легких, асимметрия заполнения сосудов. В процессе ангиографии можно измерить давление в легочной артерии и разрушить тромб концом катетера, т. е. произвести реканализацию и начать лечение антикоагулянтами и тромболитическими препаратами. Перфузионная и ингаляционная сцинтиграфия в 90 % случаев позволяет обнаружить изменения, связанные с эмболией легочной артерии, однако эти методы не столь информативны, как ангиография. В настоящее время наиболее перспективным методом диагностики тромбоэмболии легочной артерии становится КТ-ангиография легочных артерий. Ее существенным преимуществом перед традиционной рентгеноконтрастной ангиопульмонографией является быстрота выполнения и необременительность для обследуемого. При КТ-ангиографии можно выявить тромбы в просвете легочной артерии (рис. 19.14), а также изменения в ткани легкого (инфаркты), экссудат в плевральной полости, изучить состояние сердца (тромбы в его полостях, постинфарктный кардиосклероз или аневризма). Для определения источника эмболии целесообразно исследовать вены таза и конечностей с помощью дуплексного ультразвукового сканирования. Лечение. Основной целью лечения является восстановление кровотока в легочной артерии. Объем лечебных мероприятий определяется массивностью, тяжестью эмболии. В качестве первоочередных мероприятий необходимо внутривенно ввести 5000 ЕД гепарина, придать возвышенное положение верхней части тела больного,
начать инсуффляцию кислорода через назальный катетер (не менее 3 л в 1 мин), ввести обезболивающий препарат или седа-тивное средство, установить катетер в подключичную вену для немедленного внутривенного капельного (или с помощью инфузома-та) введения гепарина со скоростью до 1250 ЕД/ч, чтобы обеспечить постоянный уровень концентрации препарата в крови и поддерживать АЧТВ (активированное частичное тромбопластиновое время) на уровне в 1,5—2 раза выше исходного. Непрерывное внутривенное введение гепарина более надежно позволяет поддерживать постоянную концентрацию его в крови по сравнению с прерывистым. Суточная доза гепарина составляет 30 000—40 000 ЕД. Гепаринотерапия позволяет предотвратить нарастание тромбов. Такой режим лечения поддерживают в течение 7—10 дней. Затем переходят к лечению непрямыми (оральными) антикоагулянтами продолжительностью до трех месяцев. Одновременно с этим проводят интенсивную терапию при периодическом измерении центрального венозного давления. При субмассивной эмболии (II степень) наряду с указанными мероприятиями целесообразно назначить се рде ч н ы е и антиаритмические средства, антибиотики для профилактики инфекции. При массивной тромбоэмболии (III степень) с выраженными клиническими симптомами и тенденцией к ухудшению состояния гепаринотера-пию целесообразно дополнить тромболитической терапией, если нет противопоказаний к ее применению. Клинический опыт показал, что тромболитическая терапия не имеет существенных преимуществ перед гепаринотерапией. Очень важным лечебным и одновременно диагностическим звеном в лечении является а н г и о п у л ь м о н о граф и я и реканализация (разрушение) эмбола катетером с целью улучшения кровотока в соответствующей артерии. Противошоковые мероприятия должны быть дополнены введением стероидных гормонов (преднизолон, гидрокортизон и др.). Все лекарственные вещества вводят внутривенно вместе с растворами полиглюкина, реополиглюкина, глюкозо-новокаиновой смесью. При массивной эмболии, протекающей на фоне тяжелого шока, возможно о п е рат и в н ое удаление эмбола — эмболэктомия (при неэффективности противошоковой терапии и наличии противопоказаний к тромболитической терапии). Эмболэктомия (в том числе в условиях применения искусственного кровообращения) сопровождается высокой летальностью. Менее опасным является эндоваскулярное удаление эмбола специальными отсасывающими тромбы катетерами. При рецидивирующей хронической эмболии легочной артерии показано лечение антикоагулянтами непрямого действия, а в случае возникновения микроэмболии повторно — имплантация в нижнюю полую вену кава-фильтра, задерживающего эмболы. Прогноз. При I и II степени эмболии и адекватном лечении прогноз благоприятный, при III и особенно IV степени летальность крайне высокая, так как адекватная помощь, как правило, запаздывает. У некоторых больных полного расплавления тромбов не происходит, сохраняется остаточная обтурация артерий малого круга кровообращения. У этих больных спустя месяцы или даже годы после эпизода тромбоэмболии легочной артерии появляются одышка и "необъяснимая" легочная гипертензия с явлениями пра-вожелудочковой недостаточности. Глава 20 ЛИМФАТИЧЕСКИЕ СОСУДЫ КОНЕЧНОСТЕЙ Начальным звеном лимфатических сосудов являются лимфатические капилляры. Различают поверхностные и глубокие лимфатические сосуды. Первые собирают лимфу из кожи и подкожной клетчатки, вторые — из подлежащих тканей. Поверхностные лимфатические сосуды верхней конечности расположены по ходу подкожных вен, глубокие — по ходу магистральных артерий и вен. Первые вливаются в лимфатические узлы локтевого сгиба и подмышечные лимфатические узлы, вторые — в подмышечные лимфатические узлы. Поверхностные лимфатические сосуды нижней конечности следуют по ходу большой и малой подкожных вен и несут лимфу в основном в поверхностные и глубокие паховые лимфатические узлы. Глубокие лимфатические узлы располагаются по ходу магистральных сосудов голени и бедра, впадают в подколенные и глубокие паховые узлы. Через сеть лимфатических сплетений лимфа из глубоких лимфатических узлов попадает в поясничные лимфатические узлы, образующие правый и левый лимфатические стволы. Последние несколько выше сливаются вместе и образуют с лимфатическими сосудами брюшной полости грудной лимфатический проток. Лимфатические сосуды имеют адвентицию, мышечный слой представлен мышечными элементами, способными сокращаться и продвигать лимфу в проксимальном направлении. Интима очень тонкая, снабжена клапанами. Лимфатические, сосуды имеют симпатическую иннервацию, способны стимулировать сокращения, а при неблагоприятных условиях спазмиро-ваться. Интерстициальная жидкость, богатая белками, возвращается в лимфатические капилляры и лимфатические сосуды. Лимфатические узлы паховой и подмышечной областей представляют первый иммунологический барьер, осуществляют фильтрационную функцию. В лимфатических капиллярах давление очень низкое (0—3 мм водн. ст.). В крупных лимфатических сосудах, благодаря наличию клапанов и продвижению лимфы в центростремительном направлении, давление повышается до 20 мм водн. ст. Дата добавления: 2015-01-18 | Просмотры: 876 | Нарушение авторских прав |