|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
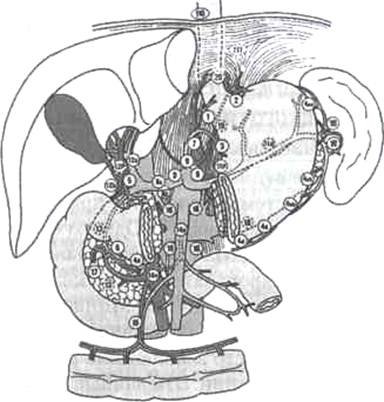
Тактика хирургического леченияХирургический метод остается «золотым» стандартом радикального лечения злокачественных опухолей желудочно-кишечного тракта, позволяющим надеяться на полное выздоровление. Традиционно, радикальные операции по поводу рака включали обязательное моноблочное удаление регионарных лимфатических узлов. Впервые такой подход был предложен более 100 лет назад Holsted-oм при хирургическом лечении рака молочной железы. С тех пор это положение определяет стратегию онкохирургии в целом и тактику хирургического лечения рака желудочно-кишечного тракта различных локализаций в частности. Атлас по хирургической анатомии лимфатической системы желудка и прилежащих органов был опубликован в 1936 году японским исследователем Inoue Y. Однако в клинической практике эти данные нашли применение существенно позже. Впервые концепция агрессивной тактики в хирургии рака желудка была сформулирована американским хирургом Wangesteen О.Н. Анализируя результаты выживаемости в клинике Миннесотского Университета в 30 - 40 годы, автор отметил отсутствие пациентов, переживших 5 лет наблюдения после хирургического лечения. Причем наиболее часто заболевание рецидивировало в регионарных лимфатических коллекторах, в зоне операции. Эти данные послужили стимулом к активизации тактики хирургического лечения с обязательным удалением регионарных лимфатических узлов. Столь агрессивная тактика, проповедуемая автором на протяжении 3 десятилетий, стала основой улучшения отдаленных результатов: 5-летняя выживаемость в клинике возросла до 17 %. Позднее концепция расширенной лимфаденэктомии, как стандартного элемента радикального хирургического лечения рака желудка, широко проповедовалось ведущими хирургами-онкологами из Memorial Sloan Kettering Cancer Center (New-York) - McNeer G., Pack Т., Sunderland D. Авторы отработали технические аспекты выполнения расширенных вмешательств при раке желудка со стандартным удалением забрюшинных лимфатических узлов чревного ствола и его ветвей. Понятие превентивной расширенной лимфодиссекции было впервые введено при хирургическом лечении рака желудка для обозначения операций, сопровождавшихся плановым удалением пораженного органа и зон регионарного метастазирования. На сегодняшний день в литературе широко применяются два термина, отражающие характер выполняемых вмешательств с учетом лимфатической системы желудка. Следует акцентировать внимание, что термин «лимфодиссекция», являясь более емким, нежели термин «лимфаденэктомия», включает моноблочное удаление не только лимфатических узлов, но и всего лимфатического аппарата (лимфатических сосудов и окружающей жировой клетчаткой) в пределах фасциальных футляров. Именно это положение, обоснованное временем и опытом, является теоретической предпосылкой возможности выполнения радикальной операции при раке желудка, путем удаления первичного очага с зонами возможного регионарного лимфогенного метастазирования. Причем первое положение - улучшение локального контроля со снижением возможности местного рецидива, также заключает в себе и другую предпосылку - возможность определения распространенности процесса. В литературе опубликованы результаты нескольких проспективных рандомизированных исследований, позволяющих полноценно оценить значимость расширенного объема лимфодиссекции в хирургическом лечении рака желудка. Поэтому большинство хирургов-онкологов в практической работе ориентируются на характеристики рака желудка - раннее лимфогенное метастазирование с высокой частотой поражения регионарных лимфатических узлов уже при прорастании подслизистого слоя - более 15 %, собственный опыт и традиции отечественных хирургов-онкологов, а также опыт ведущих клиник мира. Концепция превентивного моноблочного удаления зон регионарного метастазирования вместе с первичным очагом при раке желудка связана с именем японского хирурга Jinnai (1962), который на основании своих результатов рассматривал такой объем вмешательства как радикальный. С этого момента расширенная радикальная лимфодиссекция как обязательный интегрированный этап операции стала общепризнанной доктриной хирургического лечения рака желудка в Японии. В настоящее время, на основании работ Japanese Gastric Cancer Association (JGCA, 1998) детально описаны 16 групп регионарных лимфатических узлов (рис.2), формирующих три последовательные (не в истинном понимании последовательности) этапа метастазирования от различных отделов желудка - с N1 до N3: • Первый этап: перигастральные лимфоколлекторы, расположенные в связочном аппарате желудка (№№1-6), • Второй этап: забрюшинные лимфатические узлы, расположенные по ходу ветвей чревного ствола (лимфатические узлы по ходу левой желудочной артерии (№7), общей печеночной артерии (№8а+р), чревного ствола (№9), в воротах селезенки (№10), по ходу селезеночной артерии (№11 p+d)).
Рис. 2. Схема регионарных лимфатических узлов желудка Japanese Gastric Cancer Association, 1998).
• Третий этап: лимфатические узлы гепатодуоденальной связки (№12а+р+Ь), ретро-панкреатодуоденальные (№13), лимфатические узлы по ходу верхней брыжеечной артерии (№14a+v), в корне брыжейки поперечно-ободочной кишки по ходу средней ободочной артерии (№15), парааортальные лимфоузлы, расположенные на различном уровне брюшной аорты (№16а1-а2, Ь1-Ь2), а также хиатальные и заднемедиастинальные лимфоколлекторы для рака проксимального отдела желудка с переходом на пищевод. Следует отметить, что для различных локализаций первичной опухоли в желудке лимфатические узлы, даже в пределах одной группы, могут относиться к различным этапам метастазирования, что определяется эмпирически, на основании исследования отдаленных результатов хирургического лечения. На основании классификации и с учетом исследований по результатам выживаемости вовлечение лимфатических коллекторов N, - ^рассматривается как регионарное метастазирование, тогда как вовлечение лимфоузлов N3 - как распространенность, соответствующая четвертой стадии заболевания. Различные варианты лимфодиссекции нашли свое отражение в классификации объема вмешательства. Согласно этой классификации вариант лимфодиссекции классифицируется на основании последнего удаляемого этапа метастазирования (Табл. 4).
Таблица 4. Тип хирургического вмешательства
На сегодняшний день данная классификация степени радикальности выполняемой лимфодиссекции применима лишь для Японских и нескольких специализированных Европейских и Американских клиник, так как в большинстве публикаций лимфодиссекция D2 уже рассматривается как расширенная. Впервые сравнительный анализ результатов расширения объема лимфодиссекции на ретроспективном материале был выполнен Mine с соавт. (1970): авторы исследования отметили улучшение отдаленных результатов при выполнении расширенной лимфодиссекции, особенно при выявлении лимфогенных метастазов - 21 % после лимфодиссекции D2-D3 против 10 % после ограниченной диссекции D 0-D1. В подобном исследовании, выполненном Y. Kodama с соавторами (1981) десятилетием позднее, авторы также отмечают улучшение отдаленных результатов при сравнении расширенных операций D2-D3 со стандартным (ограниченным) объемом лимфодиссекции В0-О1(Табл. 5). По данным одного из ведущих специалистов по вопросам расширенной лимфодиссекции профессора Keiichi Maruyama (1993), к началу 90-х годов отработка методологических приемов выполнения расширенной лимфодиссекции позволила значительно улучшить отдаленные результаты лечения. Таблица 5. Анализ 5-летней выживаемости в зависимости от объема лимфодиссекции
Несмотря на расширение объема вмешательства и увеличение резектабельности до 95 %, отмечено стабильное снижение послеоперационной летальности до 0,4 %. На Ежегодном Конгрессе JRSGC в 1992 году были проанализированы отдаленные результаты лечения более 61 тысячи больных раком желудка, получавших хирургическое лечение в 98 институтах страны (Sawai К. et al., 1994). Отдаленные результаты проанализированы по стадиям заболевания. Анализ результатов продемонстрировал, что: • при I стадии без метастазов в лимфатические узлы наиболее хорошие результаты отмечены в группе стандартных D2 и расширенных D3 радикальных гастрэктомий (соответственно по 92,4 %), однако также возможно выполнение радикальной резекции (88,1 %). При выполнении стандартной гастрэктомий D1 отмечена наиболее низкая 5-л.в. - 74,0 %, • при II стадии достоверно лучшие результаты 5-л.в. отмечены при выполнении стандартной и расширенной радикальной лимфодиссекции (соответственно 76,8 % и 75,9 %), чем при выполнении стандартной гастрэктомий (52,5 % и 66,1 % соответственно), • при III стадии более чем двукратное достоверное улучшение 5-л.в. отмечено после стандартных и расширенных радикальных операций (45,7 % и 47,7 % соответственно), чем после стандартных вмешательств (24,6 %), • при III стадии наиболее хорошие отдаленные результаты отмечены после выполнения расширенных радикальных гастрэктомий D3 (РРГ). По данным Sawai К. и соавторов (1994) 5-л.в. после выполнения РРГ при метастазах в ^составляет 41,8 %, что значительно лучше, чем при выполнении СРГ 21,2 % (разница статистически достоверна: р<0,05). С учетом накопленного опыта ведущих клиник, занимающихся проблемой хирургического лечения рака желудка, в плане значительного улучшения отдаленных результатов лечения при удовлетворительных непосредственных результатах в Японии объем лимфодиссекции D2 считается стандартным. Несмотря на значительные успехи развития хирургического лечения рака желудка в Японии, Европейские и Американские хирургические школы к началу 90-х годов находились лишь на этапе отработки идеологии и методологии расширенных операций. Однако последовательность в работах Японских исследователей, отсутствие достоверного улучшения отдаленных результатов при использовании различных вариантов комбинированного лечения с неоадъювантной и адъювантной химиотерапией явились промоторами для активизации хирургической тактики лечения рака желудка. Результаты рандомизированных исследований Dent DM и соавторов (1988), а также Robertson SC и соавторов (1994) из-за маленьких сравнительных групп пациентов, высокой частоты непосредственных осложнений и летальности, а также некоторых статистических неточностей не могут претендовать на достоверность выполненного анализа. Так, по данным Robertson, в группе расширенных операций в 50 % случаев выявлен поддиафрагмальный абсцесс в ложе удаленной селезенки, у 10 % выявлена несостоятельность пищеводных соустий. Послеоперационные осложнения потребовали в 20 % выполнения экстренных релапаротомий. На наш взгляд, в обоих исследованиях не корректно определены показания для выполнения расширенных операций, а количество удаленных лимфатических узлов по группам не совсем соответствует критериям расширенной лимфодиссекции. На II-м Международном Конгрессе по Раку Желудка (Munich, Germany, 1997) были опубликованы результаты проспективного рандомизированного многоцентрового исследования, проведенного Голландской Группой по Изучению Рака Желудка (Bonenkamp JJ. et al., 1997). Целью исследования был сравнительный анализ стандартных D0-D1 и расширенных D2 операций по непосредственным и отдаленным результатам. Исследование включало репрезентативную выборку 711 пациентов - 380 выполнены стандартные, а 331 расширенные вмешательства. Статистический анализ материалов исследования показал, что расширенные операции сопровождаются значительным увеличением непосредственных осложнений (43 % против 25 %) и летальности (10 % против 4 %). Анализ 3-летних результатов не продемонстрировал увеличения выживаемости в группе расширенных операций - 60 % D1 против 55 % D2. Подробный анализ материалов рандомизированного исследования Голландской группы по изучению рака желудка был представлен на III Международном конгрессе по раку желудка (Seoul, Korea, 1999) в обзорной лекции, сделанной руководителем отделения абдоминальной онкологии Национального Института Рака (Tokyo, Japan), профессором Mitsuru Sasako(1999) (Он являлся суправизором исследований Голландской Группы). По мнению М. Sasako, основными недостатками представленных исследований, несмотря на очень хорошую организацию и подробный статистический анализ, не позволяющими рассматривать данные исследования как достоверные, являются: 1. Большое количество участвующих в исследовании клиник (многоцентровое исследование), что обуславливает большое количество участвующих в протоколе хирургов, и, как следствие, снижение индивидуального опыта каждого отдельного хирурга (по данным автора, некоторые хирурги выполняли не более 5 расширенных операций в год, что является неадекватным). 2. Отсутствие индивидуальной специализации некоторых хирургов, участвующих в протоколе, по проблеме расширенных операций при раке желудка. Этот фактор несет в себе несколько негативных последствий и, в первую очередь, ухудшение непосредственных результатов за счет увеличения хирургических осложнений, частоты повторных операций и летальности в группах расширенных операций. Во многом это обусловлено отсутствием стандартизации выполняемых вмешательств. Так в качестве одного из отрицательных факторов М. Sasako приводил такую деталь, как использование сшивающих аппаратов во всех случаях формирования пищеводных анастомозов, несмотря на индивидуальные особенности. Это обусловлено отсутствием опыта формирования ручного шва пищеводного соустья. 3. Снижение истинной радикальности вмешательств, в связи со снижением количества удаляемых лимфоколлекторов и, как следствие, повышение вероятности оставления метастатически измененных узлов и ранний рецидив заболевания. По данным Bunt AMG и соавторов (1995, 1996), в Голландском протоколе среднее количество удаляемых при расширенных вмешательствах лимфоколлекторов первого этапа метастазирования (N1) составляло 13, а второго этапа (N2) 11 узлов. В противоположность этому количеству суправизирующим хирургом (Sasako M.) при расширенных операциях в среднем удалялось 35 узлов первого (N,) и 25 узлов второго (N2) этапов метастазирования. 4. Отсутствие в некоторых вмешательствах стандартизации выполняемой процедуры: так, не у всех больных с экстирпациями желудка выполнялась спленэктомия, что можно рассматривать либо как некоторое отступление от Японской методологии расширенной гастрэктомий D2, либо как включение в эту группу органосохраняющих расширенных операций D2. В первом случае такое отступление неизбежно может отразиться на отдаленных результатах лечения, а во втором случае повлияет на статистический анализ в результате объединения пациентов различных групп. Последнее положение об отсутствии гомогенности в анализируемых группах в Голландском протоколе косвенно подтверждается последующими данными о выживаемости, опубликованными вначале на III (Seoul, Korea, 1999), а затем и на IV (New-York, USA, 2001) Международных Конгрессах по Раку Желудка. Так по материалам Hartgrink H. (2001), основанных на материалах Голландского протокола, отмечается улучшение отдаленных результатов лечения в группе с D2 лимфодиссекцией при наличии метастазов в лимфоколлекторы первого этапа метастазирования (N1), то есть при II и Ша стадиях. Причем достоверно лучшие отдаленные результаты лечения были получены в группе пациентов с сохранением поджелудочной железы и селезенки, т.е. при выполнении органосохранных вмешательств с лимфодиссекцией D2. Таким образом, становится очевидным, что отсутствие улучшения отдаленных результатов в группе расширенных операций во многом объясняется небольшим опытом, а также техническими и тактическими упущениями. На IV Международном конгрессе по раку желудка (New-York, USA, 2001) на Консенсусной конференции, посвященной проблеме расширенной лимфодиссекции при хирургическом лечении рака желудка, большинство участников отмечало улучшение результатов за счет снижения частоты локорегионарного рецидива заболевания и увеличения пятилетней выживаемости. В заключении председатель Консенсусной Конференции профессор Brennan M.F. (Президент Конгресса) отметил, что при отработке методики в специализированных центрах непосредственные результаты сопоставимы с результатами стандартных вмешательств, а отдаленные результаты приближаются к данным Японской Ассоциации по Раку Желудка (JGCA). С учетом накопленного опыта лимфодиссекция D2 является достаточно безопасной процедурой и должна стать обязательным элементом хирургического лечения рака желудка.
Дата добавления: 2015-02-06 | Просмотры: 816 | Нарушение авторских прав |