|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
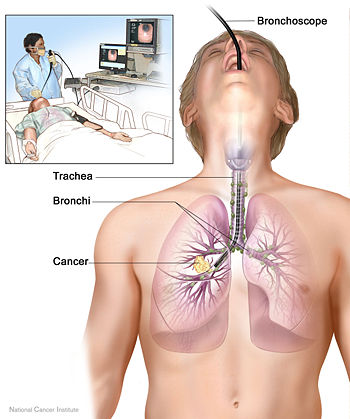
III. Верхушечный рак ПанкостаВерхушечный рак Панкостасопровождается формированием округлого образования в области верхушки легкого, плевральных изменений, деструкции верхних ребер и соответствующих позвонков. Говорить о раке Панкоста можно лишь в случае, когда он имеет истинно бронхогенное происхождение. Рентгенологическая диагностика вовлечения с процесс средостенных лимфоузлов значительно повышается при применении контрастирования пищевода. Однако, как правило, одного этого метода бывает недостаточно. Многочисленные исследования показали, что рентгенография грудной клетки мало чувствительна для выявления метастазов в медиастинальных лимфатических узлах, определения прорастания опухоли в грудную стенку или органы средостения. Бронхологическое обследование. Проведение бронхофиброскопии (БФС) рекомендовано всем больным для выявления как центральных, так и периферических поражений легких (рис. 15).
Рис. 15. Схема проведения бронхоскопии.
С точки зрения принципов диагностики, БФС играет двойную роль в обследовании больных с подозрением на рак легкого: морфологическая верификация диагноза и определение местного распространения опухоли (рис. 16).
Процент осложнений в результате применения БФС для диагностики рака легкого крайне низок (менее 2%) и включает пневмоторакс и значительные кровоизлияния (более 50 мл). Слабые кровотечения встречаются часто и обычно не дают последствий. Трансторакальная пункция. Наличие выпота в плевральной полости при имеющейся опухоли легкого или подозрении на нее, особенно при периферической локализации, является показанием для проведения плевральной пункции с забором пунктата на цитологическое исследование. В большинстве случаев при периферическом положении опухоли удается провести иглу непосредственно в опухолевый узел для забора биоптата. Основное назначение трансторакальной пункции периферической опухоли любого генеза заключается в заборе аспирационного материала (пункционная биопсия) для цитологического (при тонкоигольной пункции обычными длинными иглами) или гистологического (при толстоигольной пункции специальными иглами) исследования (рис. 17).
Трансторакальная пункция значительно повышает специфичность других методов исследования, прежде всего лучевых. Эффективность метода значительно повышается при проведении иглы строго в опухолевый узел под рентгенологическим контролем. Из всех методов компьютерной томографии для этой цели может использоваться только рентгеновская (РКТ) (рис. 18).
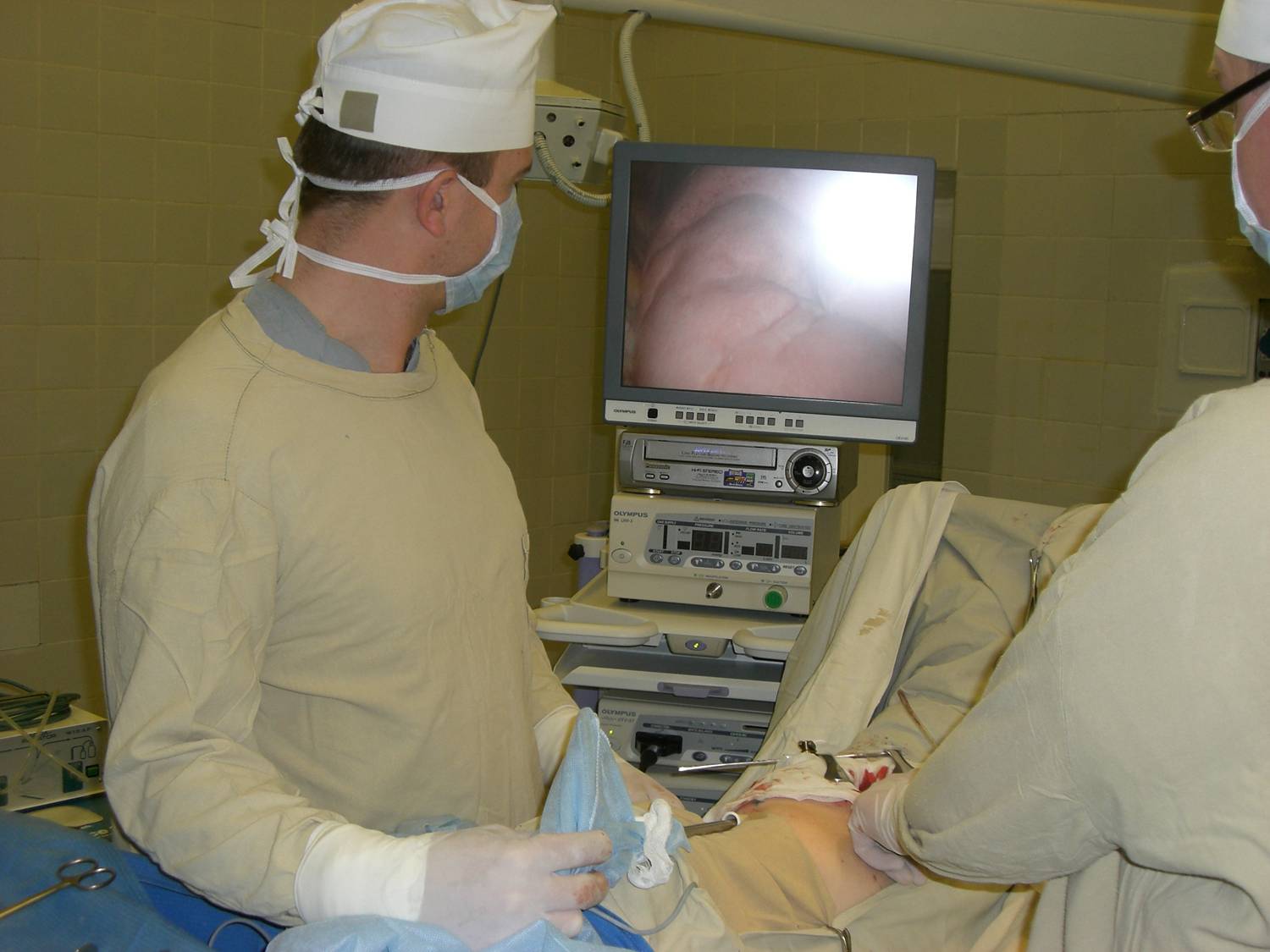
Особенно этому способствует внедрение методики РКТ во флюороскопическом режиме, что позволяет выполнять манипуляцию в реальном режиме времени. Показаниями этого исследования являются: 1) округлые образования в любой зоне легкого, особенно в плаще; 2) подозрение на метастаз в легком; 3) множественные внутрилегочные шаровидные тени. Противопоказания: 1) единственное легкое; 2) нарушения в системе гемостаза; 3) подозрение на эхинококкоз; 4) выраженная сердечно-легочная недостаточность; 5) легочная гипертензия. Морфологическое подтверждение периферического рака легкого составляет в среднем 83%, причем из прикорневой зоны этот показатель находится на уровне 62%, из средней - 79%, плащевой - 88%. Степень дифференцировки опухолевых клеток удается установить в 40% случаев. Наиболее часто встречающимся осложнением после ТТП является пневмоторакс, который возникает у 25-30% пациентов, при этом в 5-10% случаев требуется дренирование плевральной полости. Другими осложнениями могут быть внутрилегочные гематомы и реже - тяжелые кровоизлияния, воздушная эмболия и диссеминация опухоли по пути иглы. Описаны редкие случаи летальных осложнений. Видеоторакоскопическая биопсия. Данный метод диагностики (рис. 19) показан больным с солитарными затемнениями в легких, когда совокупность вышеизложенных методов верификации опухоли не позволяет полностью исключить или подтвердить рак легкого.
Рис. 19. Момент выполнения видеоторакоскопической биопсии.
Удельный вес видеоторакоскопии среди всех оперативных вмешательств по поводу рака составляет 9%. В данном случае, несмотря на кажущуюся сомнительность показаний, видеоторакоскопия абсолютно показана для своевременной диагностики рака легкого, т.к. выполнение ее менее опасно, чем пропустить рак. В случае выполнения видеоторакоскопии у каждого второго больного выявляют рак легкого I-II стадии, что дает возможность выполнить органосохраняющие операции у 90% пациентов. С целью морфологической верификации опухоли во время видеоторакоскопии производят пункционную или бранш-биопсию узла, в некоторых случаях выполняют плоскостную, клиновидную или сегментарную резекцию новообразования с выполнением интраоперационного экспресс-гистологического исследования с последующим дополнительным гистологическим исследованием взятого препарата. Медиастиноскопия. Это инвазивное оперативное эндоскопическое исследование, при котором вскрывается и осматривается средостенье с целью получения морфологического материала из медиастинальных структур (в большинстве случаев проводят биопсию лимфоузлов) (рис. 20, 21).
Рис. 20. Создание тоннеля в средостенье. Современный медиастиноскоп.
Оценка плеврального выпота при немелкоклеточном раке легких. Около 1/3 пациентов, страдающих НМРЛ, имеет в момент диагностики плевральный выпот. Наличие плеврального выпота у больного раком легких чаще всего свидетельствует о плевральных метастазах, однако в 30-40% случаев экссудат может быть также вследствие парапневмонического процесса и других заболеваний. Поэтому доказательство злокачественности необходимо, так как от этого может зависеть тактика лечения. Первичным методом оценки плеврального содержимого является торакоцентез с цитологическим исследованием 50-100 мл жидкости, что позволяет поставить диагноз приблизительно у 65% пациентов с выпотом злокачественной природы. Поскольку повторное цитологическое исследование плевральной жидкости увеличивает вероятность выявления опухолевых клеток, целесообразно в случае первичного негативного заключения повторить процедуру. Если после торакоцентеза не получено подтверждения злокачественной природы поражения, но клинические подозрения сохраняются, то на следующем этапе целесообразной представляется торакоскопия. При торакоскопиидиафрагмальная, висцеральная и медиастинальная плевра легко доступна для осмотра и прицельной биопсии. Дополнительным преимуществом является возможность определить степень поражения внутригрудных лимфатических узлов или прорастание других медиастинальных органов и структур, которые могли бы помешать успешной резекции и излечению. Лабораторные методы диагностики. Всем пациентам следует выполнять полный клинический и биохимический анализы крови, которые включают в себя определение электролитов, щелочной фосфатазы, альбумина, трансаминаз, общего билирубина и креатинина. В диагностике рака лёгкого используются опухолевые маркеры - сложные белки с углеводным или липидным компонентом, которые синтезируется в большом количестве злокачественными клетками. В настоящее время в клинической практике применяется 5-7 маркеров для диагностики: 1) мелкоклеточного рака легкого а) нейроспецифическая энолаза (NSE), б) раково-эмбриональный антиген (РЭА); 2) плоскоклеточного рака легкого а) цитокератиновый фрагмент (CYFRA 21-1), б) маркер плоскоклеточного рака - гликопротеин (SCC), в) раково-эмбриональный антиген (РЭА); 3) аденокарциномы легкого а) раково-эмбриональный антиген (РЭА), б) цитокератиновый фрагмент (CYFRA 21-1), в) полипептидный антиген (СА 125); 4) крупноклеточного рака легкого а) цитокератиновый фрагмент (CYFRA 21-1), б) маркер плоскоклеточного рака (SCC), в) раково-эмбриональный антиген (РЭА). Методологияиспользования маркеров заключается в следующем: 1) у больного с морфологически верифицированным диагнозом рака легкого до начала лечения определяют уровень маркеров, концентрация которых повышена; 2) через 3 недели после операции вновь определяют уровень маркеров, который был повышен до операции, сохранение высокой концентрации даже одного маркера свидетельствует о нерадикальности оперативного лечения; 3) в дальнейшем, если больному не проводят дополнительное лечение, каждые 4-6 месяцев определяют уровень маркеров, который был повышен до лечения, повышение уровня свидетельствует о рецидиве заболевания, причем оно опережает на 3-6 месяцев его клинические проявления; 4) при консервативной противоопухолевой терапии уровень маркеров определяют до лечения и спустя 2 недели после окончания каждого курса, для контроля её эффективности. К сожалению, ни один из исследовавшихся опухолевых маркеров не показал достаточной чувствительности и специфичности для того, чтобы дать возможность надежного выявления скрытого заболевания или контроля эффективности лечения. По этой причине рутинные измерения онкомаркеров при скрининге, определении стадии или оценке развития заболевания в настоящее время не рекомендованы. Морфологический диагноз. Достоверность результата может зависеть от количества и качества жизнеспособных клеток в пробе. Диагноз может быть поставлен на основании цитологических проб либо хирургических биопсий.Цитологическое исследование мокроты является одной из самых доступных процедур. Возможность точного установления диагноза повышается при использовании произвольно откашлянных образцов и исследовании многих (по крайней мере трех), а не единичных проб.Гистологические биопсийные пробы могут быть получены с помощью эндобронхиальной, трансбронхиальной, трансторакальной биопсии или открытых процедур, таких как инцизионная клиновидная биопсия, торакоскопическая биопсия. Дата добавления: 2015-02-05 | Просмотры: 2112 | Нарушение авторских прав |