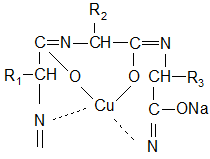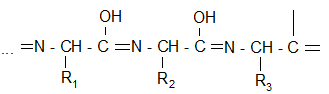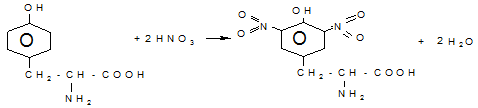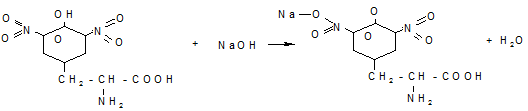|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Лабораторный практикум
Тема: α-АМИНОКИСЛОТЫ, пептиды, белки. Цель: 1. Изучить химические свойства аминокислот. 2. Научиться с помощью качественных реакций определять – аминогруппу, ароматические аминокислоты, пептидные связи, белки. Техника безопасности: 1. С концентрированными кислотами и щелочами работать осторожно, под вытяжным шкафом, в очках. 2. С раствором нингидрина работу проводить под вытяжным шкафом, вдали от огня. Нингидрин не должен попадать на кожу.
Ход работы:
ОIIЫТ №1. Амфотерные свойства аминокислот. А) В пробирку поместите 5 капель 1% раствора α-аланина или аминокислоты и добавьте по каплям 9,1% хлороводородной кислоты подкрашенной индикаторам конго в синий цвет до появления розово-красной окраски. Напишите уравнение реакций и объясните изменение окраски. Б) В пробирку поместите 5 капель 1% р-ра аминокислоты м по каплям добавьте 0,1% раствор гиидроксида натрия, подкрашенного фенолфталеином до исчезновения окраски. Объясните происходящее явление и напишите реакции.
ОПЫТ №2. Реакция глицина с азотистой кислотой. В пробирку поместите 5 капель 1% раствора глицина и равный объем 5% раствора нитрата натрия. Добавьте 2 капли конц. уксусной кислоты и осторожно взболтайте смесь. Наблюдается выделение газа: реакция используется для качественного определения аминогрупп в аминокислотах. Напишите схему взаимодействия глицина с азотной кислотой.
ОПЫТ №3. Нингидриновая реакция на аминогруппу в α – положении. Растворы α – аминокислот при нагревании с нингидрином дают сине-фиолетовое окрашивание. В этой реакции α – аминокислоты окисляются нингидрином, подвергаясь при этом окислительному дезаминированию и деркабоксилированию.
Нингидрин α – аминокислота альдегид нингидрин (восст.)
Восстановленный нингидрин конденсируется с другой молекулой нингидрина в окисленной форме, образуя окрашенный продукт конденсации.
В пробирку поместите 4 капли 1% раствора глицина и 0,1% раствора нингидрина. Содержимое пробирки осторожно нагреть до появления сине-красного цвета.
ОПЫТ №4. Биуретовая реакция на пептидные связи. В щелочной среде при добавлении к раствору белка гидрата окиси меди образуется комплексное (хелатное) соединение розово-фиолетового цвета. Такую реакцию дают белки, некоторые аминокислоты, пептиды, биурет, средние пептиды.
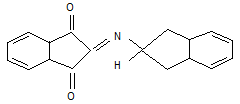
Кетонная форма полипептида
Биуретовый комплекс Енольная форма
В пробирку поместите 5-6 капель белка, добавьте равный объем, 30% раствора NaOH и по стенке добавьте 1-2 капли раствора сульфата меди. Наблюдается появление красно—фиолетового окрашивания.
ОПЫТ №5 Ксантопротеиновая реакция на ароматические аминокислоты Ксантопротеиновая реакция на ароматические аминокислоты - реакция нитрования бензольного ядра циклических аминокислот концентрированной азотной кислотой.
Диноитротирозин (желтый)
В результате образуется нитропроизводные аминокислот, имеющие желтую окраску. В щелочной среде нитропроизводные образуют соли хиноидной структуры. окрашенные в оранжевый цвет (ксантиновый)
Натриевая соль динитротирозина (оранжевый)
В белке содержится достаточное колнчесво ароматических аминокислот, поэтому ксантопротеиновая реакция применяется и для определения белков. В пробирку поместите 10 капель раствора тирозина и 2 капли конц. азотной кислоты. Содержимое пробирки осторожно нагрейте до растворенья осадка. Образуется раствор лимонно-желтого цвета. Охладив пробирку осторожно добавьте 1-3 капли 10% раствора гидроксида натрия до появления ярко—оранжевого цвета. Написать уравнения реакции.
ГЛАВА 9. УГЛЕВОДЫ. Вопросы к занятию.
1. Общая характеристика и классификация углеводов. 2. Моносахариды, их стереоизомерия (D и L-ряды). 3. Цикло-оксотаутометрия. Формулы Хеуроса, мутаротация. 4. Химические свойства моносахаридов: реакции по >C=О, ОН-связи. 5. Глюкозидный гидрооксил. Пентозы (ксилоза, рибоза) и гексоза (глюкоза, фруктоза, галактоза). 6. Олигосахариды,. Дисахариды: лактоза, сахароза(строение, состав, циклооксотаутометрия). 7. Восстанавливающие и не восстанавливающие дисахариды. Виды О-гликозидной связи. 8. Полисахариды: крахмал, гликоген, целлюлоза, декстрины. 9. Гетерополисахариды и их роль в биологии и медицине.
Дата добавления: 2015-02-06 | Просмотры: 1448 | Нарушение авторских прав |
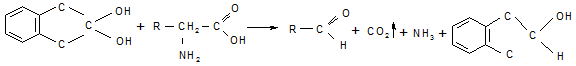
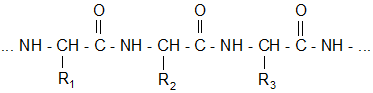 Впервые данный комплекс получен Биуретом (NH2CONHCONH2). Отсюда и название – биуретовая реакция. Схематично реакцию Cu(OH)2 пептидами можно представить так:
Впервые данный комплекс получен Биуретом (NH2CONHCONH2). Отсюда и название – биуретовая реакция. Схематично реакцию Cu(OH)2 пептидами можно представить так: