|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
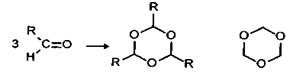
Реакции полимеризацииПолимеризация характерна только для простейших альдегидов и кетонов (формальдегид, ацетальдегид, ацетон). Формальдегид и ацетальдегид легко вступают в реакцию тримеризации:
R = H, CH 3 триоксиметилен Продукт тримеризации формальдегида - триоксиметилен - был открыт А. М. Бутлеровым. Триоксиметилен, так же как и тример ацетальдегида - паральдегид, деполимеризуется при нагревании. При нагревании с минеральными кислотами полимеры альдегидов распадаются на исходные продукты.
Образование полимеров можно рассматривать как результат нуклеофильной атаки атомом кислорода одной молекулы альдегида карбонильного атома углерода другой молекулы. Так, при стоянии 40%-го водного раствора формальдегида, называемого формалином, в виде белого осадка образуется полимер формальдегида — параформ. формальдегид параформ (n = 7 – 100) Реакции конденсации. Наличие в молекуле альдегида или кетона слабого СН-кислотного центра приводит к тому, что α-водородные атомы этих карбонильных соединений обладают некоторой протонной подвижностью.
альдегид (R=H) или кетон
В частности, под действием оснований такие протоны могут отщепляться с образованием соответствующих карбанионов. Последние играют роль нуклеофилов по отношению к карбонильным субстратам. Таким образом, оказываются возможными реакции, в которых одна молекула карбонильного соединения (метиленовая компонента) присоединяется к карбонильной группе другого карбонильного соединения (карбонильная компонента). Такие процессы относятся к реакциям конденсации. Конденсацией называется реакция, приводящая к усложнению углеродного скелета и возникновению новой углеродной связи, причем из двух или более относительно простых молекул образуется новая, более сложная молекула. Иногда в результате реакции конденсации выделяется молекула воды или другого вещества. In vitro реакции конденсации альдегидов и кетонов проходят в присутствии каталитических количеств кислот или щелочей. Так, ацетальдегид на холоду при действии разбавленных растворов щелочей превращается в альдоль; при проведении реакции в более жестких условиях альдоль дегидратируется с образованием кротонового альдегида.
уксусный альдегид альдоль кротоновый альдегид (3-гидроксибутаналь) (бутен-2-аль)
Поэтому конденсацию альдегидов или кетонов, протекающую по первому типу, называют альдольной конденсацией, или альдолъным присоединением, а по второму типу — кротоновой конденсацией. Использование в качестве катализаторов кислот и проведение реакции в более жестких условиях способствуют образованию продуктов кротоновой конденсации. Некоторые примеры реакций альдольного присоединения приведены ниже.
пропионовый альдегид пропионовый альдегид 3-гидрокси-2-метил- (карбонильная компонента) (метиленовая компонента) пентаналь, 60%
формальдегид 3-метилпропаналь 3-гидрокси-2,2-диметил- (карбонильная компонента) (метиленовая компонента) пропаналь, 50%
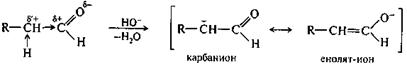
Реакции альдольного присоединения обратимы. Обратный процесс называется альдольным расщеплением (ретроальдольный распад). В условиях организма осуществляются оба процесса, например, альдольная конденсация пировиноградной кислоты и N -ацетил-D-маннозамина с получением нейраминовой кислоты (см. 13.1.4); сшивание цепей тропоколлагена с образованием коллагена (см. 12.3); альдольное расщепление серина на глицин и формальдегид (см. 12.1.5) и 1,6-дифосфата D-фруктозы на фосфат дигидроксиацетона и 3-фосфат D-глицеринового альдегида (см. 13.1.5). Рассмотрим механизм альдольной конденсации в щелочной среде. На первой стадии реакции гидроксид-ион отрывает из α-положения протон, имеющий повышенную подвижность (СН-кислотность) за счет электроноакцепторного влияния карбонильной группы.
Другая причина легкого отщепления протона заключается в образовании карбаниона, стабилизированного путем смещения электронной плотности к кислороду. Этот ион, имеющий мезомерное строение (см. 2.3.1), можно называть и енолят-ионом в соответствии с его второй граничной структурой. Следующая стадия реакции — нуклеофильное присоединение мезомерного иона к карбонильной группе другой молекулы карбонильного соединения с образованием аниона альдоля. Мезомерный ион на этой стадии реагирует по атому углерода, а не по атому кислорода в соответствии с принципом ЖМКО (см. 5.2), так как относительно мягкий электрофильный центр (атом углерода карбонильной группы) предпочтительно связывается с относительно более мягким нуклеофильным центром — атомом углерода мезомерного иона, а не более жестким атомом кислорода.
Анион альдоля, являясь алкоксид-ионом, т. е. более сильным основанием, чем гидроксид-ион, отрывает далее протон от воды.
Важным свойством альдегидов, отличающим их от кетонов, является способность альдегидов чрезвычайно легко окисляться в карбоновые кислоты (см. 9.1.1).
альдегид карбоновая кислота
Дата добавления: 2015-02-06 | Просмотры: 1787 | Нарушение авторских прав |