|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Генез наиболее важных синдромов при ХПН. 1 страница
азотемия — самый точный из общепринятых критериев дефекта азотовы-делительной функции почек — уровень креатинина в сыворотке крови, так как он мало зависит от экстраренальных факторов (голодание, количество белка в пище и др.); электролитные расстройства развиваются в основном в связи с нарушениями функции канальцев, но лишь при уремии отмечается закономерность их нарушений — гипонатриемия, гиперкалиемия, гиперфосфатемия, ги-пермагниемия и гипокальциемия, тогда как в более ранних стадиях ХПН у разных больных могут быть разнонаправленные изменения; ацидоз обусловлен ограничением поступления кислых веществ в мочу, нарушением ацидо- и аммониогенеза канальцами, гиперхлоремией (у больных с наследственными и врожденными, особенно обменными, нефропатиями возможен и алкалоз); анемия — низкий синтез эритропоэтинов в юкстагломерулярном комплексе, угнетение эритропоэза уремическими токсинами, укорочение продолжительности жизни эритроцитов, нарушение белковосинтетической функции печени и дефицит железа, кровопотери с мочой; остеодистрофии — снижение образования в почках 1,25-дигидроксихо-лекальциферола, синтеза кальцитонина, а отсюда низкое всасывание кальция в кишечнике; гипокальциемия и ацидоз, гиперфосфатемия стимулируют активность околощитовидных желез, повышается уровень паратгормона, что, наряду с дефицитом кальцитонина, обеспечивает мобилизацию кальция из кости, остеодистрофию; гипертензия вызвана, с одной стороны, дефицитом синтеза почкой проста-гландинов, гипергидратацией и гиперволемией, задержкой натрия, с другой — гиперпродукцией ренина в юкстагломерулярном аппарате, что при недостатке ингибитора или избытке акцелератора ренина в плазме приводит к образованию комплекса ренина и ангиотензиногена с образованием вначале неактивного вещества ангиотензина I, который под влиянием конвертирующего энзима переходит в вазопрессорное вещество — ангиотензин II. Считают, что гиперфосфатемия и ацидоз развиваются при снижении СКФ менее 30%, а гиперкалиемия — если СКФ менее 10% от нормы, тогда как ги-перкреатининемия — при СКФ менее 50%. Классификация. Классификация ХПН предусматривает выделение 4 стадий: I стадия — компенсированная (полиурическая) — уменьшение резервных возможностей почек (при применении нагрузочных проб) без нарушения го-меостатических констант (impaired renal function — IRF); II стадия — субкомпенсированная — стадия неустойчивой гиперазотемии III стадия — декомпенсированная — стадия отчетливых признаков ХПН (chronic renal failure — CRF); IV стадия — терминальная, уремическая стадия со свойственной ей олиго-анурией, поражением ряда органов и систем (end-stage renal disease). Клиническая картина В I стадии (полиурической) клиника определяется тем заболеванием, которое привело к ХПН (табл.153). Может выявляться никтурия. Третья стадия характеризуется анорексией, нарастающими неврологическими изменениями (апатия, мышечная слабость или мышечные спазмы, чередующиеся с возбуждением, головные боли, ухудшение зрения, судороги, в том числе и как следствие тетании), сухостью и зудом кожи, геморрагиями и некрозами на коже и слизистых оболочках, диспепсией, болями в костях и суставах, деформацией костей, шумным дыханием, нарастающей симптоматикой отека легких и нарушений сердечно-сосудистой деятельности с бради-кардией и гипертензией. В терминальной стадии появляются запах мочевины изо рта, стоматит, фарингит, перикардит и плеврит, отек легких и, наконец, развивается кома.
Таблица 153 Характеристика стадий ХПН и объем основных лечебных мероприятий (Папаян А. В., Архипов В. В., 1997).
Лечение. При ХПН I стадии лечение должно быть направлено на основное заболевание и в связи с недостаточностью функции почек является симптоматическим. В стадии Па назначают диету по типу стола № 36 (количество белка ограничивается до 1,5 г/кг). При высоких цифрах азотемии назначают строгую диету с суточным количеством белка 0,6-0,7 г/кг, но достаточной энергетической ценностью, то есть рацион должен быть обогащен углеводами и жирами. Этим задачам отвечает диета Джиордано—Джиованнетти, из которой полностью исключены мясо, рыба, творог. Для детей 11-14 лете ХПН разработан вариант диеты Джиордано—Джиованнетти: первый завтрак — омлет из 2 желтков, винегрет (200 г), чай (200 г) и безбелковый хлеб (30 г) с маслом (15 г); второй завтрак: пастила (30 г), яблоки печеные (180 г), сок виноградный (100 г); обед —суп фруктовый с рисом (300 г), каша пшеничная с изюмом (200 г), кисель из свежих фруктов (200 г), хлеб безбелковый (40 г) с маслом (10 г); полдник — свежие фрукты (200 г); ужин — картофель жареный, яблоки (210 г), чай с сахаром (200 г), пастила (30 г), хлеб безбелковый (30 г), масло сливочное (15 г). Рекомендуют переводить ребенка на эту диету уже при уровне остаточного азота 30 ммоль/л, то есть в стадии Па ХПН. По мере уменьшения азотемии количество белка в диете увеличивают до 1-1,5 г/кг в сутки. Количество соли в рационе зависит от наличия гипертензии, отеков, суточного диуреза и экскреции натрия (баланс должен быть нулевым), так как ограничение соли в момент полиурии может привести к гипонатриемии. При гипокалиемии в диету вводят продукты, богатые калием (бананы, урюк, изюм, чернослив). Учитывая особенности диеты и болезни, всем больным с ХПН назначают витамины Вс, В(, В2, Е, В6 в дозах, превышающих физиологические потребности в 4 раза. Симптоматическую терапию проводят следующим образом. При ацидозе — ежедневное введение гидрокарбоната натрия (0,5-2 ммоль/кг в сутки). При гипертензии — бессолевая диета, каптоприл (энап), диазоксид, препараты раувольфии, сс-метилдопа, гемитон и другие гипотензивные препараты в сочетании с мочегонными (фуросемид). При остеопатии и гипокальциемии — препараты кальция внутрь в возрастающих дозах (под контролем уровня кальция в сыворотке крови), витамин D (4000-40 000 МЕ/сут) под контролем реакции Сулковича. При анемии — трансфузии эритроцитной массы при уровне гемоглобина ниже 50 г/л, но эффект от них нестойкий. В последние годы доказана эффективность лечения больных анемией при ХПН препаратами эритропоэтина. Регулярный гемодиализ при ХПН у детей необходимо начинать в стадиях III—IV при уровне креатинина в сыворотке крови более 0,528 ммоль/л и клиренсе эндогенного кретинина менее 10 мл/мин на 1,73 м2. Гемодиализ проводят 2-3 раза в неделю по 3,5-4 ч. На фоне регулярных гемодиализов строгих ограничений белка в диете не требуется, но необходимо снижение количества жидкости и менее строгое ограничение натрия. При интеркуррентных заболеваниях, сопровождающих ХПН, возможно резкое ухудшение состояния — почечная недостаточность острого периода (нарастание отеков, анемии, азотемии, резкое ухудшение общего состояния). У таких больных гемодиализ — единственная рациональная тактика. Иногда 1-2 сеансов достаточно для стабилизации клинико-лабораторных данных. Трансплантация почки должна предусматриваться для больных с ХПН, находящихся на регулярном гемодиализе. Имеются данные о больных, у которых уже 20 лет хорошо функционирует трансплантат. Прогноз Зависит от причины ХПН. ХПН в I стадии обратима, если можно активно влиять на ее причину (например, удалить камень при МКБ). Глава 16 БОЛЕЗНИ СИСТЕМЫ КРОВИ.АНЕМИИ. Анемия (anaemia: an — отрицание + греч. haima — кровь; синоним — малокровие) — состояние, характеризующееся снижением содержания гемоглобина в единице объема крови (менее 110 г/л у детей раннего и дошкольного возраста и менее 120 г/л у школьников), чаще при одновременном уменьшении количества эритроцитов (менее 4 х1012/л) и гематокритного показателя (ниже 35%). В англо-американской литературе предлагают считать анемией у детей первых двух лет жизни (по окончании периода новорожденности) снижение гемоглобина менее 100 г/л и гематокритного показателя ниже 31%.
Классификация Существуют разные подходы к классификации анемий, но наибольшее распространение получил патогенетический, предусматривающий разделение анемий по ведущему механизму их возникновения и развития, который и представлен ниже. I. Постгеморрагические анемии (вследствие как наружных, так и внутренних кровопотерь): 1. Острые. 2. Хронические. II . Анемии вследствие недостаточности эритропоэза. 1. Наследственные апластические анемии: А. Панцитопения (в сочетании с врожденными пороками развития — тип Фанкони; без врожденных аномалий — тип Эстрена—Дамеше-ка); Б. С парциальным поражением эритроидного ростка (анемия Блекфе-на—Даймонда). 2. Приобретенные апластические анемии: А. С панцитопенией (острая, подострая, хронические формы); Б. С парциальным поражением эритропоэза, в том числе транзиторная эритробластопения младенцев. 3. Дизэритропоэтические анемии (наследственные и приобретенные). 4. Сидеробластные анемии (наследственная, приобретенные). 5. Дефицитные анемии (анемии вследствие дефицита специфических факторов): А. Мегалобластические анемии а) фолиеводефицитные (недостаток в питании или мальабсорбция); б) витамин В12-дефицитные (мальабсорбция или нарушение транс- в) оротовая ацидурия. а) железодефицитные; б) медьдефицитные; в) отравления свинцом; г) синдром талассемии (бессимптомное носительство гена талассе- 6. Физиологическая анемия младенцев. 7. Ранняя анемия недоношенных. III. Гемолитические анемии. 1. Наследственные: A. Мембранопатии: а) дефицит или нарушение структуры белка мембраны (микросфе- б) нарушение липидов мембраны (акантоцитоз и др.). Б. Ферментопатии (нарушения активности ферментов пентозофосфат-ного шунта, гликолитического цикла, обмена нуклеотидов, глютати-она). B. Дефекты структуры цепей глобина (гемоглобинопатии S, С, D, Е и 2. Приобретенные: А. Иммунопатологические (изоимммунные — гемолитическая болезнь новорожденных, переливание несовместимой крови; аутоиммунные; гаптеновые; медикаментозные). Б. Инфекционные (бактериальные, цитомегаловирусная и другие вирусные, паразитарные). В. Витаминодефицитные (Е-витаминодефицитная анемия недоношенных). Г. Токсические (отравления тяжелыми металлами и другими химическими веществами, оксидантами). Д. Болезнь Маркьяфавы—Микеле (пароксизмальная ночная гемогло-бинурия). Е. ДВС-синдром разной этиологии и механическое повреждение эритроцитов. IV. Анемии смешанного генеза. A. При острых инфекциях, сепсисе. B. При опухолях и лейкозах. Безусловно, данная классификация учитывает лишь ведущий патогенетический признак и во многих случаях одну и ту же анемию можно отнести к разным группам. Например, эритропоэз неадекватен при талассемиях, мак-роцитарных витамин В)2-дефицитных анемиях, а при панцитопении Фанко-ни укорочена продолжительность жизни эритроцитов. Хроническая постгеморрагическая анемия по патогенезу — железодефицитная. При хронических инфекционных и воспалительных заболеваниях повышено потребление железа ретикулоэндотелиальными клетками и развивается железодефицитная анемия, лечение препаратами железа при которой оказывает минимальное влияние на гемопоэз. При острых инфекционных заболеваниях анемия может быть следствием: подавления эритропоэза, укорочения продолжительности жизни эритроцитов, фрагментации эритроцитов (например, при ДВС-син-дроме), иммуноопосредованной деструкции эритроцитов (гаптеновой). Однако считаем патогенетическую классификацию нужной, дающей основание для дифференцированной диагностики и терапии. ' Морфологическая классификация анемий. В современных автоматических счетчиках крови Coulter получают следующие показатели: MCV (Mean corpuscular volume) — средний объем эритроцитов в фемто-литрах — фл (фл = Ю-15 л), нормальные величины 75-100 фл.
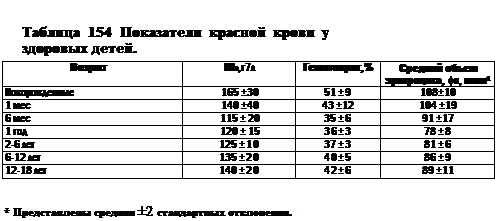
МСНС (Mean corpuscular hemoglobin concentration) — средняя концентрация гемоглобина в эритроцитах; расчет — деление уровня гемоглобина в г% на гематокритное число: нормальные величины 32-36 г%. RDW (Red blood cell distribution width) — показатель распределения эритроцитов по объему, показатель степени анизоцитоза (ПСА), нормальные величины 13,5 + 1,5%. Рассчитывают путем деления стандартного отклонения среднего объема на величину среднего объема у больного и умножают на 100. Следует подчеркнуть, что все нормальные величины даны для детей старше 2 мес жизни. Нормальные показатели красной крови у детей представлены в табл. 154. В соответствии с изложенным, выделяют: микроцитарные анемии (MCV менее 75 фл), нормоцитарные (MCV 75-100 фл) и макроцитарные (MCV более 100 фл). Нормоцитарно-нормохромньши анемиями являются: острые постгеморрагические и гемолитические, а также анемии при миелодисплазиях, опухолях, гипопролиферативные (при почечной, эндокринной патологии, интоксикациях, белковой недостаточности) и гипопластические на поздних стадиях. Микроцитарно-нормохромные анемии могут быть обусловлены теми же причинами, а также наследственным микроцитозом, эллиптоцитозом, пиро-пойкилоцитозом. Микроцитарно-гипохромные анемии (MCV менее 75 фл, МСНС менее 30 г%) отмечают при: железодефицитных и медьдефицитных состояниях, талассе-миях, хроническом отравлении свинцом, идиопатическом легочном гемоси-дерозе, сидеробластных состояниях, семейной микроцитарной гипохромной и пиридоксин-чувствительных анемиях.
Показатель однородности популяции эритроцитов, степени анизоцитоза также полезен при дифференциальном диагнозе анемий (табл. 155). По степени тяжести анемии делят на: легкие (НЬ в пределах 85-110 г/л, а число эритроцитов снижено до 3,5 х 1012/л), средней тяжести (НЬ — менее 85, но более 65 г/л, а число эритроцитов 2,5-3.4 х 1012/л) и тяжелые (НЬ — менее 65 г/л, а число эритроцитов менее 2,5 х 1012/л). По регенераторной способности костного мозга: регенераторные (число ретикулоцитов — 15-50%о, ретикулоцитарный индекс более 1, но менее 2), ги-порегенераторные (ретикулоцитарный индекс 1 и менее) и гиперрегенераторные (число ретикулоцитов более 50%о, ретикулоцитарный индекс более 2). Гиперрегенераторная анемия — типичный признак избыточного разрушения эритроцитов. Ретикулоцитарный индекс рассчитывают умножением величины показателя гематокрита на число ретикулоцитов (в%) и делят на нормальный показатель гемокрита. Например, у 7-летнего ребенка при гематокрите 20% число ретикулоцитов 2% — ретикулоцитарный индекс равен 2 х 20:40, то есть 1, что указывает на недостаточную эритропоэтическую активность костного мозга при анемии. Острая постгеморрагическая анемия (ОПА). ОПА — заболевание, развивающееся в результате быстрой потери значительного количества крови (обычно более 10% объема циркулирующей крови, составляющего у здоровых детей старше 2 мес примерно 70-75 мл/кг массы тела). Об ОПА у новорожденных см. наш учебник «Неонатология» (СПб, Специальная литература, 1996). Этиология 1. Травмы, приведшие к наружным или внутренним кровотечениям. 2. Кровотечения в желудочно-кишечном тракте, локализующиеся: в нижних отделах пищевода (из-за варикозного их расширения при портальной гипертензии, грыже пищеводного отверстия диафрагмы, коротком пищеводе, его ахалазии), желудке и двенадцатиперстной кишке (язвенная болезнь, острые стрессорные язвы желудка при ожогах, отравлениях, почечной недостаточности, заболеваниях печени; прием ацетилсалициловой кислоты и других медикаментов), кишечнике (полипы, язвенно-некротический энтероколит, инвагинация, трещина заднего прохода, геморрагический васкулит, портальная гипертензия и др.). 3. Кровотечения после мелких хирургических операций (экстракция зуба, тонзиллэктомия, аденотомия и др.), развивающиеся у детей с сопутствующей наследственной или приобретенной патологией системы гемостаза. 4. Маточные кровотечения у девушек как с дизовариальной патологией, так и при тромбоцитопениях или тромбоцитопатиях. 5. Разрыв аневризм сосудов с кровотечением в мозг или во внутренние органы, кровотечение из гемангиом. 6. Тромбо-геморрагический синдром. 7. Геморрагические диатезы и геморрагические заболевания. 8. Злокачественные опухоли и лейкозы, гипо- и апластические анемии. 9. Острая печеночная недостаточность. 10. Кровотечения в момент хирургических операций при травмах сосудов. Основным в остром периоде является объем потери крови и развивающееся вследствие этого несоответствие объема циркулирующей крови (ОЦК) и объема сосудистого русла, что может привести к постгеморрагическому шоку, протекающему в 4 стадии: централизация кровообращения, переходная стадия, стадия децентрализации кровотока и терминальная. Важно отметить, что в первые сутки после острой кровопотери клинический анализ крови может быть без отклонений от нормы и лишь к концу первых суток с максимумом
Таблица 156 Клиническая картина стадий нарушения гемодинамики при постгеморрагическом шоке у детей старше года.
через 2-3 сут развивается снижение гематокритного показателя и уровня эритроцитов, гемоглобина. Вторая стадия шока развивается у взрослых при кровопотере 25-30% ОЦК. Новорожденные более чувствительны к кровопо-тере, тогда как дети старше года вследствие симпатикотонии даже несколько более резистентны, чем взрослые, и у них артериальная гипотензия появляется обычно при потере 30-35% ОЦК. В отдаленном периоде после кровопоте-ри, превышающей 15% ОЦК, развивается железодефицитная анемия. Клиника В значительной мере определяется преморбидным фоном, причиной и скоростью кровопотери, локализацией внутреннего кровоизлияния. При профуз-ном кровотечении может развиться коллапс, в генезе которого может иметь значение и психоэмоциональный стресс, связанный с видом теряемой крови. В то же время, при очень быстрой кровопотере 30% ОЦК может возникнуть острая коронарная и миокардиальная недостаточность. Усредненная картина постгеморрагического шока представлена в табл. 156. Диагноз Диагноз основан на сопоставлении клинико-лабораторных данных. Важно помнить, что сразу после острой кровопотери уровни НЬ и эритроцитов могут находиться на обманчиво высоком уровне и лишь после гемодилюции их снижение может отразить размер кровопотери. В ближайшие часы после кровопотери развиваются тромбоцитоз и нейтрофилез, к концу суток — гипопротеинемия, а в ближайшие дни — ретикулоцитоз. При ОПА эритроциты нормохромные и нормоцитарные. Лечение. Начинать лечение следует с остановки кровотечения. Всех больных, у которых по анамнестическим или клиническим данным предполагают кровопотерю более 10% ОЦК, а также больных с желудочно-кишечными кровотечениями, внутренними кровоизлияниями необходимо направить в стационар — отделение реанимации. При систолическом артериальном давлении менее 70 мм рт. ст. необходимо переливание коллоидных кровезаменителей (6% гидроксиэтилкрах-мал — ХАЕС-стерил, поливинол, полиглюкин, раствор желатина, 5% альбумин или др.) из расчета 10-15 мл/кг. Медлить с внутривенной инфузией нельзя, ибо гиповолемия — основная причина тканевой гипоксии, сердечной недостаточности. После устранения гиповолемии, если АД не нормализуется, начинают вливание инотропных препаратов (допамин, добутрекс) и далее решают вопрос о необходимости хирургической помощи, переливания эритроцитной массы, виде питания и др. Всех больных важно согреть, назначить кислородную поддержку, кардиотрофики. При ОПА вопрос о переливании эритроцитной массы возникает в зависимости от клинической картины, но чаще при НЬ менее 60-65 г/л, ибо после переливания крови и ее препаратов даже при правильном подборе донорской крови возможны разнообразные осложнения. Согласно данным литературы, примерный риск гемотрансфузионных осложнений следующий: вирусный гепатит — 1: 200, острый гемолиз — 1: 25 000, анафилактоидная гипотензия — 1:15 000, лихорадка (негемолитическая) — 1: 200, аллергия — 1: 1000, отсроченный гемолиз — 1: 2500, аллоимммуниза-ция к эритроцитам — 1:100, аллоиммунизация к лейкоцитам, тромбоцитам — 1:10 гемотрансфузий [Walker R. Н., 1987]. Общепризнано, что риск всех упомянутых осложнений достоверно ниже после переливания эритроцитной массы. Желательно применять эритроцитную массу не более 3-дневной консервации. При тяжелых анемиях с НЬ менее 50 г/л скорость переливания эритроцитной массы 1 мл/кг в мин. Считают, что переливание эритроцитной массы 1 мл/кг массы тела больного повышает гематокритный показатель на 1%. При острой кровопотере желательно достичь гематокритного показателя 35%. При тяжело протекающей ОПА с явлениями вторичной сердечной недостаточности прибегают к дробным трансфузиям эритроцитной массы по 2-4 мл/кг, решают вопрос о целесообразности назначения фуросемида, мягких сердечных гликозидов, кардиотрофиков. После купирования острой кровопотери назначают на 3 мес препараты железа внутрь.
Хроническая постгеморрагическая анемия (ХПА). Этиология ХПА у детей встречается реже, чем у взрослых. Ее причинами могут быть: заболевания желудочно-кишечного тракта (язвы, полипы, болезнь Крона, диафрагмальная грыжа, кровососущие нематоды — анкилостомы, власоглав), легких (идиопатический гемосидероз), почек (мочекаменная болезнь, гема-турическая форма хронического нефрита), геморрагические заболевания и диатезы, приводящие к рецидивирующей кровоточивости слизистых оболочек. В первые дни и месяцы жизни ХПА может быть следствием фето-мате-ринских и фето-фетальных трансфузий. Патогенов При ХПА в костном мозге начинают превалировать медленно развивающиеся клетки, число делений в эритроне уменьшается, из-за дефицита железа развивается неэффективный эритропоэз, укорачивается длительность жизни эритроцитов. В периферической крови отмечают гипохромные пойкилоциты и микроциты. Вследствие дефицита железа развиваются различные гипови-таминозы (в основном группы В, С, А), иммунодефицит.
Клиника Симптоматика ХПА складывается из признаков основного заболевания, приведшего к ней, и клиники железодефицитной анемии, изложенной в главе 5, частых инфекционных процессов. Лечение Прежде всего, необходимо лечить то заболевание, которое осложнилось ХПА. Лечение собственно анемии сводится к назначению препаратов железа, витаминов, диеты по принципам, описанным в подразделе «Лечение» раздела «Железодефицитные анемии» (глава 5). Показания к трансфузии эритроцитной массы определяют в зависимости от возраста, причины и клинической картины анемии, наличия сопутствующих болезней. У детей первого года жизни обычно задумываются о необходимости трансфузии эритроцитной массы при НЬ менее 70 г/л, а у дошкольников и школьников — менее 50-60 г/л. Прогноз Прогноз зависит от заболевания, приведшего к развитию постгеморрагической анемии и возможности его лечения.
Наследственные апластические анемии. Анемия Фанкони (АФ) — наследственно обусловленное заболевание с общим поражением гемопоэза, врожденными аномалиями развития и нарушенными репаративными возможностями организма при повреждениях ДНК, что проявляется в хромосомной нестабильности, обнаружении многочисленных аномалий хромосом. Конституциональная панцитопения возможна и у детей без врожденных пороков (тип Эстрена—Дамешека), при сочетании с дискератозом. Этиология АФ — аутосомно-рецессивное заболевание с вариабельной пенетрантнос-тью и генетической гетерогенностью. 20% детей с АФ родились от родственных браков, частота которых в популяции примерно 0,5%. Гетерозиготное носительство встречается с частотой 1: 300. При кариотипировании лимфоцитов" и фибробластов больных АФ обнаруживают в большом проценте случаев (10-70) хромосомные аномалии в виде разрывов хроматид, перестроек, транслокаций, брешей и т. д. Считают, что дефектные гены, ответственные за снижение репаративных свойств организма, расположены в 22-й и 20-й хромосомах. Повышенная частота хромосомной нестабильности выявлена и у клинически здоровых носителей рецессивного гена АФ и при других вариантах конституциональной панцитопении, протекающей без врожденных аномалий. Патогенез В костном мозге выявляют пониженную клеточность (гипоцеллюляр-ность), угнетение всех ростков кроветворения (эритроидного, миелоидного, мёгакариоцитарного), разрастание жировой ткани. Таким образом, дефект гемопоэза при АФ локализован на уровне стволовой клетки, хотя и уровни гуморальных гемопоэтических факторов у детей с АФ снижены, или они отсутствуют. Кроветворные клетки имеют повышенное время созревания, усиление апоптоза. Уровень фетального гемоглобина повышен до 5-15% еще до развития цитопении. Длительность жизни эритроцитов детей с АФ существенно снижена (в 2,5-3 раза). Дата добавления: 2014-10-03 | Просмотры: 1208 | Нарушение авторских прав |