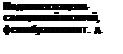|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Генез наиболее важных синдромов при ХПН. 9 страница
Дифференциальную диагностику проводят с другими видами геморрагических диатезов. Особенно необходимо разграничивать тромбоцитопатии с болезнью Виллебранда (опорный пункт диагностики — дефектная агрегация с ристоцетином, что бывает только при болезни Виллебранда и синдроме Бер-нара— Сулье). Изучение состояния коагуляционного звена гемостаза у больных позволяет исключить дефициты VIII, II, V, X, I и III факторов свертывания, для которых также характерен микроциркуляторный тип повышенной кровоточивости.
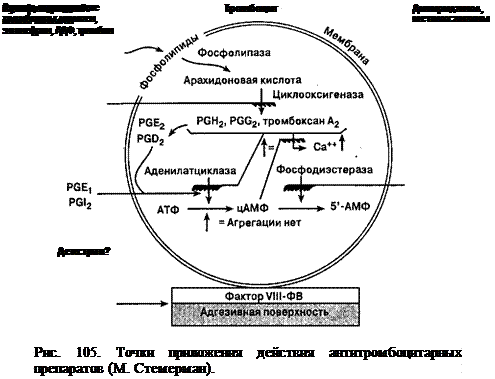
Диета в соответствии с возрастом и сопутствующими заболеваниями. Режим определяется интенсивностью геморрагического синдрома. Обычно необходимости в постельном режиме нет. Назначают препараты, способствующие улучшению адгезивно-агрегационной функции тромбоцитов: е-аминокапроно-вую кислоту, дицинон, адроксон, пантотенат кальция, АТФ внутримышечно в сочетании с препаратами магния внутрь, хлорофиллин натрия, препараты лития. Все перечисленные медикаменты применяют в обычных возрастных дозировках курсами. Показана также фитотерапия (см. т. 2, стр. 335), курсовое назначение препаратов-стабилизаторов мембран (эссенциале и др.), ан-тиоксидантов (витамин Е и др.), выявление и лечение НЦД. Необходимо избегать нарушающих функцию тромбоцитов препаратов, особенно ацетилсалициловой кислоты, которая, ингибируя простагландин-синтетазу (циклоксигеназу), резко тормозит синтез тромбоксанов, блокируя тем самым агрегацию (рис.105). Парацетамол не нарушает агрегацию тромбоцитов, тогда как все остальные нестероидные противовоспалительные препараты угнетают. Кроме того, угнетают агрегацию тромбоцитов эуфиллин, трен-тал, дипиридамон, преднизолон, гепарин, пенициллины, большие дозы витамина С, сульфаниламиды, цитостатики, мочегонные средства и др. Из пенициллинов особенно резко угнетает агрегационную функцию тромбоцитов карбенициллин. Назначение одновременно 3 ингибиторов функции тромбоцитов может вызвать желудочно-кишечное кровотечение у детей с эрозивными процессами в желудочно-кишечном тракте. Прогноз При наследственных тромбоцитопатиях в случаях отсутствия внутричерепных геморрагии для жизни благоприятный, если проводят адекватную терапию и вовремя ликвидируют выраженную кровопотерю. Следует отметить, что массивные внутричерепные геморрагии характерны лишь для очень тяжелых форм тромбастении, болезни Виллебранда и синдрома Бернара—Сулье.
Вазопатии. Включение вазопатии в группу геморрагических диатезов весьма условно, и это скорее традиция. Различают наследственные вазопатии (болезнь Рандю—Ослера, ангиоматоз сетчатки — синдром Гиппеля—Линдау; синдром гиперэластичной кожи — синдром Элерса—Данлоса; гемангиомы в сочетании с тромбоцитопенией, анемией — синдром Казабаха—Мерритта; телеангиэк-тазии кожи с атаксией — синдром Луи-Бар) и приобретенные вазопатии (геморрагический и другие виды аллергических васкулитов; симптоматические васкулиты при коллагенозах, медикаментозных и пищевых аллергозах; инфекционные и токсические вазопатии; гиповитаминозные вазопатии — дефициты витаминов С, Р и др.). Подавляющее большинство этих заболеваний описано в учебнике по детской дерматологии, некоторые — в настоящем учебнике. Наиболее распространенная вазопатия у детей — геморрагический вас-кулит.
Геморрагический васкулит (ГВ). ГВ (болезнь Шенлейна—Геноха, анафилактоидная пурпура, капил-ляротоксикоз) — иммунопатологическое заболевание, характеризующееся системным васкулитом и проявляющееся симметричными, чаще мелкоточечными кровоизлияниями на коже, обычно в сочетании с болью и отечностью суставов, болями в животе, поражением почек. ГВ диагностируют у 2-2,5 на 10 ООО детского населения в год. Чаще заболевают дети от 6 мес до 7 лет. Среди больных мальчиков в 2 раза больше, чем девочек. Этиология и патогенез Причина болезни не установлена, но у некоторых детей отмечена связь ее развития с перенесенными острыми вирусными заболеваниями, бактериальными инфекциями (чаще стрептококковыми — у 50% больных), профилактическими прививками, введениями гамма-глобулина, лекарственной аллергией,
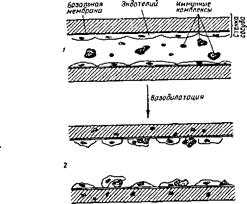
Рис. 106. Развитие иммунокомплексного васкулита (схема) (А. И. Воробьев и др.). 1 — циркуляция комплексов (отложений нет); 2 — отложение комплексов в стенке сосуда (локализация поражений зависит от состава комплексов); 3 — васкулит (нейтрофильно-макрофагальная реакция, тромбоз).
гельминтозами. Специфическое наследственное предрасположение (то есть наличие аналогичного заболевания в семье) имеется лишь у небольшого числа больных, тогда как отягощение родословной аллергическими болезнями есть у большинства детей. У многих больных удается обнаружить очаги хронической инфекции. Полагают, что ведущую роль в патогенезе может играть III тип аллергических реакций — иммунокомплексное поражение, приводящее к лейкоцитокластическому васкулиту (рис. 106). Не исключена также триггерная роль каких-то неизвестных эндогенных (?) веществ, поступающих из кишечника. У некоторых детей в основе патогенеза болезни лежит иммунодефицитное состояние, в частности, дефицит С2-комплемента. По мнению А. В. Папаяна, решающую роль в патогенезе ГВ могут играть реакции по типу феномена Швартцмана (рис. 107). Подтверждением иммунокомплексного поражения сосудов при ГВ является обнаружение в местах поражения (в коже, внутри сосудов) иммуноглобулинов А, М, G, фибриногена, СЗ-комплемента. Такие изменения находят у 2/3 больных, хотя у всех имеются отложения в сосудах почек комплексов с Свертывание
Активация факторов свертывания VII и X
Лейкоциты
Сывороточные
компоненты комплемента
(подавляются антикомплементарной сывороткой, фактором яда кобры) Повреждение, преципитация, отложение фибрина и снижение его клиренса Выделение тромбопластических веществ Повреждение ткани
Рис. 107. Иммунологические и неиммунологические реакции при феномене Швартцмана (P. X. Кормен, С. С. Асгар). СЗ-9 — фракции комплемента; BP — фактор сыворотки, активирующий комплемент; ВА — его активная форма; ПМЛ — полиморфно-ядерные лейкоциты. IgA. У части больных обнаружен высокий уровень IgA в крови и В-лимфоци-тов с IgA. По мере затухания болезни количество В-лимфоцитов с IgA в крови снижается, но этого не происходит у больных нефропатией. В последнее десятилетие обращают внимание на то, что маркером васкулита может служить повышенный уровень в крови антигена фактора Виллебранда (ФВаг). Грубых изменений свертывающей системы крови обычно не находят, но, как правило, регистрируют тенденцию к гиперкоагуляции. У '/3 детей с ГВ имеется ДВС-синдром. Поражение почек вызвано иммунными комплексами с IgA и может носить характер очагового, сегментарного (по типу IgA-нефропатии при болезни Берже), реже — острого, подострого диффузного гломерулонефрита. Классификация. Г. А. Лыскина и соавт. (2000) предлагают следующую клиническую классификацию ГВ. 1. Форма (эволюция) болезни: начальный период; ремиссия; рецидив; 2. Клинические формы: 3. Клинические синдромы: суставной; абдоминальный; почечный. 4. Степень тяжести. — общее состояние удовлетворительное; — необильные высыпания; — возможны артралгии. Среднетяжелая: — общее состояние средней тяжести; — обильные высыпания; — артралгии,артрит; — периодические боли в животе; — микрогематурия; — небольшая протеинурия (следы белка в моче). Тяжелая: — общее состояние тяжелое; — высыпания обильные сливные с элементами некроза; — рецидивирующие ангионевротические отеки; — упорные боли в животе; — желудочно-кишечное кровотечение; — макрогематурия; — нефротический синдром; — острая почечная недостаточность. 5. Характер течения:
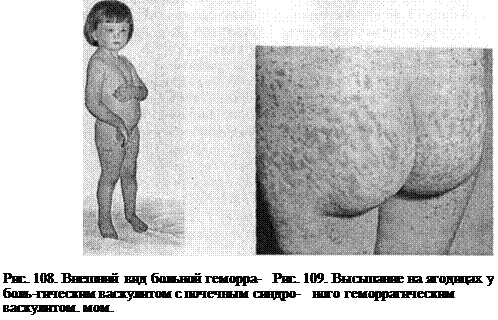
(рецидивирующее). Клиника. Наиболее типичным признаком является поражение кожи (рис. 108, 109). При отсутствии кожных изменений диагноз не ставят. Начало болезни (чаще через 1-2 нед после острого респираторного заболевания) может быть ост рым с одновременным появлением нескольких синдромов, но поражения кожи иногда возникают и позже суставного и абдоминального синдромов. Обычно изменения появляются на коже нижних конечностей, затем на ягодицах, верхних конечностях, груди, пояснице, лице и шее. В типичных случаях вначале это мелкие (около 2-3 мм в диаметре) эритематозные пятна или макулопапулы. При надавливании элементы становятся бледными, но в дальнейшем теряют эту способность. Иногда на начальном этапе болезни при назначении гепарина сыпь может исчезнуть за несколько часов. Чаще сыпь через некоторое время становится геморрагической и элементы приобретают красно-багровую окраску. Далее сыпь бледнеет, становясь коричневой, а потом с желтоватым оттенком, но обычно не цветет. Кожные поражения чаще симметричные, группируются вокруг суставов, на ягодицах, внутренней поверхности бедер, разгибательных поверхностях конечностей. Кожные поражения могут быть полиморфные за счет дальнейших подсыпаний. Волнообразность подсыпаний — типичный признак. Кроме того, у больных иногда могут быть явления многоморфной или нодозной (узловатой) эритемы, ангионевротического отека, а также отечности кистей, стоп, голеней, век, лица. Элементы сыпи могут достигать 2-3 см в диаметре. Вследствие сопутствующей вторичной тромбоцитопатии (особенно на фоне назначения нестероидных противовоспалительных средств) возможны носовые кровотечения, экхимозы. Зуд для ГВ нехарактерен. При тяжелом течении возможна некротическая пурпура, которой предшествуют буллезные высыпания. Некрозы могут оставлять после себя рубцы. Суставной синдром — припухлость, болезненность, гиперемия — бывает у 2/3 больных в крупных суставах (коленных, локтевых, голеностопных и др.). Чаще поражение несимметричное. Артрит при ГВ обычно быстро проходит и стойких деформаций после себя не оставляет. Абдоминальный синдром развивается приблизительно у 2/3 больных ГВ и характеризуется внезапными схваткообразными, очень резкими болями, которые чаще локализуются возле пупка, могут сопровождаться стулом черного или алого цвета (мелена), тошнотой, повторной рвотой (гематомезис). Живот слегка вздут, но напряжение брюшной стенки при неосложненном течении обычно отсутствует. Стул может учащаться. При рентгеноскопии желудочно-кишечного тракта обнаруживают снижение подвижности кишечника, сегментарные сужения, вероятно, обусловленные отеком и геморрагиями. Нарушения моторики могут привести к непроходимости, инвагинации, инфарктам, перфорации кишки и перитониту (у 2-3% больных). Анализ на скрытую кровь в стуле (реакция Грегерсена) положителен при серийном исследовании у 80% больных. Почечный синдром встречается у 1/3-1/2 больных в виде очагового или сегментарного, диффузного гломерулонефрита, подострого экстракапиллярного пролиферативного нефрита. Выделяются 4 клинические формы поражения почек: 1) транзиторная гематурия; 2) капилляротоксический нефрит, гематурическая форма; 3) капилляротоксический нефрит с нефротическим синдромом и гематурией; 4) быстропрогрессирующий гломерулонефрит. Первые две формы встречаются с одинаковой частотой 45% и протекают благоприятно. У некоторых детей микроизменения в моче или даже макрогематурия без экстраренальных симптомов и грубого нарушения функции почек держатся достаточно длительно — несколько недель или месяцев и даже лет. В этих случаях речь идет, вероятно, о сегментарном нефрите. У '/3 больных нефро-патией имеется клиника типичного острого нефрита с четкими экстрареналь-ными симптомами и синдромами. Течение этого вида нефропатии также чаще доброкачественное, но может привести и к хроническому нефриту. Наиболее тяжелое осложнение — подострый нефрит, ОПН. Поражения других органов при ГВ редки — в процесс вовлекается головной мозг (преходящие судороги, парезы конечностей, асимметрия сухожильных рефлексов, симптомы поражения черепных нервов вследствие отека, реже кровоизлияния), глаза, отмечается припухлость яичек. Изменения сердечнососудистой системы, умеренная гепатоспленомегалия преходящи и отмечаются лишь в острой фазе. Температура тела при ГВ обычно субфебрильная в течение 1-й недели болезни, на высоте болевого синдрома. Стойкий субфебрилитет или лихорадка — признаки сопутствующей инфекции. Диагноз. Ставят на основании клинических данных, и он не требует дополнитель-> ных исследований для подтверждения. В анализе периферической крови обнаруживают разной степени выраженности лейкоцитоз (умеренный), увеличенную СОЭ, нейтрофилез, эозинофилию, тромбоцитоз. Учитывая частое поражение почек, всем больным необходимо систематически делать анализы мочи. При наличии изменений в моче производят исследования для оценки функционального состояния почек. В связи с тем, что у '/3 больных может быть ДВС-синдром, целесообразно регулярно подсчитывать количество тромбоцитов, в разгар болезни изучить состояние гемостаза больного (время свертывания венозной крови, толерантность к гепарину, тромбиновое и парциальное тромбопластиновое время, уровень фибриногена, продуктов деградации фибриногена и фибрина в крови, этаноловый и протаминсульфатный тесты). Большие затруднения вызывает своевременная диагностика осложнений абдоминального синдрома — аппендицита, инвагинации, перфорации кишечника и перитонита. Такие дети нуждаются в совместном наблюдении педиатра и детского хирурга в динамике.
Дифференциальный диагноз. Дифференциальный диагноз проводят, прежде всего, в зависимости от клиники, с ревматизмом, кожными болезнями, заболеваниями желудочно-кишечного тракта. Иногда абдоминальный синдром на несколько часов и даже на 1-3 дня предшествует кожным поражениям, и тогда лишь наблюдение за больным в динамике, отсутствие локальной симптоматики позволяют поставить правильный диагноз. Как уже отмечалось, наличие ГВ не исключает возможности аппендицита, инвагинации, перитонита после перфорации, и поиски соответствующей симптоматики у больного в остром периоде должны быть каждодневными. При этом следует помнить о травматичности глубокой пальпации для больных с ГВ. Их надо пальпировать осторожно и нечасто. Дифференцировать ГВ от других видов геморрагического васкулита можно на основании наличия у больных капилляротоксикозом триады: поражения кожи, суставов и абдоминальный синдром, что для других форм нехарактерно. Дифференциальная диагностика с коагулопатиями и нарушениями тромбоцитар-ного звена гемостаза, как правило, затруднений не вызывает. Лечение. Специфической терапии ГВ не существует. Если установлена связь с перенесенной бактериальной инфекцией или у больного имеются декомпенсиро-ванный очаг хронической инфекции, лихорадка, показан курс антибиотиков. Тщательный анализ анамнеза должен навести на мысль о пищевом или лекарственном аллергене, который необходимо устранить из рациона и лечения. Впрочем, лучше отменить все медикаменты, на фоне которых возникла пурпура. Диета в остром периоде с ограничением животных белков, поваренной соли, экстрактивных веществ, продуктов, содержащих много гистамина или являющихся его либераторами. Нежелательны также продукты промышленного консервирования. Полезны кисломолочные продукты. Режим постельный на 2-3 нед, затем его постепенно расширяют, так как возможны рецидивы пурпуры, объясняемые как ортостатическая пурпура. Всем детям целесообразно назначение активированного угля или других энтеросорбентов холестирамина, полифепана внутрь. Применяют также желудочные капли, антигистаминные препараты, пантотенат кальция, рутин, умеренные дозы аскорбиновой кислоты, фитотерапию, хотя эффективность их и сомнительна. При болях в животе, не проходящих после приема желудочных капель, назначают обезболивающие — но-шпу, баралгин и др. Считают патогенетически показанным назначение одного из дезагрегантов: дипиридамол (Курантил, Персантин) по 5 мг/кг/сутки в 4 приема, или пенток-сифиллин (Трентал, Агапурин) по 5-10 мг/кг/сутки в 3 приема, или тиклопи-дин (Тиклид) по 5-10 мг/кг/сутки 2 раза в день. Длительность терапии 3 мес [Лыскина Г. А. и соавт., 2000]. При среднетяжелом течении ГВ эти авторы рекомендуют назначать сочетанно 2 дезагреганта, а при рецидивирующем — добавлять к терапии плаквинил (Делагил) по 5-6 мг/кг/сутки 1 раз на ночь в течение 6-12 мес и/или а-блокаторы — ницерголин (Сермион) или троксевазин, препараты никотиновой кислоты (ксантинола никотинат, Компламин, Теони-кол), кетотифен (Задитен), мембраностабилизаторы (витамины А по 1 мг в сутки, Е по 20-25 мг/сутки, димефосфон по 20 мг/кг 3 раза в день). Выраженная активность процесса с бурным абдоминальным, кожным и суставным синдромом — показание к сочетанному применению преднизолона и гепарина. Изолированное назначение преднизолона опасно, так как он способствует гиперкоагуляции, а склонность к развитию ДВС-синдрома при этом заболевании имеется (даже если нет четких признаков его наличия). Преднизолон обычно назначают в дозе 1 мг/кг, а гепарин 200-300 ЕД/кг в сутки, разделенной на 4-6 введений под кожу живота. Если на фоне гепари-нотерапии время свертывания венозной крови продолжает оставаться укороченным (менее 8 мин), то дозу можно увеличить в 1,5 раза. Гепарин нельзя вводить 2 или 3 раза в день (!), так как это провоцирует развитие внутрисосу-дистых тромбов. Отмена гепарина должна быть постепенной, но за счет снижения дозы, а не уменьшения числа инъекций (!). Иногда при бурной клинической картине приходится прибегать к инфузионной терапии, и в этом случае можно достичь оптимального введения гепарина — внутривенно капельно с равномерным его поступлением в организм в течение суток. Предшествует началу гепаринотерапии вливание свежезамороженной плазмы как источника антитромбина III. При тяжелом течении ГВ Лыскина Г. А. и соавт., помимо гепаринотерапии и глюкокортикоидов, рекомендуют 5-8 сеансов плазмафереза 2-3 объемов циркулирующей крови. Первые три сеанса плазмафереза проводят ежедневно, последующие — 1 раз в 3 дня. В качестве замещающих препаратов используют свежезамороженную плазму, растворы альбумина, глюкозы, низкомолекулярные декстраны. Возможно сочетание пульс-терапии преднизолоном (15-20 мг/кг/сутки в течение 3 дней) и плазмафереза. У больных подострым нефритом или с бурным течением гломерулонеф-рита прибегают к сочетанному назначению иммунрдепрессантов (азатиоприн или циклофосфамид) с глюкокортикоидами и гепарином, антиагрегантами (курантил). Цитостатики не следует давать только в связи с затяжным или волнообразным течением болезни. У таких детей необходимо искать гельминтов, очаги инфекции, выявлять аллерген, то есть искать причину. Всегда нужно помнить, что назначение иммунодепрессантов в педиатрии — ultima ratio (последний довод). Прогноз Считают, что 60% больных ГВ выздоравливают в течение месяца, а 95% — в течение года. Хронический нефрит развивается у 1-2% больных ГВ. Летальность при ГВ около 3% и даже менее за счет форм с висцеральными осложнениями и случаев хронического нефрита. Диспансерное наблюдение При поражении почек соответствует изложенному в главе 15. Если поражение почек отсутствует, дети находятся на диспансерном учете у участкового педиатра в течение 5 лет. Каждые полгода ребенка показывают стоматологу, оториноларингологу для своевременной диагностики и санации наиболее распространенных очагов инфекции. Так же регулярно исследуют кал на яйца гельминтов. Не реже чем один раз в квартал и после каждого перенесенного ОРЗ делают анализы мочи. Медицинское освобождение от прививок дают на 2 года. Плановая терапия не показана.
ДИССЕМИНИРОВАННОЕ ВНУТРИСОСУДИСТОЕ СВЕРТЫВАНИЕ КРОВИ. Диссеминированное внутрисосудистое свертывание (ДВС-синд-ром) — общепатологический процесс, сутью которого первично является усиленная внутрисосудистая коагуляция, активация клеток крови и сосудистого эндотелия, приводящая к блокаде микроциркуляции сгустками/тромбами и повышению вязкости крови. Вызванная этим активация каскадной системы плазменных протеаз: калликреин/кининовой, фибринолитической, системы комплемента («протеолитический взрыв») и повышенное потребление факторов субстратов (про- и антикоагулянтов), тромбоцитов приводят к поражению эндотелия, кардио-васкулярному коллапсу и геморрагическому синд- Частота Согласно Р. Ковачи (1997), у взрослых госпитализированных больных частота ДВС-синдрома составляет 1: 1000 и он занимает второе место после болезней печени как причина приобретенных коагулопатий. По данным нашего сотрудника Д. О. Иванова, среди новорожденных, находящихся на отделении реанимации, лабораторно ДВС-синдром можно выявить примерно у одной трети детей (у 100% новорожденных с сепсисом). Этиология и патогенез. Причины, приводящие к ДВС-синдрому, группируют следующим образом: 1) активирующие внутреннюю систему гемокоагуляции через активацию XII фактора (фактор Хагемана) при травме эндотелиальных клеток — инфекции (как правило, сепсис, вызванный грамотрицательными микробами, реже грамположительными, тяжелые внутриутробные вирусные инфекции — герпес, цитомегалия, краснуха), тяжелые асфиксия и ацидоз, гипотермия, любой этиологии длительная гипотензия, шок, по-лицитемия, синдром дыхательных расстройств, как неонатальный, так и взрослого типа, сосудистые катетеры; 2) повреждающие ткани с освобождением тканевого тромбопластина и в присутствии VII фактора активирующие внешнюю систему гемокоагуляции — акушерские осложнения: предлежание плаценты, преждевременная ее отслойка, инфаркты и хорионангиома плаценты, эклампсия, внутриутробная смерть одного плода из двойни, эмболия околоплодными водами, повреждение мозга, острый лейкоз и опухоли, некротический энтероколит; 3) вызывающие внутрисосудистый гемолиз (аспергиллезный сепсис, тяжелые формы гемолитической болезни новорожденных, переливание несовместимой по основным эритроцитарным антигенам крови); 4) снижающие интенсивность удаления активированных факторов свертывания крови за счет угнетения ретикулоэндотелиальной системы — тяжелые заболевания печени, укусы змей, гипотермия, ретикулоэндо-телиальные гипофункции. Наиболее частые причины ДВС-синдрома у детей — шоковые состояния и тяжелое течение кишечных инфекций. М. С. Мачабели выделила четыре стадии ДВС-синдрома: 1) стадия гиперкоагулемии; 2) стадия нарастающей коагулопатий потребления и фибринолитической активности (снижение количества тромбоцитов и уровня фибриногена в крови при нормо- или гиперкоагуляции в первой фазе); 3) стадия дефибриногенизации и патологического фибринолиза со снижением уровня практически всех факторов свертывания крови и глубокой тромбоцитопенией (как результат нарушения микроциркуляции возникает гипоксия с дистрофическими изменениями внутренних органов и нарушением их функции, то есть шок); 4) восстановительная стадия, которую иногда следует расценивать как стадию остаточных тромбозов и блокад. По мнению некоторых зарубежных авторов, обеднение крови факторами свертывания, по крайней мере во II стадии ДВС-синдрома, является скорее результатом удержания их в ретикулоэндотелиальной системе, чем потребления при образовании внутрисосудистых тромбов. До недавнего времени тромботическую тромбоцитопеническую пурпуру (ТТП), гемолитико-уремический синдром (ГУС) всегда относили к ДВС-син-дрому. Однако у большинства таких больных не обнаружено коагулопатии (нормальные величины АЧТВ, ПВ, ТВ и уровни I, V, VIII факторов свертывания крови), но выявлен высокий уровень в крови фактора Виллебранда с высоким молекулярным весом, что может стимулировать агрегацию тромбоцитов. Отсюда пусковым фактором патогенеза стали рассматривать: 1) активацию моноцитов с выделением ими ФНО, ИЛ-ib, ИЛ-6, ИЛ-8 и тромбоцитов с агрегацией их; 2) воспаление эндотелия (системный васкулит), вызываемое вероцитоток-сином некоторых грамотрицательных бактерий. Узловым же звеном патогенеза ДВС-синдрома является рассеянная по всему сосудистому руслу декомпенсированная тромбинемия с истощением механизмов антисвертывающей, а затем свертывающей системы. Шок — закономер-нейший как этиологический, так и патогенетический фактор ДВС-синдрома. Классификация Классификация ДВС-синдрома (по Папаяну—Цыбулькину): 1) по течению — острое, подострое, хроническое; 2) по степени декомпенсации периферического кровотока — компенсированное, субкомпенсированное, декомпенсированное; 3) по распространенности — локализованное, диссеминированное. Одновременно целесообразно выделение стадий по Мачабели. Клиническая картина. Проявления заболевания зависят от причины, приведшей к ДВС-синдро-му, стадии коагулопатии потребления и степени декомпенсации периферического кровотока. Прямого соответствия между стадиями коагулопатии потребления и клинической картиной нет. Тромбозы могут быть как в I стадии, так и во II, и в III: Типичные геморрагические расстройства при ДВС-синд-роме смешанного типа: длительные кровотечения из мест инъекций, венепункций, хирургических травм; разной степени выраженности кожный геморрагический синдром (пурпура) — петехии, экхимозы; спонтанные кровотечения (носовые, легочные, желудочно-кишечные, мелена и др.); кровоизлияния во внутренние органы (легкие, почки, желудочно-кишечный тракт), мозг; клинические проявления тромбозов сосудов (некрозы кожи, ОПН как признак тромбоза почечных сосудов; надпочечниковая недостаточность — следствие кровоизлияния в них и некроза; увеличение конечности в объеме, акроциа-ноз, цианоз и др.). У большинства детей в III стадии развивается микроанги-опатическая гемолитическая анемия. Поражения нервной системы вплоть до комы, судорог являются как признаком изменений именно в мозге, так и отражением степени декомпенсации периферического кровотока, то есть шока. Хронический ДВС-синдром проявляется легкой травматизацией и кровоточивостью из слизистых оболочек, нарушениями функции почек, преходящими неврологическими синдромами. Нередко встречается тромбофлебит. ГУС развивается обычно у детей раннего и дошкольного возраста после колиэнтерита, дизентерии или ОРВИ и характеризуется сочетанием признаков гемолитической анемии, тромбоцитопенической пурпуры и гломеруло-нефрита и (или) двустороннего коркового некроза почек с развитием ОПН. Молниеносная пурпура — крайней тяжести вариант течения системного васкулита. В типичном случае возникает в период выздоровления от бактериальных и вирусных инфекций и характеризуется симметричными кожными геморрагиями, четкими васкулитами, некрозами кожи и подкожной клетчатки. Чаще поражаются ягодицы и ноги. Вслед за тромботическими поражениями возникает токсикоз, в генезе которого основную роль играют токсины некротизированных тканей. У ряда больных именно очаговые расстройства кровообращения в ногах служат первым признаком болезни, а генерализованный кожный геморрагический синдром развивается позже. Клиническая картина тромботической тромбоцитопенической пурпуры имеет много общего с ГУС, так как в основе лежат диффузные тромбозы и эмболии. Наряду с чертами ГУС имеются признаки нарастающего поражения мозга — расстройство сознания, судороги, слепота, афазия и др., то есть шок, нарушения функции почек, лихорадка. Диагноз. Распознание стадии гиперкоагуляции возможно лишь при лабораторном исследовании на основании укорочения времени свертывания венозной крови (норма 4-8 мин), времени рекальцификации (норма 80-120 с); могут быть повышены уровни тромбоцитов, фибриногена и других факторов свертывания, положительны тесты паракоагуляции (этаноловый и протаминсульфат-ный), снижена активность свободного гепарина. Во II стадии закономерным изменением общих коагуляционных тестов является их разнонаправленность, но типичным является увеличение времени активированного парциального тромбопластинового, протромбинового и тромбинового тестов, тромбоцитопения, спонтанная агрегация тромбоцитов, положительные тесты на наличие продуктов паракоагуляции (этаноловая и протаминсульфатная пробы) и растворимые комплексы фибрин-мономера, повышение уровня ПДФ в сыворотке крови и снижение уровня антитромбина III. В III стадии ДВС-синдрома дефицит факторов свертывания в крови резко выражен (особенно фибриногена и факторов V, VIII, XIII), резко повышены фибринолитическая активность и время свертывания венозной крови, имеется глубокая тромбоцитопения, а увеличенное тромбиновое время не корригируется добавлением плазмы здорового донора. Очень характерно наличие в мазке венозной крови шиповид-ных, фрагментированных эритроцитов (шистоциты). Этот признак всегда есть у больных ГУС и ТТП. Дата добавления: 2014-10-03 | Просмотры: 1211 | Нарушение авторских прав |