|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Генез наиболее важных синдромов при ХПН. 11 страница
Гипергликемию и кетонурию иногда обнаруживают при ацетонемической рвоте, уремической и печеночной коме, базальных менингитах и менингоэн-цефалитах, травмах ЦНС. Помимо характерного анамнеза в дифференциальной диагностике может помочь пробное однократное введение инсулина (0,1 ЕД/кг массы тела внутривенно струйно), нормализующее гликемию при указанных состояниях в течение 1-2 ч й существенно не влияющее на содержание глюкозы в крови при диабетических комах. ДКА требует дифференциальной диагностики с пневмонией, острыми хирургическими заболеваниями брюшной полости, энцефалитом. Для своевременной диагностики сахарного диабета и особенно ДКА, любому больному с неясным диагнозом или находящемуся в отделении интенсивной терапии обязательно определяют уровень глюкозы в крови и моче и кетоновые тела в моче. Жировая инфильтрация печени (жировой гепатоз) развивается вследствие истощения запасов гликогена и избыточного поступления СЖК, нейтрального жира в гепатоциты. Печень увеличена, плотная, может быть болезненной из-за растяжения капсулы и нарушения оттока желчи. В крови повышен уровень холестерина, липидов, СЖК. Диабетические микроангиопатии (ДМА). — наиболее тяжелое осложнение сахарного диабета. Это генерализованное поражение мелких сосудов, выражающееся в утолщении базальной мембраны капилляров, затем в гиали-нозе сосудистой стенки с нарушением кровоснабжения и функции органов. ДМА развивается вследствие: 1) нарушения реологических свойств крови (гиперлипидемия; изменение белкового спектра плазмы, появление аномальных белков, например, гликозилированных белков; повышение адгезии и агрегации тромбоцитов, эритроцитов); 2) повреждения сосудистой стенки (гипергликемия, избыток катехолами-нов и глюкокортикоидов, гипоксия, циркулирующие иммунные комплексы). Наследственная предрасположенность сказывается преимущественным поражением того или иного органа и скоростью прогрессирования ДМА. ДМА имеются уже в момент манифестации сахарного диабета или раньше и могут быть обнаружены при биопсии (латентная стадия). Функциональная стадия клинически не проявляется, но ее можно диагностировать при инструментальном обследовании: капилляроскопии, термоскопии, офтальмоскопии. Органическая фаза ДМА характеризуется поражением соответствующих органов. Диабетическая нефропатия приводит к хронической почечной недостаточности, ретинопатия заканчивается отслойкой сетчатки и слепотой. Длительно существующая ангиопатия нижних конечностей сопровождается появлением трофических язв, поражения суставов и связок стопы («диабетическая стопа»). Диабетическая артропатия, энтеропатия, полинейропатия, энцефалопатия и другие нарушения становятся причиной инвалидизации больных сахарным диабетом. Диабетическая макроангиопатия при СД выражается в уплотнении стенок крупных сосудов, избыточном отложении солей кальция в них. Клинически у детей и подростков не проявляется. Лечение. Лечение доклинических стадий СД1типа не разработано. Чаще прибегают к назначению диеты с максимальным ограничением углеводов (до 50%) при нормальном или умеренно повышенном содержании белка и физиологическом — жира. Такая диета целесообразна при наличии ожирения, и ее рекомендуют до нормализации массы тела. У детей с низкой или нормальной массой тела возможно применение малых (1-4 ЕД/сут) доз инсулина на фоне диеты с ограничением легкоусвояемых углеводов, но физиологической калорийностью. В настоящее время проводят клинические испытания никотинамида, как средства, способствующего у части больных с аутоиммунным инсулитом обратному развитию иммунопатологического процесса. Предпринимают попытки иммунокорригирующей терапии. В лечении манифестной стадии СД I типа используют введение препаратов инсулина с заместительной целью в сочетании с диетой и дозированной физической нагрузкой. Цель лечения больных СД — максимальная компенсация нарушений обмена веществ. Критериями компенсации является стойкая нормогликемия, аглюкозурия, уровень гликозилированного гемоглобина 7-9%, нормальное содержание холестерина, липидов в крови, отсутствие осложнений, физиологическое физическое и половое развитие, нормальная физическая и умственная работоспособность. Препараты инсулина различают по длительности гипогликемического эффекта на препараты короткого, полупродленного и продленного действия (табл. 179).
Лечение явного сахарного диабета без ДКА начинают с инсулина короткого действия в суточной дозе 0,5-0,7 ЕД/кг, разделенной на 4-5 инъекций, за 30 мин до еды: перед завтраком — 50% дозы; перед обедом 15-20%; перед ужином — 20-25%; перед сном — 5-10%. Можно использовать инсулины полупродленного действия (50% суточной дозы за 1 ч до завтрака, 30-35% перед обедом, 15-20% на ночь), возможно однократное введение пролонгированного инсулина в 7-8 ч утра с «подколами» малых доз (2-4 ЕД) инсулина короткого действия перед едой. Далее при фиксированной диете производят подбор дозы и режима инсулинотерапии для постоянного лечения. Используют любые препараты или их комбинации при 2-3-кратном введении. Корректировку уровня глюкозы в крови осуществляют из расчета, что 1 ЕД инсулина снижает гликемию на 2,2 ммоль/л. Менее надежна регуляция дозы инсулина по наличию глюкозы в моче, определяемой перед каждой инъекцией инсулина. При аглюкозурии дозу снижают на 2-4 ЕД, при глюкозурии до 0,5% — не меняют, при глюкозурии 1% и более — повышают на 2-4 ЕД. Пока ребенок находится в лечебном учреждении, дозу вводимого инсулина корригирует врач в зависимости от показателей гликемии и глюкозурии. Одновременно проводят обучение детей старше 12 лет, родителей или лиц, которые будут ухаживать за больным дома. Программа обучения включает приобретение навыков контроля глюкозурии и гликемии с помощью специальных тест-наборов, регуляции дозы инсулина в зависимости от показателей и самостоятельного введения инсулина. Самоконтроль сахарного диабета позволяет уменьшить влияние стрессов, физической нагрузки и других непрогнозируемых факторов на уровень гликемии, добиться компенсации у большинства больных. Для постоянного лечения выбирают один из режимов введения инсулина, наиболее подходящий для условий жизни и потребности конкретного больного: —препараты короткого и промежуточного действия перед завтраком и ужином; —препараты короткого и промежуточного действия перед завтраком и ужином и короткого — перед обедом; —инсулины короткого и промежуточного действия перед завтраком, короткого действия перед обедом и ужином и инсулин промежуточного действия на ночь; —инсулин короткого действия перед завтраком, обедом и ужином и промежуточного — на ночь. При необходимости режим инсулинотерапии можно подобрать индивидуально.
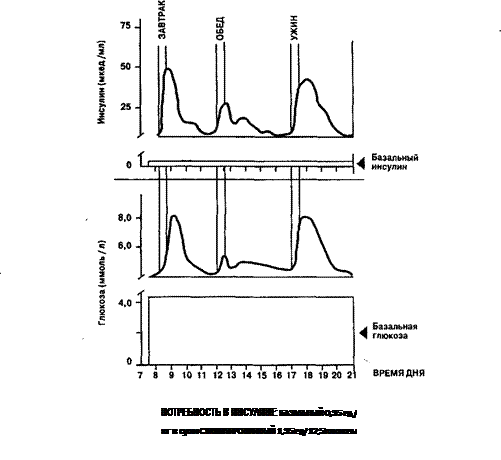
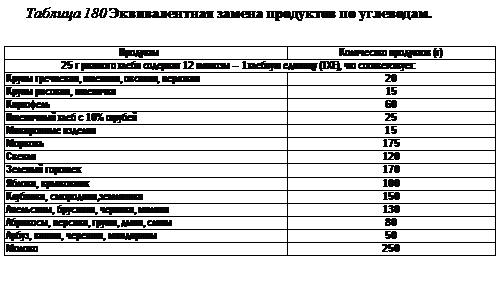
Общий метод регуляции вводимых доз инсулина основан на особенностях физиологической секреции инсулина (рис. 110). Базальный (продленный или полупродленный) инсулин обеспечивает базальную (без еды) гликемию. Его средняя суточная доза составляет около 0,35 ЕД/кг массы тела и контролируется по уровню глюкозы крови натощак (оптимально 3,5-5,5 ммоль/л). Препараты короткого действия используют для коррекции посталиментарной гликемии. За 30 мин до каждого приема пищи вводят инсулин короткого действия из расчета 1,3 ЕД на 12 г съеденных углеводов. Корректировка гликемии в зависимости от чувствительности к инсулину, остаточной секреции инсулина направлена на нормализацию уровня глюкозы в крови после еды (через 1 ч — до 8,9; через 2 ч — до 7,8; через 3 ч — до 6,7 ммоль/л). Современная инсулинотерапия требует постоянного самоконтроля в домашних условиях, хорошей информированности родителей больного ребенка. В противном случае используют традиционную инсулинотерапию, когда врач назначает препарат в минимальной, необходимой для сохранения жизни больного дозе, но таким образом возникают условия для быстрого развития осложнений. При рациональной терапии у части детей через 2-3 нед потребность в экзогенном инсулине снижается, иногда до 2-4 ЕД в сутки. Таким больным либо сохраняют минимальные дозы инсулина при расширенной диете, либо отменяют инсулин на фоне диеты с резким ограничением углеводов и при постоянном ежедневном контроле гликемии и глюкозурии. Диета при сахарном диабете должна быть физиологической по калорийности, содержанию белков, жира, углеводов, витаминов, минеральных веществ. Особенностью диеты является исключение легкоусвояемых углеводов (сахар, мед, конфеты, пшеничная мука, манная, рисовая крупы, крахмал, виноград, бананы, хурма) и замена их на углеводы, содержащие большое количество клетчатки, замедляющей всасывание глюкозы (ржаная мука, пшеничная мука с добавлением отрубей, гречневая, пшенная, перловая, овсяная крупы, картофель, овощи, фрукты, ягоды). Необходимым условием диетотерапии является фиксированное по времени и количеству распределение углеводов в течение суток в зависимости от получаемого инсулина. По возможности учитывают индивидуальные привычки и особенности питания в семье. Так, при 1-2-кратном введении инсулина пролонгированного действия больной получает углеводы в определенных количествах через 1 ч после инъекции, каждые 2-3 ч в течение 12 ч (периода максимального действия инсулина). Использование инсулина короткого действия (кроме препаратов типа Хумалог) предполагает назначение углеводов через 20-30 мин после введения инсулина. Обычно 1 ЕД инсулина вводят на 12 г съеденных углеводов (этот показатель условно назвали 1 хлебная единица). 12 г углеводов повышают уровень глюкозы в крови на 2,8 ммоль/л. Для упрощения расчетов можно пользоваться таблицей замены углеводов (табл. 180). При отсутствии осложнений больной получает диету с физиологическим содержанием белка и жиров. Обученные подростки и взрослые, осуществляющие контроль гликемии и расчет дозы инсулина самостоятельно, могут изменять режим введения инсулина и питание в зависимости от обстоятельств и вести обычный образ жизни. Физическая нагрузка при условии достаточной дозы базального инсулина способствует снижению гликемии после еды, поэтому занятия физкультурой (ЛФК, индивидуальные тренировки) включают в лечебные мероприятия при сахарном диабете и проводят в период максимального повышения глюкозы в крови (через 1-1,5 ч после еды). Не планируемые физические нагрузки допустимы после приема дополнительных углеводов. Лечение ДКА. При I стадии ДКА (кетозе) ребенка госпитализируют в любое, лучше эндокринологическое отделение, и лечение начинают с оральной регидратации (щелочные минеральные воды, подслащенный чай, соки, ора-лит). Если ребенок не пьет или повторяется рвота, вводят внутривенно струйно изотонический раствор натрия хлорида 5 мл/кг с кокарбоксилазой. При необходимости в течение 1-3 ч проводят внутривенную капельную инфузию изотонического раствора натрия хлорида. Инсулин короткого действия назначают из расчета 1 ЕД/кг массы тела, а больному с СД длительностью более 1 года — 1,5 ЕД/кг, внутримышечно или подкожно. В первую инъекцию вводят У3-У4 суточной дозы, далее по 0,2-0,3 ЕД/кг каждые 4-6 ч с обязательным исследованием глюкозы крови, мочи, кетонурии перед каждым введением инсулина. В 1-е сутки пища должна быть механически щадящей, с достаточным количеством легкоусвояемых углеводов (жидкая каша, овощное и фруктовое пюре, соки, белый хлеб), ограничением жира. Со 2-го дня — диабетический стол. Для выведения кетоновых тел и предупреждения их обратного всасывания из желудочно-кишечного тракта делают очистительную клизму. Назначают витамины В6 (0,01 г 3 раза в день), В]2 (100-300 мкг 2 раза в неделю), эссенциале форте (1 капсула 1-2 раза в день) в течение 2-3 нед для ускорения окисления кетокислотв печени; препараты калия. Лечение ДКА II-III стадии осуществляют в реанимационном отделении любой больницы. Если медицинское учреждение находится на расстоянии 1 ч пути и более, дома или в машине скорой помощи начинают внутривенное введение изотонического раствора натрия хлорида со скоростью 10 мл/кг в час. Инсулин вводят по прибытии в больницу. Клиническую оценку состояния больного (состояние сознания, степень обезвоживания, симптомы шока и нарушения микроциркуляции, признаки ацидоза, объем мочи, динамика массы тела, признаки инфекции) проводят при поступлении и каждый час. Во всех порциях мочи исследуют уровень глюкозы и кетоновых тел. При установлении диагноза определяют уровень глюкозы крови, рН и газы венозной крови, дефицит оснований, уровни электролитов, мочевины, креатинина, гематокрит. Далее уровень глюкозы в крови определяют каждый час, а остальные показатели — каждые 2-4 ч, при необходимости чаще. Инфузионную терапию ДКА II-III стадии проводят изотоническим раствором натрия хлорида со скоростью 10-15 мл/кг в час (не более 500 мл в первый час). При наличии шока струйно вводят 0,9% раствор натрия хлорида в дозе 10 мл/кг с последующим его капельным введением. Одновременно через отдельную капельницу начинают инфузию инсулина короткого действия со скоростью 0,1 ЕД/кг/час. За первые сутки больной должен получить 100-120 мл жидкости на 1 кг массы тела. Скорость введения инсулина подбирают так, чтобы уровень глюкозы в крови снижался на 4-5 ммоль/л в час. При меньшей скорости снижения уровня глюкозы в крови дозу инсулина можно увеличить до 0,15-0,2-0,3 ЕД/кг в час. При быстром падении содержания глюкозы в крови сохраняют инфузию инсулина со скоростью не ниже 0,1 ЕД/кг в час, добавляя в инфузионные растворы глюкозу. Когда уровень глюкозы в крови снизится до 14 ммоль/л, переходят на введение 0,9% раствора натрия хлорида с 5% раствором глюкозы в соотношении 1: 1. При уровне гликемии ниже 12,0 ммоль/л вводят 5-10% раствор глюкозы. До ликвидации ацидоза целесообразно поддерживать концентрацию глюкозы в крови 8,5-11 ммоль/л за счет введения растворов глюкозы, но не снижения скорости введения инсулина (не менее 0,1 ЕД/кг/ч). Коррекцию ацидоза 4% раствором гидрокарбоната натрия проводят только в том случае, если через 4 ч после начала терапии рН крови сохраняется ниже 7,2. В случае необходимости (рН ниже 6,9) рекомендуют ввести в первый час лечения V3-1/4 рассчитанной дозы. При выраженных гемодинамических нарушениях, снижении АД у больного в прекоматозном и коматозном состоянии целесообразно начать инфузионную терапию с введения плазмы или плазмозаменяющих растворов. ДКА всегда сопровождается тяжелым дефицитом калия, даже если его уровень в плазме нормальный или несколько повышен. Если у ребенка нет анурии, одновременно с началом инфузии инсулина начинают введение препаратов калия (3-5 ммоль/кг за 24 ч). Уровень калия в крови следует поддерживать в пределах 4-5 ммоль/л и определять его концентрацию в крови, а также контролировать по данным ЭКГ каждые 2-4 ч. После ликвидации ацидоза и гиповолемии ребенка можно кормить. Обычно предлагают протертую пищу, богатую углеводами и с ограничением жира (каша, кисель, сок, белый хлеб). За 30 мин до еды вводят подкожно инсулин в дозе 0,25 ЕД/кг. Далее в течение последующего часа внутривенное введение инсулина и инфузионную терапию прекращают и переходят на один из режимов постоянного лечения. Антибиотики показаны только при сопутствующей инфекции. При гиперосмолярной коме инфузионную терапию начинают 0,45% раствором натрия хлорида, вводя его медленно: не более У4-1/5 суточного объема жидкости в первые 6 ч. После снижения осмолярности плазмы ниже 320 мОсм/л переходят на обычный режим инфузионной терапии. Стартовая доза инсулина, несмотря на высокую гликемию, не должна превышать 0,05 ЕД/кг/ч, так как такие больные отличаются высокой чувствительностью к инсулину, а при быстром снижении глюкозы может возникнуть отек мозга. При лактатацидотической коме лечение начинают с ликвидации ацидоза (4% раствор натрия гидрокарбоната), при выраженных циркуляторных нарушениях вводят плазму. При жировой инфильтрации печени дополнительно назначают гепато-трофические препараты в возрастных дозах (Легалон, ЛИВ-52, Карсил, Эссен-циале форте и др.), витамины В,, В6, В12, липоевую кислоту, желчегонные, ФТЛ. Лечение проводят длительно, курсами по 1-1,5 мес. В лечении ведущее значение имеет рациональная инсулинотерапия, при- Лечение ДМА. Начальные стадии ДМА обратимы. При хорошем контроле сахарного диабета, максимально возможной компенсации метаболических нарушений функциональные изменения могут быть обнаружены лишь через 15-20 лет от начала диабета. При плохой компенсации их находят уже через 2-5 лет. Поэтому в лечении и профилактике микроангиопатий важное значение имеет постоянный контроль сахарного диабета, применение высокоочи-щенных или человеческих инсулинов. Дополнительное значение имеет использование ангиопротекторов (трен-тал, ангинин, продектин), ингибиторов альдозоредуктазы (НИУК), липогроп-ных, антиоксидантов (витамин Е), витаминов В, РР и др. Все указанные препараты применяют курсами от 1,5-3 до 6-12 мес, только у больных с компенсированным сахарным диабетом.
Осложнения инсулинотерапии. Хроническая недостаточность инсулина с сохранением умеренной гипергликемии не приводит к значительным водно-элекролитным нарушениям, но вызывает задержку роста, полового развития, гепатомегалию, ранние сосудистые осложнения (синдром Мориака). Таблица 181 Симптомы гипогликемии у детей, больных диабетом, и рекомендации по лечению.
Хроническая передозировка инсулина (синдром Сомоджи) характеризуется повышенным аппетитом, ускорением роста, ожирением (часто по кушин-гоидному типу), гепатомегалией, склонностью к кетоацидозу, гипогликеми-ческим состояниям преимущественно ночью и утром, гипергликемией, ранним развитием микроангиопатий. Гипогликемия — снижение глюкозы крови ниже 3,0 ммоль/л — развивается у больного сахарным диабетом при введении избыточной дозы инсулина, сниженном поступлении или повышенном расходе глюкозы (нарушение диеты, физическая нагрузка). Симптомы гипогликемии и мероприятия по оказанию срочной помощи представлены в табл. 181. Повторные гипогликемии требуют неврологического обследования, дифференциальной диагностики с эпилепсией. «Инсулиновые отеки»- возможны при передозировке инсулина, особенно в сочетании с избыточной инфузионной терапией в ходе лечения ДКА. Особенно опасен отек мозга, появляющийся через несколько часов после начала лечения, обусловленный быстрым снижением уровня внеклеточной глюкозы при сохранении повышенной концентрации глюкозы в клетке и, следовательно, гипергидратацией клеток мозга. Клинически проявляется ухудшением состояния, появлением неврологической симптоматики, углублением комы у ребенка, получающего интенсивную терапию ДКА. При раннем распознавании эффективны внутривенное введение 10% раствора маннитола 1-1,5 г/кг, фуросемид. Отек может развиваться в легких, подкожной клетчатке, внутренних органах. Быстрая, в течение нескольких часов, прибавка массы тела у больного сахарным диабетом требует немедленного снижения доз инсулина и коррекции инфузионной терапии. Липодистрофии появляются в местах инъекций инсулина. Для их профилактики требуется часто менять места введения инсулина, пользоваться атравматическими иглами, очищенными препаратами. Прогноз. В настоящее время излечение больного СД невозможно, но следует стремиться к стойкой компенсации, которая достижима при постоянном контроле сахарного диабета, коррекции инсулинотерапии и диеты в домашних условиях. При длительной стойкой компенсации прогноз для жизни и трудоспособности благоприятный; он значительно ухудшается при наличии сосудистых осложнений. Разработка новых направлений в лечении сахарного диабета, во-первых, связана с совершенствованием методов введения инсулина (шприц-ручка, биостатор, микродозаторы инсулина), во-вторых, с трансплантацией поджелудочной железы или островковых клеток, в-третьих, с попытками иммуно-корригирующей терапии, дающей обнадеживающие результаты у взрослых больных. Профилактика. Профилактика СД I типа заключается в выделении и обследовании детей «группы риска». Это сибсы больных СД I типа, носители определенных гап-лотипов HLA. Обследование заключается в периодическом определении антител к островковым клеткам поджелудочной железы в сочетании с исследованием глюкозы натощак и в ходе СПТГ. Обсуждают возможность скрининга СД I типа, основанного на совокупности иммунологических и метаболических тестов. Появились первые сообщения о попытке превентивной иммуно-корригирующей терапии. Повышенная степень риска в отношении СД II типа имеется у сибсов больных, пациентов с ожирением, матерей, родивших детей с массой более 4,5 кг. Профилактика СД II типа заключается в профилактике и лечении ожирения, рациональном питании, активном образе жизни. Ранняя диагностика возможна при регулярном (1 раз в год) контроле глюкозы крови и мочи, проведении СПТГ, исследовании гликозилированного гемоглобина.
ОЖИРЕНИЕ. Ожирение — увеличение массы тела на 10% и более от максимальной по росту и полу за счет жировой ткани. Частота ожирения у детей колеблется от 5-8% у дошкольников до 20-22% у детей школьного возраста. Девочки имеют ожирение в 2-5 раз чаще, чем мальчики. Этиология Ожирение всегда развивается в результате повышенного поступления пищи и сниженного расхода энергии. Ведущее значение в формировании положительного энергетического баланса имеют генетически детерминированные особенности обмена: строение жировой ткани, например, повышенное количество адипоцитов и ускоренная дифференцировка их из фибробластов вследствие повышенной активности белков C/EBR, определяющих диффе-ренцировку адипоцитов или peroxisome proliferator activited receptor (PPAR) — рецепторов к ним; врожденная повышенная активность ферментов липогенеза и сниженная — липолиза, повышение образования жира из глюкозы при дефекте разделяющего протеина-2; сниженное образование в адипоцитах белка лептина (фактор, тормозящий центр голода в гипоталамусе) или дефект рецепторов к нему. Определенную роль в развитии ожирения имеют генетически детерминированные особенности обмена моноаминов в мозге, регулирующих пищевое поведение: норадреналин, у-аминомасляная кислота увеличивают, а дофамин, серотонин — снижают аппетит. На потребление пищи влияют пептиды мозга (опиоиды, соматолиберин, кортиколиберин, дипептид-цикло, длительно подавляющий аппетит дериват тиролиберина и др.). В реализации ожирения важное значение имеют внешние факторы: привычка к перееданию, насильственное кормление, избыточное количество углеводов и молока в пище, гиподинамия, иногда вынужденная при заболеваниях. Ожирение может развиваться при заболеваниях эндокринных желез (ги-перинсулинизм, гипотиреоз, гипогонадизм, гиперкортицизм), нарушении функции вентромедиальных и вентролатеральных ядер гипоталамуса, регулирующих аппетит и насыщение, при гипоксических, травматических, в том числе перинатальных поражениях мозга, опухолях, инфильтративных и воспалительных заболеваниях ЦНС, сопровождающихся булимией. Патогенез. Патогенез ожирения не зависит от его причины. Относительный или абсолютный избыток пищи, особенно богатой углеводами, приводит к гиперинсу-линизму. Инсулин, являясь главным липогенетическим гормоном, способствует синтезу триглицеридов в жировой ткани, а также оказывает анаболический эффект (ускорение роста, дифференцировки жировой и костной ткани). Избыточное накопление жира сопровождается вторичным изменением функции гипоталамуса — повышением секреции АКТГ и гиперкортицизмом, нарушением чувствительности вентромедиальных и вентролатеральных ядер к сигналам голода и сытости, перестройкой функции других эндокринных желез, центров терморегуляции, регуляции АД, нарушением секреции нейропептидов и моноаминов ЦНС, пептидов желудочно-кишечого тракта и т. д. Вторичное ожирение при эндокринных заболеваниях может быть следствием эндогенной или экзогенной гиперинсулинемии (инсулома, гиперкортицизм, хроническая передозировка инсулина при сахарном диабете), недостатка гормонов, усиливающих липолиз (гипотиреоз, гипопитуитаризм, гипогонадизм).
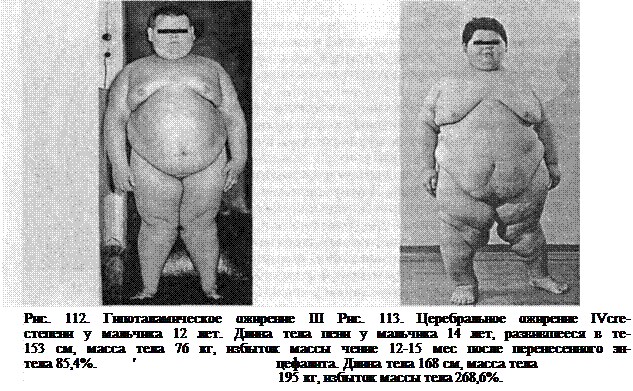
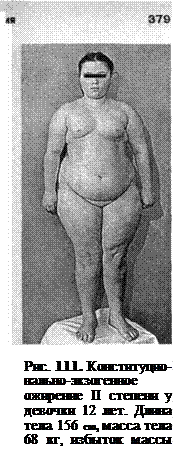
Выделяют первичное (конституционально-экзогенная, экзогенная, гипоталамическая и смешанная формы) и вторичное (при эндокринных заболеваниях) ожирение, а также наследственные синдромы с ожирением. Конституционально-экзогенное ожирение (рис. 111) развивается обычно в раннем возрасте, но может проявиться у подростков или у взрослых. Нередко ребенок рождается с крупной массой тела. У 60-85% больных родители или другие родственники имеют избыточную массу тела. Распределение подкожной жировой клетчатки равномерное, избыток массы тела редко превышает 50%, кожа нежная, эластичная. Дети, как правило, опережают сверстников в росте, имеют нормальный интеллект, физически активны. Течение заболевания может быть стабильным, но в периоде полового созревания у части больных, обычно у девочек, отмечается прогрессирование ожирения и развитие вторичного диэнцефального синдрома: быстро нарастает масса тела, появляются розовые, затем белые стрии на коже бедер, груди, живота, фолликулез, транзиторная, а в последующем постоянная артериальная гипертензия, головные боли, нарушения менструального цикла, а у мальчиков — задержка полового развития. Для мальчиков пубертатного возраста более характерно регрессирующее течение заболевания. Экзогенное (алиментарное, гиподинамическое) ожирение развивается у детей без наследственной предрасположенности при явном перекорме и/или вынужденном ограничении подвижности. Устранение причин приводит к нормализации веса. Гипоталамическое (диэнцефальное) ожирение обычно диагностируют в 5-6-летнем возрасте. В анамнезе часто отмечают осложненное течение перинатального периода (внутриутробная гипоксия, асфиксия, внутричерепная родовая травма, неонатальная гипогликемия). В первые месяцы жизни ребенок плохо прибавляет в массе тела, аппетит снижен, нередко его кормят во сне, насильно. Могут быть гипервозбудимость, срыгивания, рвоты, нарушения ритма сна и бодрствования. Во втором полугодии жизни обычно аппетит повышается, больной начинает хорошо, затем избыточно прибавлять массу тела, скорость роста увеличена. В 3-5 лет формируется ожирение, которое к 8-10-летнему возрасту достигает III—IV степени. Гипоталамическое ожирение может развиваться в любом возрасте через несколько месяцев после черепно-мозговой травмы, наркоза, инфекции ЦНС, вследствие опухоли гипоталамических отделов мозга.
Дата добавления: 2014-10-03 | Просмотры: 2178 | Нарушение авторских прав |

 Клиника.
Клиника.